Clear Sky Science · tr
KMT2A yeniden düzenlenmiş akut myeloid lösemide bir farklılaşma merkezinin Perturb‑seq haritası, sinerjik zayıflıkları ortaya koyuyor
Bu lösemi çalışması neden önemli
Akut myeloid lösemi, genellikle modern hedefli ilaçlara direnç gösteren hızlı ilerleyen bir kan kanseridir. Birçok yeni tedavi tek bir kanser sürücüsünü kapatmaya çalışır; hastalığın uyum sağlayıp geri dönmesi ise sık rastlanan bir durumdur. Bu çalışma, hastalar ve aileleri için hayati bir soruyu gündeme getiriyor: birer birer anahtarları kapatmak yerine, lösemi hücrelerini olgunlaşmamış bir durumda tutan tüm kontrol panelini haritalayabilir ve ardından kombinasyon terapilerinin tek bir ilaçtan çok daha iyi çalıştığı zayıf noktaları bulabilir miyiz?
Büyümeyi reddeden kanser hücreleri
Bu çalışmada bilim insanları, KMT2A adı verilen genin değişiklikleriyle işaretlenen yüksek riskli bir akut myeloid lösemi formuna odaklanıyor. Bu kanserlerde kan kök hücreleri olgunlaşmak yerine immatür bir evrede donup kalıyor; bu da enfeksiyonlarla savaşan beyaz kan hücrelerine dönüşmelerini engelliyor. DNA paketlenmesi üzerindeki kimyasal işaretler gibi davranan bireysel epigenetik düzenleyicileri hedefleyen önceki ilaçlar umut vermiş olsa da nadiren kalıcı remisyonda sonuçlandı. Ekip, lösemi hücrelerinin birkaç epigenetik sistemin birlikte çalışması yüzünden hayatta kaldığını; bu yüzden yalnızca birini engellemenin diğerlerinin işi devralmasına izin verdiğini düşündü. Bu işbirliğini gerçekten anlamak için kilit düzenleyiciler sırayla kapatıldığında binlerce bireysel hücrede neler olduğunu izleyebilecek bir yönteme ihtiyaçları vardı.
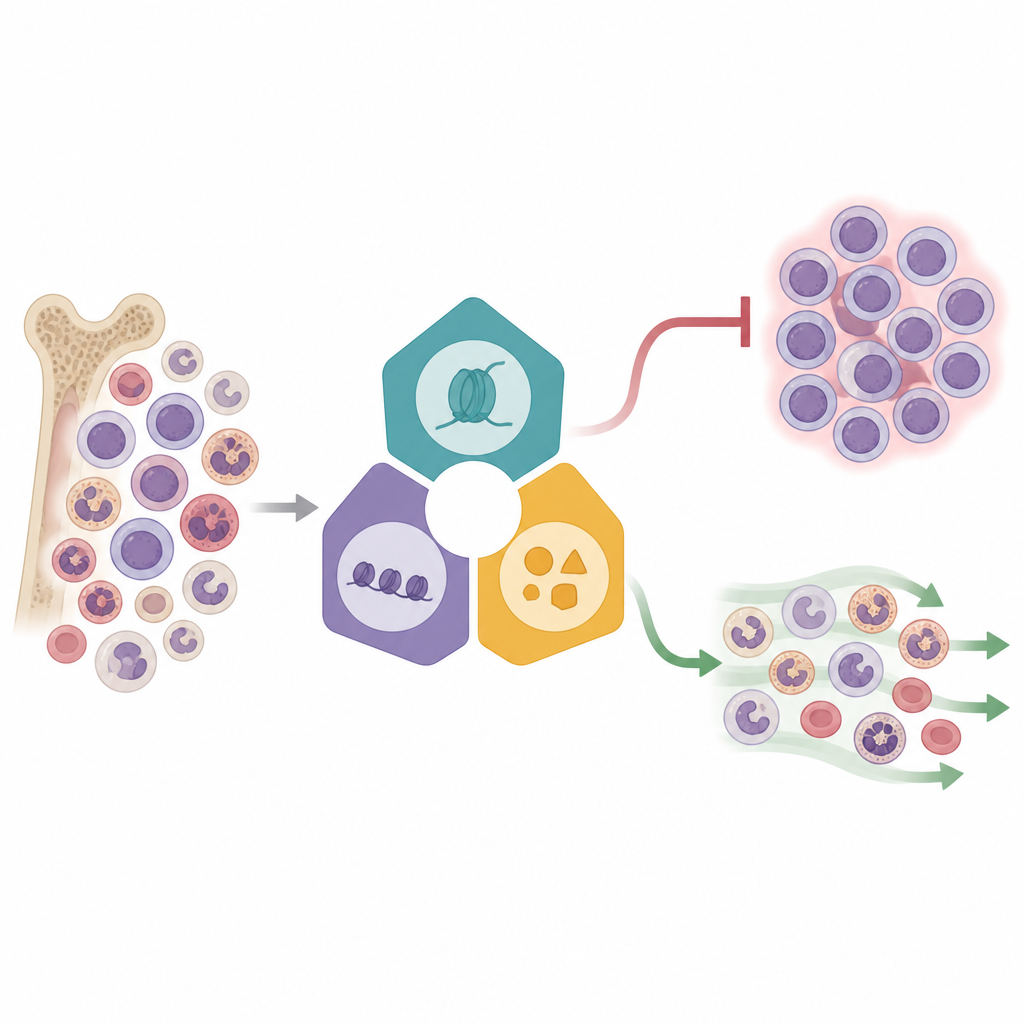
Aynı anda binlerce hücreyi okumak
Araştırmacılar, gen düzenlemeyi tek hücre RNA dizileme ile birleştiren güçlü bir yöntem olan Perturb‑seq’i kullandı. KMT2A yeniden düzenlenmiş bir lösemi hücre hattında, üç ana kompleksten seçilen 16 epigenetik düzenleyiciyi bozdu. Her düzenlenmiş hücre genetik bir barkod taşıyordu; bu da ekip için belirli bir düzenlemenin o hücrenin gen aktivite profiliyle eşleştirilmesini sağladı. Azaltılmış iki boyutlu bir alanda 31.000’den fazla hücreyi haritalayarak, hücrelerin hangi komplekse müdahale edildiğine göre gruplaştığını ve farklı yanıt desenleri ortaya koyduğunu gördüler. Özellikle Menin‑KMT2A füzyonuyla ilişkili faktörler ve ilgili enzimler bazı geniş çaplı gen aktivite değişimleri yaratırken, diğerlerinin daha ince etkileri vardı; bu da lösemi ağında farklı kontrol seviyelerine işaret ediyordu.
Hastanın hayatta kalmasını destekleyen gizli bir program
Hesaplamalı modelleme ile ekip karmaşık veriyi 17 gen programına indirgeyerek her birini koordineli bir gen aktivite deseni olarak temsil etti. Bir program öne çıktı: olgunlaşmamış hücrelerin tam işlevsel beyaz kan hücrelerine dönüşmesi süreci olan myeloid farklılaşmayla ilişkili bir gen seti. Yazarlar buna Myeloid Program adını verdi. Bu program, tam olgunluğa yakın normal kemik iliği hücrelerinde en aktif durumdaydı ve lösemi kök hücrelerini tanımlayan genlerle ters ilişkiliydi. Araştırmacılar büyük hasta veri kümelerini incelediklerinde, Myeloid Program’ın daha yüksek bazal aktivitesinin özellikle standart tedaviye iyi yanıt verme eğilimindeki hastalarda daha iyi genel sağkalım ile tutarlı bir şekilde ilişkilendirildiğini gördüler. Bu, agresif bir kanser içinde bile bazı hücrelerin daha iyi sonuçlarla ilişkili “olgunlaşmaya hazır” bir durumda daha yakın olabileceğini düşündürüyor.
Üç parçalı bir kontrol merkezi ve zayıf noktaları
Analiz, Menin, DOT1L ve KAT6A adındaki üç düzenleyicinin Myeloid Program’ı topluca baskılayan işlevsel bir merkez oluşturduğunu ortaya koydu. Bu genlerden herhangi biri bozulduğunda farklılaşma programı daha aktif hale geliyordu, ancak yalnızca kısmen. Ekip daha sonra her ortağı hedefleyen ilaçları denedi ve çarpıcı bir sinerji keşfetti. Bir Menin inhibitörünü KAT6A inhibitörüyle veya bir DOT1L inhibitörünü KAT6A inhibitörüyle eşleştirmek, tek ilaçlara kıyasla lösemi hücre büyümesini keskin şekilde azalttı ve Myeloid Program genlerinin ifadesini güçlü şekilde artırdı. Aynı zamanda, PCGF1 içeren başka bir kompleksin ters yönde bir etkisini de ortaya çıkardılar. PCGF1 kaybı, lösemi hücrelerini DOT1L inhibisyonuna karşı daha az duyarlı hale getirdi; bu da bazı epigenetik faktörlerin hedefli ilaçların etkisini köreltip dirence katkıda bulunabileceğini vurguluyor.
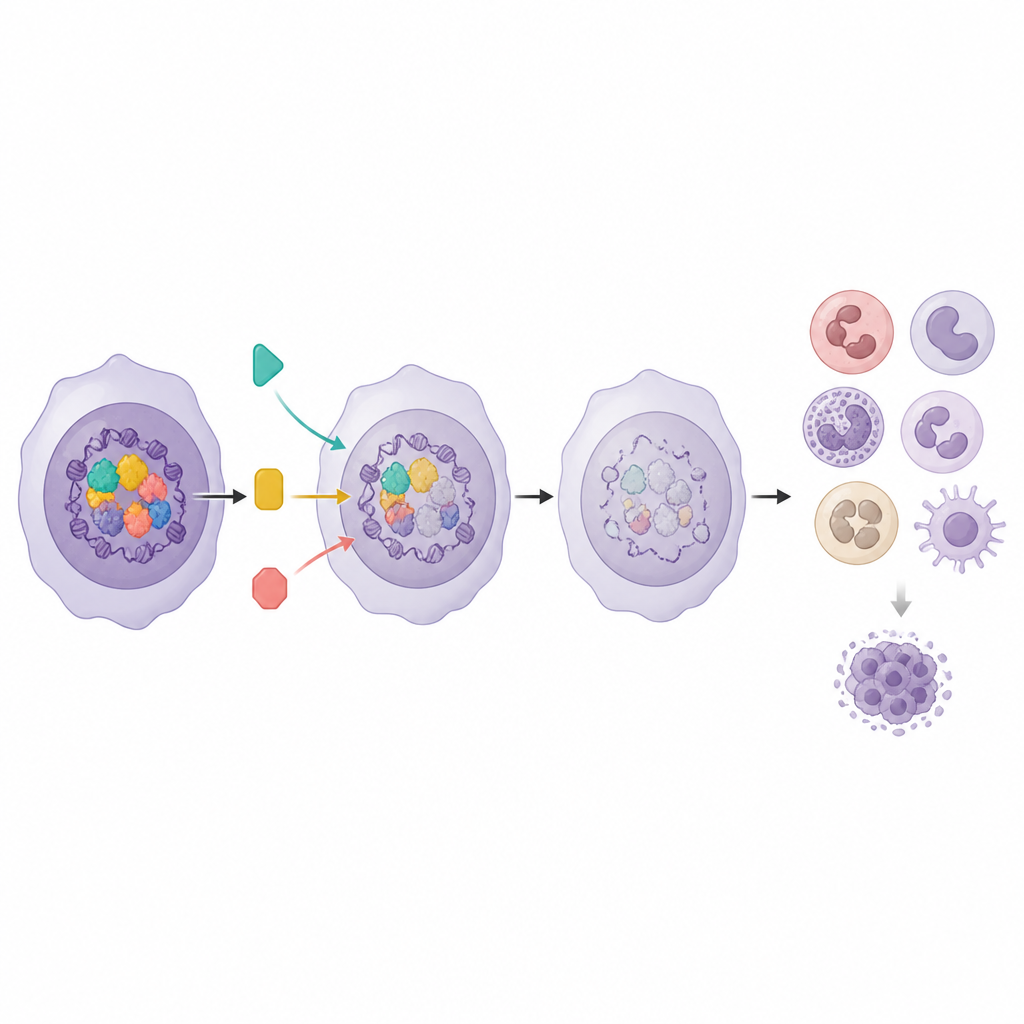
Akıllı kombinasyonları yönlendirmek için gen aktivitesini kullanmak
Myeloid Program hem hücre olgunlaşması hem de hasta sağkalımıyla bağlantılı olduğundan, araştırmacılar aktivitesinin hangi ilaçların en iyi çalışacağını öngörebileceğini de sorguladı. Hasta örneklerinde, Myeloid Program puanı daha yüksek olan lösemiler, özellikle MEK, AKT ve mTOR’u hedefleyen bazı sinyal yolakları inhibitörlerine daha duyarlıydı. Ekip, Myeloid Program’ı yükselten bir Menin inhibitörünü bu yolak inhibitörleriyle hücre modellerinde birleştirdiğinde, ilaç çiftleri belirgin bir sinerji gösterdi ve lösemi hücre büyümesini dizgevleyen dozları düşürdü. Aynı gen programı ayrıca gerçekten işbirliği yapan kombinasyonları, hücreleri yalnızca genel bir farklılaşmış duruma itenlerden ayırt etmeye de yardımcı oldu.
Gelecekteki lösemi bakımına etkileri
Halk diliyle özetle, bu çalışma tek bir “sihirli kurşun” arayışını aşarak, epigenetik düzenleyici gruplarının birlikte nasıl lösemi hücrelerini zararlı ve olgunlaşmamış bir durumda tuttuklarını haritalıyor. Hem daha iyi sağkalımı hem de artmış ilaç duyarlılığını öngören temel bir Myeloid Program’ı tanımlayarak ve bu programı baskılayan üç parçalı Menin‑KAT6A‑DOT1L merkezini belirleyerek, çalışma rasyonel kombinasyon terapileri için bir yol haritası sunuyor. Uzun vadede, hastalarda Myeloid Program aktivitesinin ölçülmesi doktorların hem olgunlaşma engelini kaldıran hem de kanserin yeni zayıflıklarından yararlanan ilaç eşleşmelerini seçmesine yardımcı olabilir; bu da akut myeloid lösemi için daha kalıcı ve kişiselleştirilmiş tedavilere yol açma potansiyeli taşıyor.
Atıf: Aryal, S., Curtiss, B.M., Zhou, X. et al. A Perturb-seq map of a differentiation hub reveals synergistic vulnerabilities in KMT2A-rearranged acute myeloid leukemia. Leukemia 40, 996–1008 (2026). https://doi.org/10.1038/s41375-026-02917-2
Anahtar kelimeler: akut myeloid lösemi, epigenetik tedavi, hücre farklılaşması, ilaç sinerjisi, tek hücre genomikleri