Clear Sky Science · zh
肿瘤微环境中的代谢网络:氨基酸与脂质代谢通路在癌症进展与治疗中的作用
为何肿瘤的“邻里”至关重要
癌症并非孤立生长。它存在于由支持细胞、免疫防御细胞和血管组成的繁忙环境中,所有细胞共同分享并争夺燃料。本文探讨癌细胞如何重塑蛋白质和脂类(即氨基酸与脂质)的利用,不仅在肿瘤细胞内,也在其整个周围环境中。理解这一隐秘的营养经济学有助于解释为什么某些肿瘤能逃避免疫系统并耐受治疗,同时也指向更聪明、更精确的治疗策略。
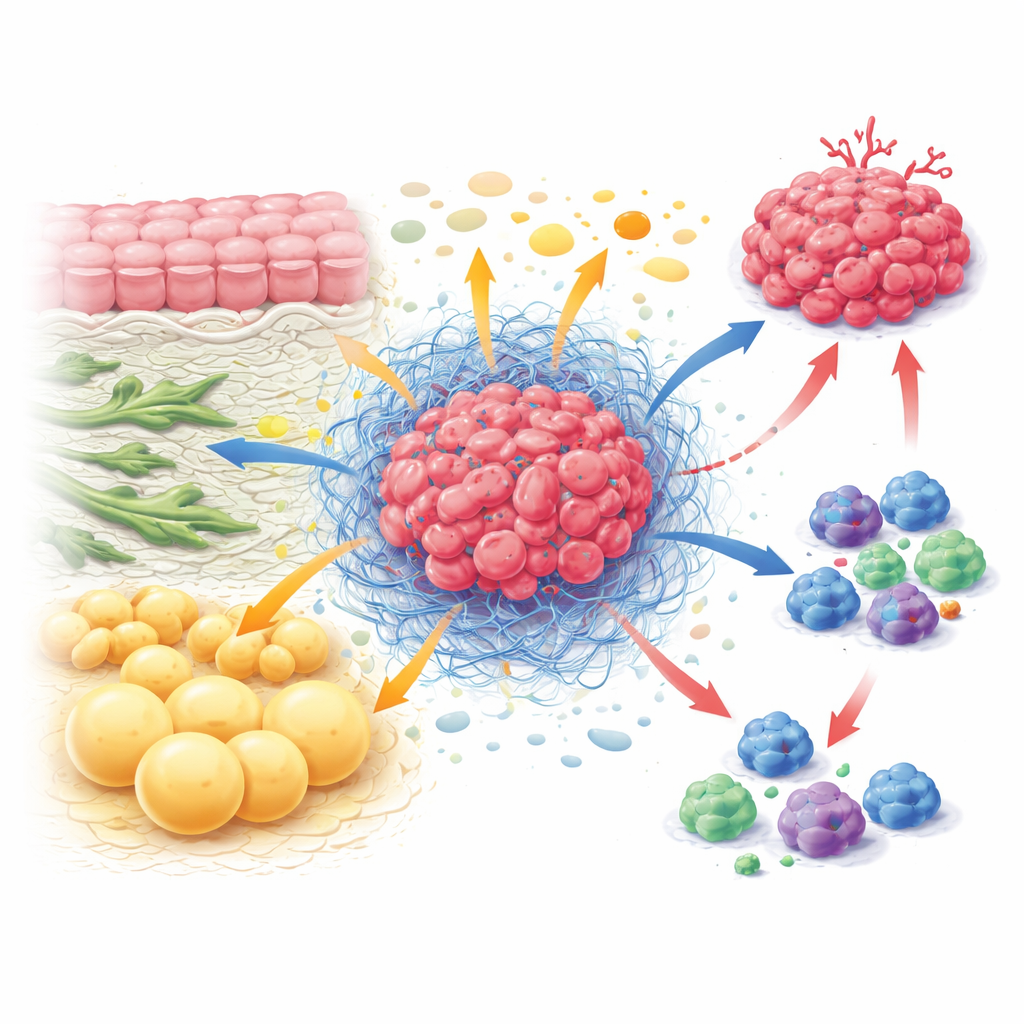
肿瘤内部的隐性经济
在肿瘤内部,癌细胞与塑造组织结构的成纤维细胞、试图攻击的免疫细胞、血管内皮细胞和脂肪细胞共存。它们一起形成肿瘤微环境,一种具有自身规则的生态系统。各类细胞并非各自为政,而是不断交换并竞争营养。成纤维细胞可以向癌细胞提供某些氨基酸等构建模块,同时通过使周围基质变硬来阻止免疫细胞进入。活跃的免疫细胞在分裂和杀伤时需要大量燃料,但常常发现自己处于饥饿状态,因为癌细胞和基质细胞往往优先获取资源。这种关于营养的持续拉扯,有助于肿瘤生长,同时削弱机体防御。
燃料之争:氨基酸作为武器
综述强调了几种既是食物又是信号分子的关键氨基酸。谷氨酰胺、精氨酸、色氨酸和支链氨基酸对癌细胞和免疫细胞都至关重要。肿瘤常常增强运输系统和相关酶的活性,使其能够大量摄取这些营养,导致杀手T细胞和自然杀伤细胞可用资源不足。同时,诸如髓系细胞和成纤维细胞等支持性细胞可以有意分解精氨酸和色氨酸,产生抑制免疫反应的代谢产物并促进耐受肿瘤的调节性T细胞。在某些小环境中,细胞也会共享氨基酸以帮助癌细胞抵抗治疗,或从受损组织回收氨基酸,形成对化疗和靶向药物的局部耐受口袋。
脂质:燃料、屏障与信号分子
脂质——脂肪、脂肪酸、胆固醇及相关分子——在这一生态系统中同样扮演重要角色。癌细胞既增加脂质合成又增强脂质氧化,利用脂质构建膜、储存能量并抵抗应激。附近的脂肪细胞和成纤维细胞可以释放脂肪酸,肿瘤易于摄取并将其存入脂质滴——这些微小储藏库可保护细胞免受毒性应激和多种药物的伤害。肿瘤中的免疫细胞也被推向高度依赖脂质代谢的状态。调节性T细胞和某些巨噬细胞利用脂肪酸存活并保持抑制性,而负荷过重的杀手T细胞则变得耗竭。特殊的脂质信使分子(如溶血磷脂酸)进一步刺激肿瘤生长、引导癌细胞向远处器官转移,并将免疫细胞排斥在肿瘤核心之外。
随空间、时间与治疗而变化
肿瘤内的代谢并不均一。从营养充足的外缘到饥饿的肿瘤核心,氧气和营养水平存在差异,而不同转移器官也提供不同的营养组合。因此,某些区域偏好糖代谢,另一些则更多依赖谷氨酰胺或脂质,而这些模式会随着肿瘤生长或接受治疗而发生变化。当治疗切断一种燃料途径时,肿瘤往往转而利用另一种,或更多依赖成纤维细胞和脂肪细胞的支持。同样的代谢转变也能通过表观遗传修饰改变基因的开启或关闭,锁定具侵袭性或免疫抑制性的状态。这种灵活性使得通过阻断单一路径来遏制癌症变得困难。
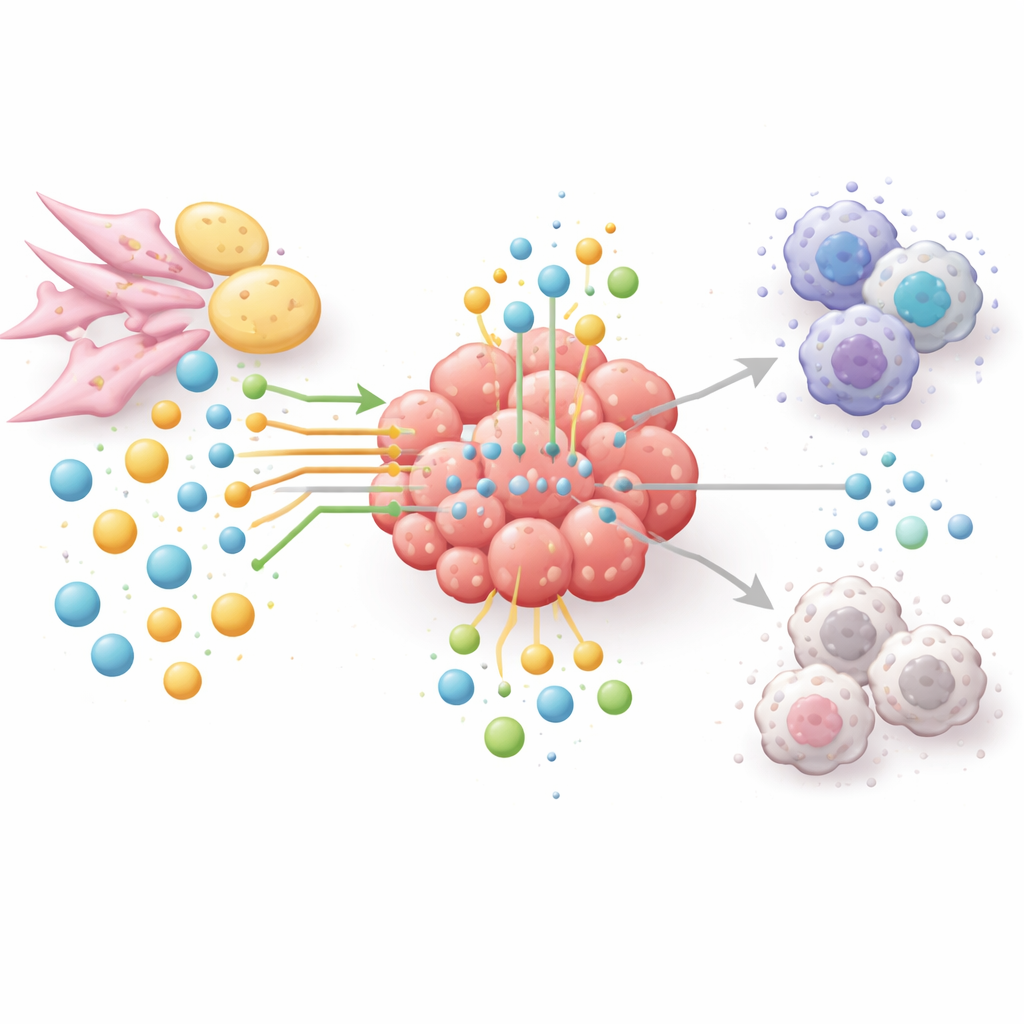
以新方式饿死肿瘤,而非伤害患者
鉴于氨基酸和脂质通路将肿瘤生长、免疫逃逸与治疗耐受联系在一起,作者主张采用基于网络的方法,而非单药针对单一酶的策略。实验性疗法目前旨在在精心选择的肿瘤中降低精氨酸或谷氨酰胺水平、抑制脂质合成或脂肪氧化相关酶,或阻断色氨酸分解及其免疫抑制性产物。许多策略正与免疫检查点抑制剂联合使用,以同时削弱肿瘤并重新激活T细胞。为选择合适的组合和患者,领域正在转向空间代谢组学、液体活检和人工智能,以绘制谁在肿瘤内部何时何地消耗何种营养的图谱。简言之,文章总结道,要战胜癌症不仅需要直接攻击肿瘤细胞,还需要重塑保护它们的整体营养网络。
引用: Sung, Y., Kim, D.K., Kim, J.S. et al. Metabolic networks in the tumor microenvironment: roles of amino acid and lipid metabolism pathways in cancer progression and therapy. Exp Mol Med 58, 1128–1148 (2026). https://doi.org/10.1038/s12276-026-01697-0
关键词: 肿瘤微环境, 癌症代谢, 氨基酸, 脂质代谢, 免疫疗法