Clear Sky Science · pt
Redes metabólicas no microambiente tumoral: papéis das vias de metabolismo de aminoácidos e lipídios na progressão do câncer e na terapia
Por que o bairro do tumor importa
O câncer não cresce isoladamente. Vive em um bairro movimentado de células de suporte, defensores imunes e vasos sanguíneos, todos compartilhando e disputando combustível. Este artigo explora como os cânceres reprogramam o uso de proteínas e gorduras — decompostas em aminoácidos e lipídios — não apenas dentro das células tumorais, mas por todo o seu entorno. Compreender essa economia oculta de nutrientes ajuda a explicar por que alguns tumores escapam do sistema imune e resistem ao tratamento, além de apontar para terapias mais inteligentes e precisas.
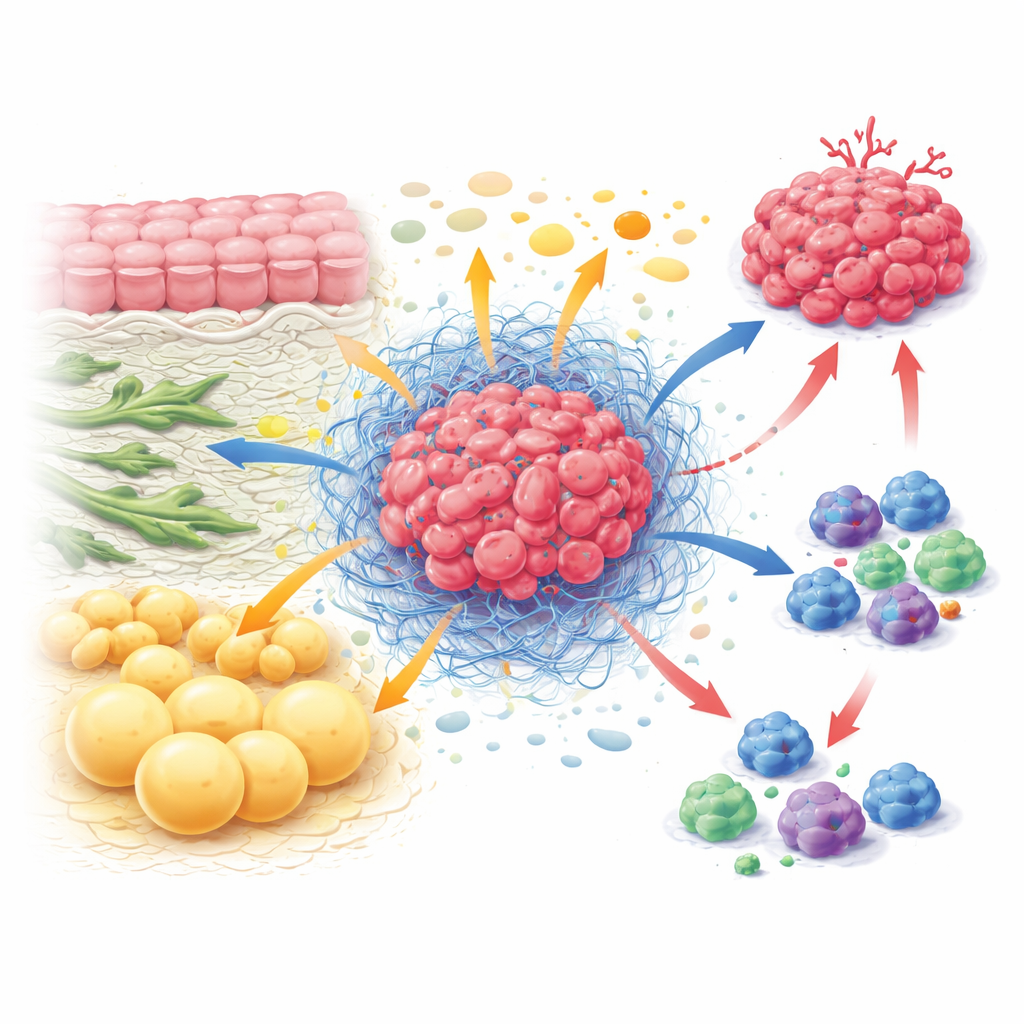
A economia oculta dentro de um tumor
Dentro de um tumor, células cancerosas coexistem com fibroblastos que moldam a estrutura do tecido, células imunológicas que tentam atacar, células de vasos sanguíneos e adipócitos. Juntos formam o microambiente tumoral, um tipo de ecossistema com regras próprias. Em vez de cada tipo celular agir isoladamente, elas trocam e competem constantemente por nutrientes. Fibroblastos podem nutrir as células cancerosas com blocos de construção, como certos aminoácidos, enquanto também endurecem o tecido circundante para dificultar a entrada de células imunes. Células imunológicas, quando ativas, precisam de grandes quantidades de combustível para se dividir e matar, mas frequentemente se veem privadas porque células tumorais e do estroma têm acesso prioritário. Essa luta contínua por nutrientes ajuda os tumores a crescerem enquanto enfraquece as defesas do corpo.
Guerras por combustível: aminoácidos como armas
A revisão destaca vários aminoácidos-chave que atuam tanto como alimento quanto como sinais. Glutamina, arginina, triptofano e aminoácidos de cadeia ramificada são cruciais para células cancerosas e imunológicas. Tumores frequentemente aumentam sistemas de transporte e enzimas que lhes permitem absorver esses nutrientes, deixando pouco para células T citotóxicas e células NK. Ao mesmo tempo, células de suporte como mieloides e fibroblastos podem deliberadamente degradar arginina e triptofano, gerando subprodutos que acalmam respostas imunes e incentivam células T reguladoras que toleram o tumor. Em alguns nichos, células também compartilham aminoácidos para ajudar o câncer a sobreviver ao tratamento, ou os reciclam de tecido danificado, criando bolsões de resistência à quimioterapia e a drogas alvo.
Gordura como combustível, escudo e sinal
Lipídios — gorduras, ácidos graxos, colesterol e moléculas relacionadas — desempenham papéis igualmente importantes nesse ecossistema. Células cancerosas aumentam tanto a produção quanto a oxidação de lipídios, usando gorduras para construir membranas, armazenar energia e resistir ao estresse. Adipócitos e fibroblastos próximos podem liberar ácidos graxos que os tumores prontamente importam e armazenam em gotas lipídicas, pequenos depósitos que protegem contra estresse tóxico e muitas drogas. Células imunes no tumor também são empurradas a depender fortemente do metabolismo lipídico. Células T reguladoras e certos macrófagos usam ácidos graxos para sobreviver e manter função supressora, enquanto células T efetoras sobrecarregadas tornam-se exauridas. Mensageiros lipídicos especiais, como a lisofosfatidato, estimulam ainda mais o crescimento tumoral, orientam a disseminação do câncer para órgãos distantes e afastam células imunes do núcleo tumoral.
Mudando no espaço, no tempo e com o tratamento
O metabolismo em um tumor não é homogêneo. Níveis de oxigênio e nutrientes variam da borda bem nutrida ao núcleo faminto, e diferentes órgãos que hospedam metástases oferecem misturas de nutrientes distintas. Como resultado, algumas regiões favorecem a queima de glicose, outras dependem mais de glutamina ou gorduras, e esses padrões mudam conforme o tumor cresce ou enfrenta terapia. Quando tratamentos cortam um combustível, tumores frequentemente mudam para outro ou passam a depender mais da ajuda de fibroblastos e adipócitos. As mesmas mudanças metabólicas também podem alterar como genes são ativados ou silenciados por marcas epigenéticas, consolidando estados agressivos ou imunosupressivos. Essa flexibilidade dificulta deter o câncer bloqueando apenas uma via.
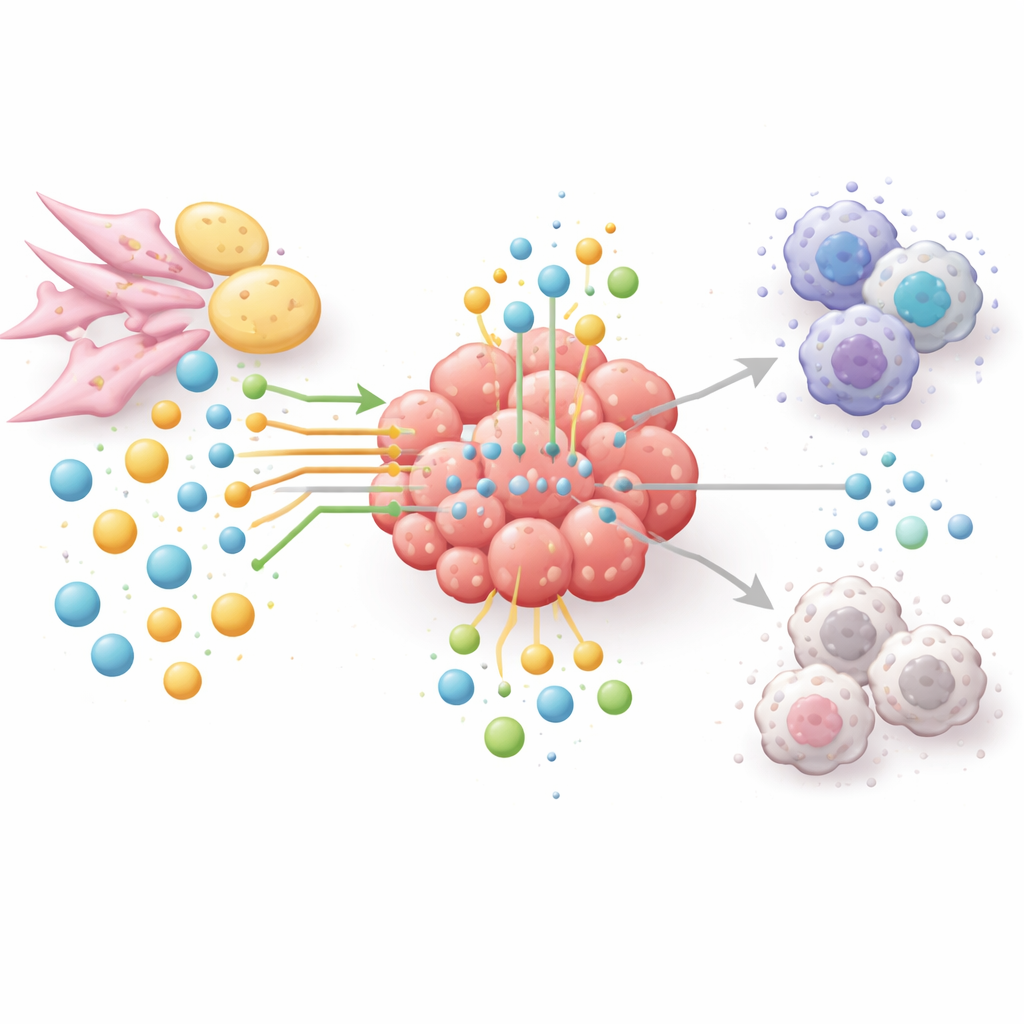
Novas formas de esfomear o tumor, não o paciente
Porque vias de aminoácidos e lipídios conectam crescimento tumoral, escape imune e resistência ao tratamento, os autores defendem uma abordagem em rede em vez de soluções de um fármaco-por-uma-enziema. Terapias experimentais agora visam reduzir arginina ou glutamina em tumores cuidadosamente selecionados, bloquear enzimas de síntese ou oxidação de lipídios, ou interromper a degradação do triptofano e seus produtos que abafam a resposta imune. Muitas dessas estratégias estão sendo combinadas com drogas de checkpoint imune para enfraquecer o tumor e reenergizar células T. Para escolher as combinações e os pacientes certos, o campo recorre a metabolômica espacial, biópsias líquidas e inteligência artificial para mapear quem está consumindo o quê, onde e quando dentro dos tumores. Em termos simples, o artigo conclui que vencer o câncer exigirá não apenas atacar diretamente as células tumorais, mas também reconfigurar toda a rede de nutrientes que as abriga.
Citação: Sung, Y., Kim, D.K., Kim, J.S. et al. Metabolic networks in the tumor microenvironment: roles of amino acid and lipid metabolism pathways in cancer progression and therapy. Exp Mol Med 58, 1128–1148 (2026). https://doi.org/10.1038/s12276-026-01697-0
Palavras-chave: microambiente tumoral, metabolismo do câncer, aminoácidos, metabolismo lipídico, imunoterapia