Clear Sky Science · sv
Metabola nätverk i tumörmikromiljön: roller för aminosyra- och lipidmetaboliska vägar i cancerprogression och terapi
Varför tumörens grannskap spelar roll
Cancer växer inte i isolering. Den lever i ett livligt grannskap av stödjeceller, immundefenderare och blodkärl—alla delar och slåss om bränsle. Denna artikel undersöker hur cancer omskriver användningen av proteiner och fetter—uppdelat i aminosyror och lipider—inte bara inne i tumörcellerna utan i hela deras omgivning. Att förstå denna dolda näringsekonomi hjälper till att förklara varför vissa tumörer undkommer immunsystemet och blir resistenta mot behandling, och det pekar mot smartare, mer precisa terapier.
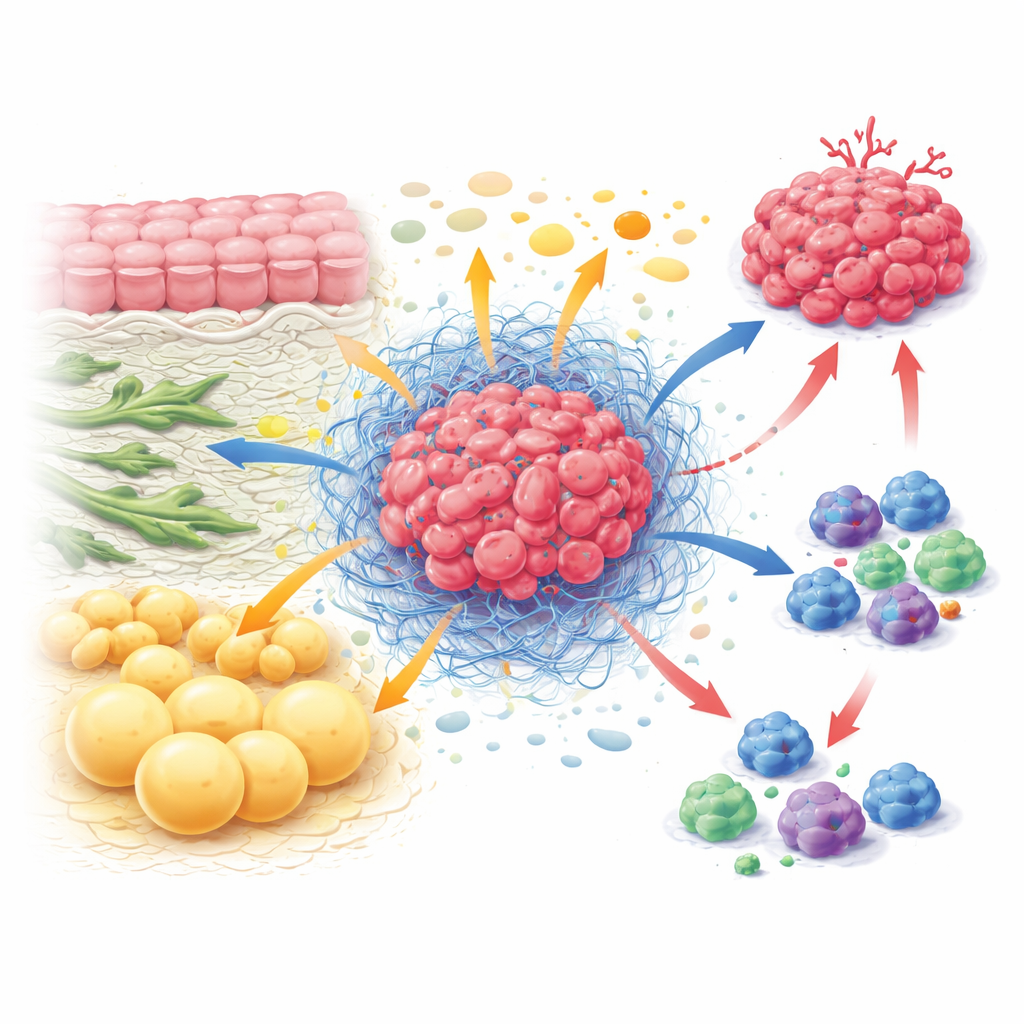
Den dolda ekonomin inne i en tumör
Inne i en tumör samexisterar cancerceller med fibroblaster som formar vävnadsstrukturen, immunceller som försöker angripa, blodkärlsceller och fettceller. Tillsammans bildar de tumörmikromiljön, en slags ekosystem med egna regler. I stället för att varje celltyp arbetar för sig, byter de ständigt ut och konkurrerar om näringsämnen. Fibroblaster kan mata cancerceller med byggstenar som vissa aminosyror, samtidigt som de gör omgivande vävnad styvare så att immunceller inte lätt kan ta sig in. Immunceller, när de är aktiva, behöver stora mängder bränsle för att dela sig och döda, men finner sig ofta uttömda eftersom cancer- och stromaceller får prioriterad tillgång. Detta konstanta dragkamp om näringsämnen bidrar till tumörtillväxt samtidigt som kroppens försvar försvagas.
Bränslekrig: aminosyror som vapen
Översikten lyfter fram flera nyckelaminosyror som fungerar både som näring och signaler. Glutamin, arginin, tryptofan och grenade aminosyror är avgörande för både cancerceller och immunceller. Tumörer ökar ofta transportörer och enzymer som låter dem suga åt sig dessa näringsämnen, vilket lämnar för lite åt mördande T‑celler och natural killer‑celler. Samtidigt kan stödjeceller som myeloida celler och fibroblaster medvetet bryta ner arginin och tryptofan och bilda biprodukter som dämpar immunsvaret och uppmuntrar regulatoriska T‑celler som tolererar tumören. I vissa nischer delar celler också aminosyror för att hjälpa cancern överleva behandling eller återvinner dem från skadad vävnad, vilket skapar fickor av resistens mot kemoterapi och målinriktade läkemedel.
Fett som bränsle, sköld och signal
Lipider—fetter, fettsyror, kolesterol och relaterade molekyler—spelar lika viktiga roller i detta ekosystem. Cancerceller ökar både fettproduktion och fettförbränning, och använder fetter för att bygga membran, lagra energi och motstå stress. Närliggande fettceller och fibroblaster kan frisätta fettsyror som tumörer lätt importerar och packar in i lipiddroppar, små lagringsdepåer som skyddar mot toxisk stress och många läkemedel. Immunceller i tumören pressas också mot ett tungt beroende av fettmetabolism. Regulatoriska T‑celler och vissa makrofager använder fettsyror för att överleva och förbli suppressiva, medan överbelastade mördande T‑celler blir utmattade. Särskilda lipidsignaler, såsom lysofosfatidinsyra, stimulerar vidare tumörtillväxt, vägleder cancer till spridning i avlägsna organ och avvisar immunceller från tumörkärnan.
Förändring över rum, tid och behandling
Metabolismen i en tumör är inte enhetlig. Syre- och näringsnivåer varierar från den välmatade yttre randen till den svältande kärnan, och olika organ som är värdar för metastaser erbjuder skilda näringsblandningar. Som ett resultat gynnas vissa regioner av sockermetabolism, andra förlitar sig mer på glutamin eller fetter, och dessa mönster skiftar när tumören växer eller utsätts för terapi. När behandlingar stänger av ett bränsle, växlar tumörer ofta till ett annat eller förlitar sig mer på hjälp från fibroblaster och fettceller. Samma metaboliska skiften kan också ändra hur gener slås på eller av via epigenetiska markörer, vilket låser in aggressiva eller immunsuppressiva tillstånd. Denna flexibilitet gör det svårt att stoppa cancer genom att blockera en enda väg.
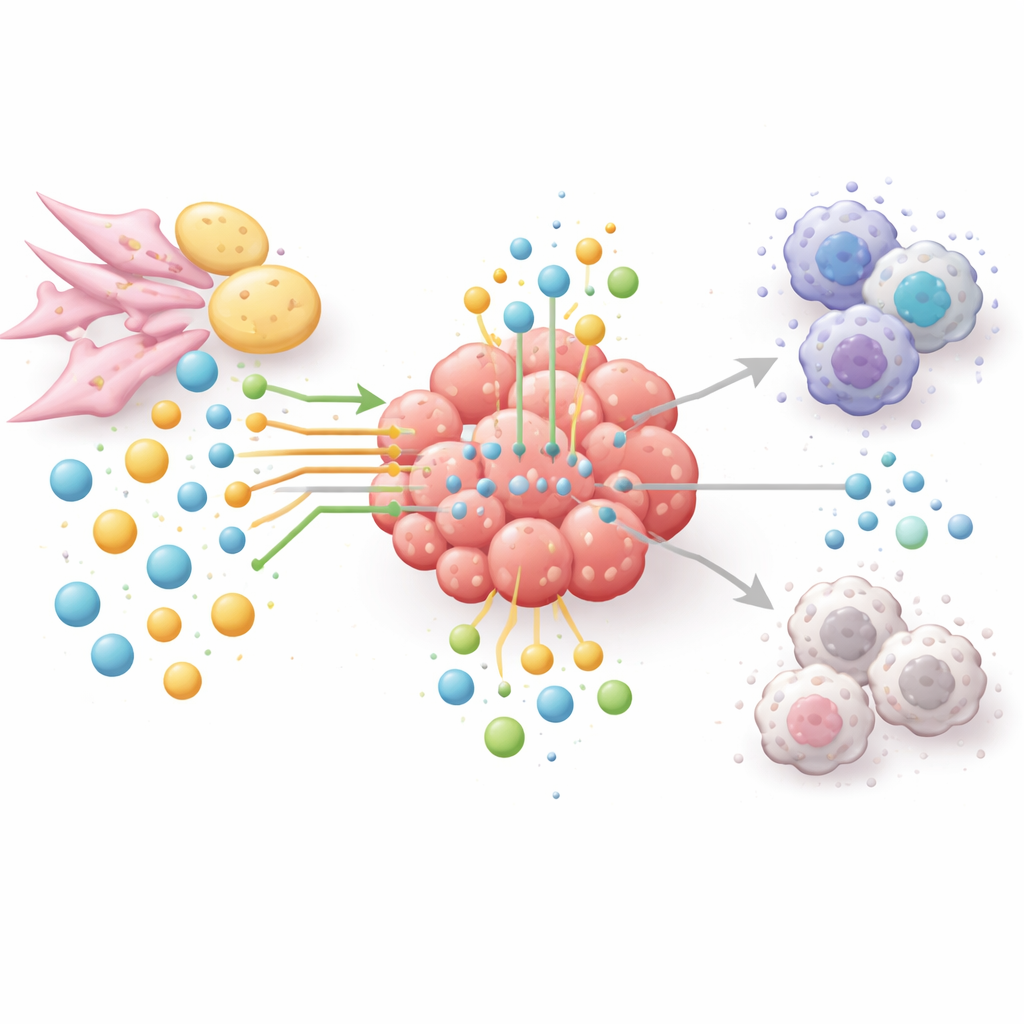
Nya sätt att svälta ut tumören, inte patienten
Eftersom aminosyra‑ och lipidvägar länkar tumörtillväxt, immundegörelse och behandlingsresistens menar författarna att man bör anta ett nätverksbaserat angreppssätt snarare än en läkemedel‑per‑enzym‑taktik. Experimentella terapier syftar nu till att sänka arginin eller glutamin i noggrant utvalda tumörer, blockera fett‑syntes eller fettförbränningsenzymer, eller stänga av tryptofanbrytning och dess immundämpande produkter. Många av dessa strategier kombineras med immuncheckpoint‑läkemedel för att både försvaga tumören och återuppväcka T‑celler. För att välja rätt kombinationer och patienter vänder sig fältet till spatial metabolomik, likvidbiopsier och artificiell intelligens för att kartlägga vem som äter vad, var och när inne i tumörer. I enkla termer drar artikeln slutsatsen att det som krävs för att vinna över cancer inte bara är att angripa tumörceller direkt utan också att omskapa hela näringsnätverket som skyddar dem.
Citering: Sung, Y., Kim, D.K., Kim, J.S. et al. Metabolic networks in the tumor microenvironment: roles of amino acid and lipid metabolism pathways in cancer progression and therapy. Exp Mol Med 58, 1128–1148 (2026). https://doi.org/10.1038/s12276-026-01697-0
Nyckelord: tumörmikromiljö, cancermetabolism, aminosyror, lipidmetabolism, immunterapi