Clear Sky Science · es
Redes metabólicas en el microambiente tumoral: roles de las vías de metabolismo de aminoácidos y lípidos en la progresión y terapia del cáncer
Por qué importa el vecindario del tumor
El cáncer no crece de forma aislada. Vive en un vecindario activo de células de soporte, defensores inmunitarios y vasos sanguíneos, todos compartiendo y compitiendo por combustible. Este artículo explora cómo los cánceres reconfiguran el uso de proteínas y grasas —descompuestas en aminoácidos y lípidos— no solo dentro de las células tumorales, sino en todo su entorno. Comprender esta economía oculta de nutrientes ayuda a explicar por qué algunos tumores eluden al sistema inmune y resisten los tratamientos, y apunta hacia terapias más inteligentes y precisas.
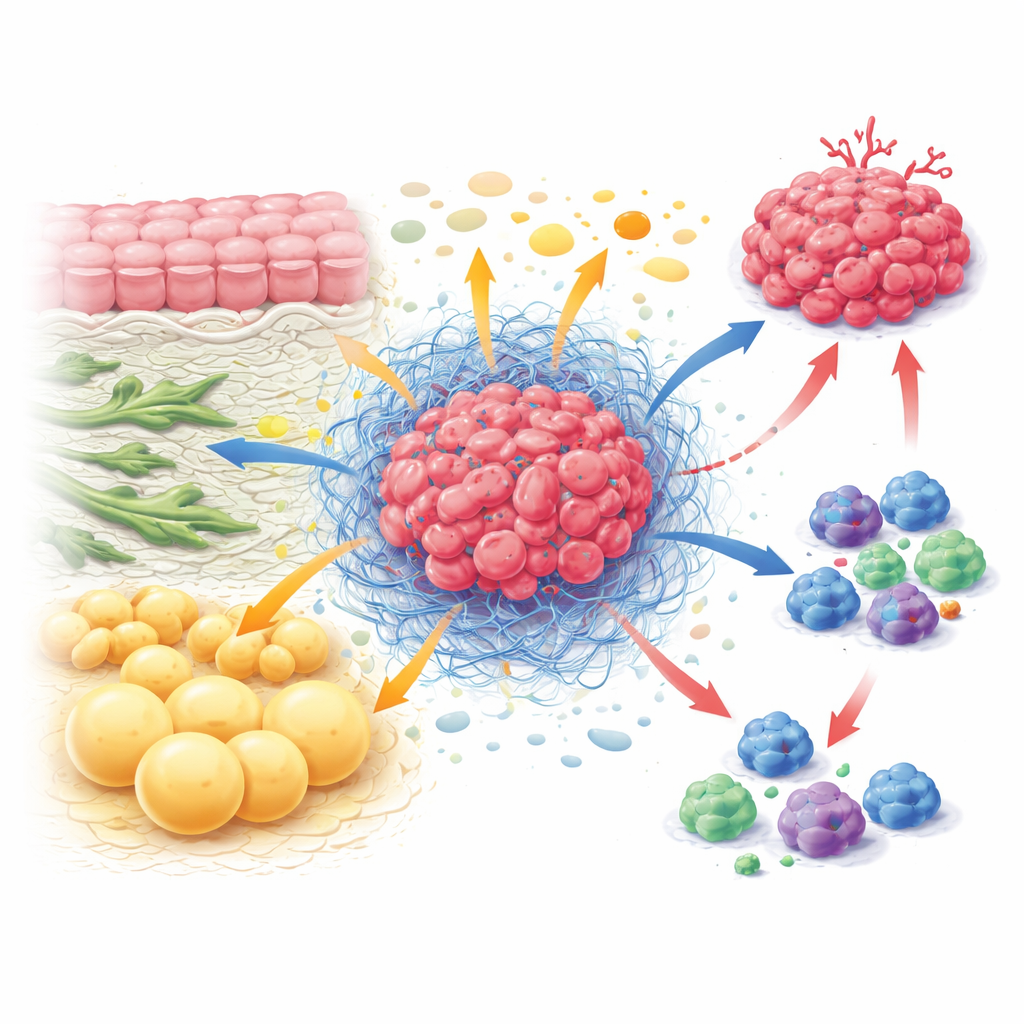
La economía oculta dentro de un tumor
Dentro de un tumor, las células cancerosas coexisten con fibroblastos que dan forma a la estructura tisular, células inmunitarias que intentan atacar, células vasculares y adipocitos. Juntos forman el microambiente tumoral, una especie de ecosistema con sus propias reglas. En lugar de que cada tipo celular actúe de forma independiente, intercambian y compiten continuamente por nutrientes. Los fibroblastos pueden alimentar a las células cancerosas con bloques de construcción como ciertos aminoácidos, mientras también endurecen el tejido circundante para que las células inmunitarias no puedan entrar con facilidad. Las células inmunitarias, cuando están activas, necesitan grandes cantidades de combustible para dividirse y matar, pero a menudo se encuentran hambrientas porque las células tumorales y estromales tienen acceso prioritario. Este empuje y tironeo constante sobre los nutrientes ayuda a que los tumores crezcan a la vez que debilita las defensas del organismo.
Guerras por el combustible: los aminoácidos como armas
La revisión destaca varios aminoácidos clave que actúan tanto como alimento como señales. La glutamina, la arginina, el triptófano y los aminoácidos de cadena ramificada son cruciales tanto para las células cancerosas como para las inmunitarias. Los tumores a menudo aumentan los sistemas de transporte y las enzimas que les permiten absorber estos nutrientes, dejando muy poco para las células T citotóxicas y las células NK. Al mismo tiempo, células de soporte como las mieloides y los fibroblastos pueden degradar deliberadamente arginina y triptófano, generando subproductos que apagan las respuestas inmunitarias y fomentan células T reguladoras que toleran el tumor. En algunos nichos, las células también comparten aminoácidos para ayudar al cáncer a sobrevivir al tratamiento, o los reciclan a partir de tejido dañado, creando bolsillos de resistencia a la quimioterapia y a fármacos dirigidos.
La grasa como combustible, escudo y señal
Los lípidos —grasas, ácidos grasos, colesterol y moléculas relacionadas— desempeñan papeles igualmente importantes en este ecosistema. Las células cancerosas aumentan tanto la producción de grasas como su degradación, utilizando lípidos para construir membranas, almacenar energía y resistir el estrés. Las células adiposas y los fibroblastos cercanos pueden liberar ácidos grasos que los tumores importan con facilidad y almacenan en gotas lipídicas, pequeños depósitos que protegen frente al estrés tóxico y a muchos fármacos. Las células inmunitarias en el tumor también se ven empujadas hacia una fuerte dependencia del metabolismo lipídico. Las células T reguladoras y ciertos macrófagos usan ácidos grasos para sobrevivir y mantenerse supresores, mientras que las células T citotóxicas sobrecargadas se agotan. Mensajeros lipídicos especiales, como el lisofosfatidato, estimulan además el crecimiento tumoral, guían la diseminación del cáncer a órganos distantes y repelen a las células inmunitarias del núcleo tumoral.
Cambios según el espacio, el tiempo y el tratamiento
El metabolismo en un tumor no es uniforme. Los niveles de oxígeno y nutrientes varían desde el borde bien nutrido hasta el núcleo hambriento, y distintos órganos que alojan metástasis ofrecen mezclas de nutrientes diferentes. Como resultado, algunas regiones favorecen la quema de azúcar, otras dependen más de la glutamina o de las grasas, y estos patrones cambian a medida que el tumor crece o enfrenta terapia. Cuando los tratamientos bloquean un combustible, los tumores a menudo cambian a otro o dependen más de la ayuda de fibroblastos y adipocitos. Los mismos cambios metabólicos también pueden alterar cómo se activan o silencian genes mediante marcas epigenéticas, consolidando estados agresivos o supresores inmunitarios. Esta flexibilidad dificulta detener el cáncer bloqueando una sola vía.
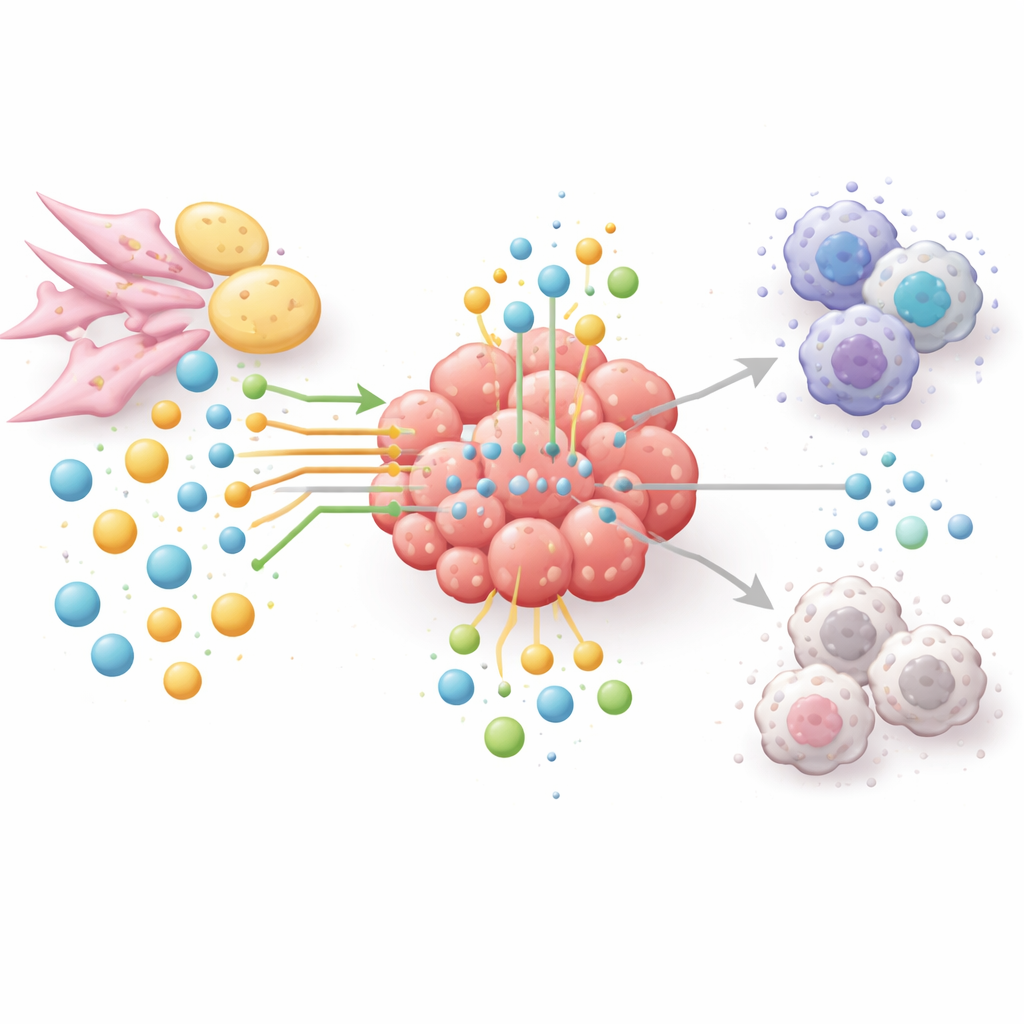
Nuevas formas de dejar sin comida al tumor, sin dañar al paciente
Puesto que las vías de aminoácidos y lípidos conectan el crecimiento tumoral, la evasión inmune y la resistencia al tratamiento, los autores abogan por un enfoque basado en redes en lugar de soluciones de un fármaco para una enzima. Las terapias experimentales intentan ahora reducir la arginina o la glutamina en tumores cuidadosamente seleccionados, bloquear enzimas de síntesis o degradación de grasas, o inhibir la descomposición del triptófano y sus productos que apagan la respuesta inmune. Muchas de estas estrategias se combinan con fármacos de puntos de control inmunitario para debilitar el tumor y reactivar las células T. Para elegir las combinaciones y los pacientes adecuados, el campo recurre a la metabolómica espacial, biopsias líquidas e inteligencia artificial para mapear quién come qué, dónde y cuándo dentro de los tumores. En términos sencillos, el artículo concluye que ganar contra el cáncer requerirá no solo atacar directamente las células tumorales, sino también reconfigurar toda la red de nutrientes que las protege.
Cita: Sung, Y., Kim, D.K., Kim, J.S. et al. Metabolic networks in the tumor microenvironment: roles of amino acid and lipid metabolism pathways in cancer progression and therapy. Exp Mol Med 58, 1128–1148 (2026). https://doi.org/10.1038/s12276-026-01697-0
Palabras clave: microambiente tumoral, metabolismo del cáncer, aminoácidos, metabolismo de lípidos, inmunoterapia