Clear Sky Science · it
Reti metaboliche nel microambiente tumorale: ruoli dei percorsi del metabolismo degli aminoacidi e dei lipidi nella progressione del cancro e nella terapia
Perché conta il quartiere del tumore
Il cancro non cresce in isolamento. Vive in un quartiere affollato di cellule di supporto, difensori immunitari e vasi sanguigni, tutti a condividere e contendere combustibile. Questo articolo esplora come i tumori riorganizzino l’uso di proteine e grassi — scomposti in aminoacidi e lipidi — non solo all’interno delle cellule tumorali, ma in tutto il loro contesto circostante. Capire questa economia nascosta di nutrienti aiuta a spiegare perché alcuni tumori sfuggono al sistema immunitario e resistono ai trattamenti, e indica verso terapie più intelligenti e precise.
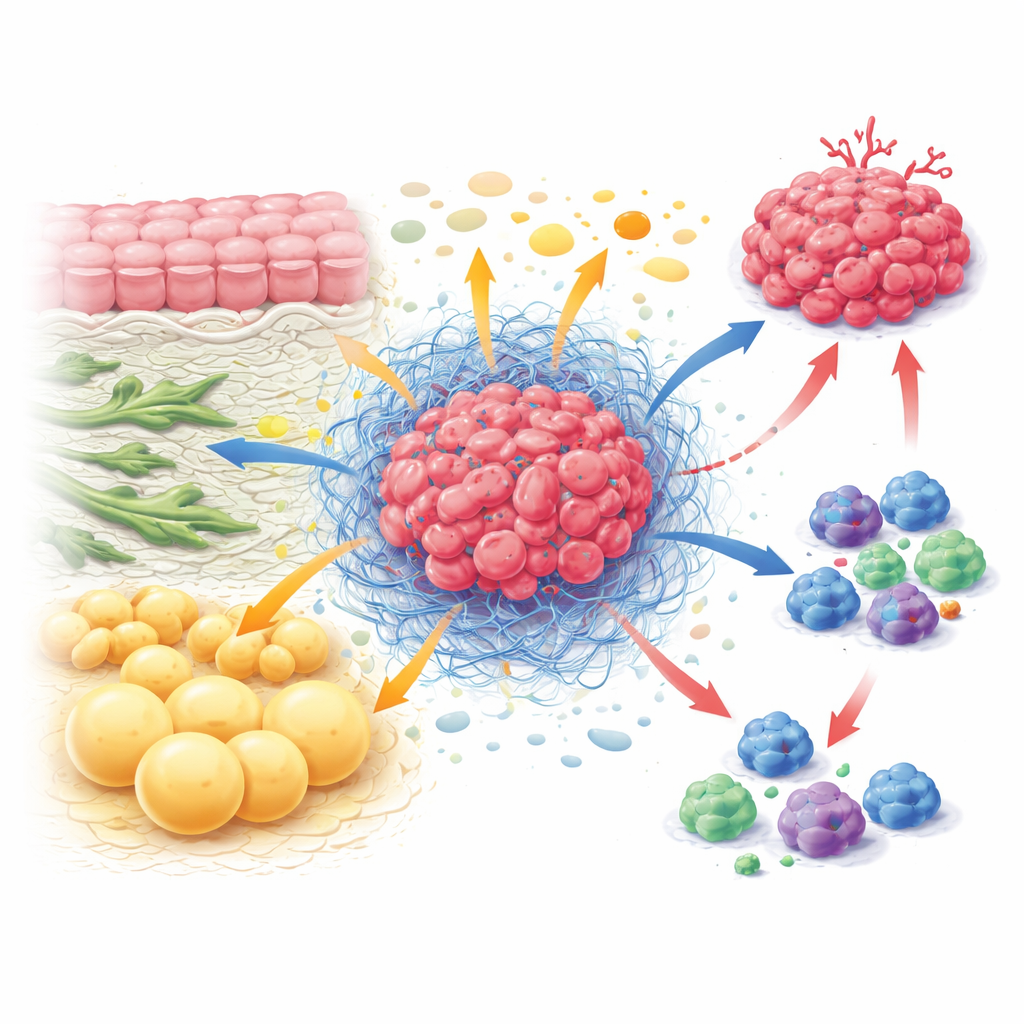
L’economia nascosta all’interno di un tumore
All’interno di un tumore, le cellule cancerose coesistono con fibroblasti che modellano la struttura del tessuto, cellule immunitarie che cercano di attaccare, cellule dei vasi sanguigni e adipociti. Insieme formano il microambiente tumorale, una sorta di ecosistema con regole proprie. Invece che ogni tipo cellulare agisca isolatamente, scambiano e competono costantemente per i nutrienti. I fibroblasti possono nutrire le cellule cancerose con blocchi costitutivi come alcuni aminoacidi, mentre al contempo irrigidiscono il tessuto circostante in modo che le cellule immunitarie non possano facilmente entrare. Le cellule immunitarie, quando sono attive, necessitano grandi quantità di combustibile per dividersi e uccidere, eppure spesso si trovano affamate perché le cellule tumorali e stromali ottengono accesso prioritario. Questa continua spinta e contrapposizione per i nutrienti favorisce la crescita tumorale indebolendo le difese dell’organismo.
Guerre per il combustibile: gli aminoacidi come armi
La recensione mette in evidenza diversi aminoacidi chiave che fungono sia da cibo sia da segnali. Glutammina, arginina, triptofano e aminoacidi ramificati sono cruciali sia per le cellule tumorali sia per le cellule immunitarie. I tumori spesso potenziano sistemi di trasporto ed enzimi che permettono loro di assorbire questi nutrienti, lasciando troppo poco per le cellule T citotossiche e le cellule natural killer. Allo stesso tempo, cellule di supporto come le cellule mieloidi e i fibroblasti possono degradare deliberatamente arginina e triptofano, generando prodotti di scarto che attenuano le risposte immunitarie e favoriscono le cellule T regolatorie che tollerano il tumore. In alcune nicchie, le cellule condividono anche aminoacidi per aiutare il cancro a sopravvivere ai trattamenti, o li riciclano dal tessuto danneggiato, creando sacche di resistenza alla chemioterapia e ai farmaci mirati.
Il grasso come combustibile, scudo e segnale
I lipidi — grassi, acidi grassi, colesterolo e molecole correlate — svolgono ruoli altrettanto importanti in questo ecosistema. Le cellule cancerose aumentano sia la produzione sia l’utilizzo dei grassi, impiegandoli per costruire membrane, immagazzinare energia e resistere allo stress. Gli adipociti e i fibroblasti vicini possono rilasciare acidi grassi che i tumori importano facilmente e accumulano in goccioline lipidiche, piccoli depositi di stoccaggio che proteggono dallo stress tossico e da molti farmaci. Anche le cellule immunitarie nel tumore sono spinte a fare un largo affidamento sul metabolismo lipidico. Le cellule T regolatorie e alcuni macrofagi usano gli acidi grassi per sopravvivere e mantenere la loro funzione soppressiva, mentre le cellule T citotossiche sovraccariche diventano esauste. Speciali messaggeri lipidici, come la lisofosfatidico acido, stimolano ulteriormente la crescita tumorale, guidano la diffusione del cancro verso organi distanti e respingono le cellule immunitarie dal nucleo del tumore.
Variare nello spazio, nel tempo e con la terapia
Il metabolismo in un tumore non è uniforme. I livelli di ossigeno e di nutrienti variano dal bordo esterno ben nutrito al nucleo affamato, e gli organi che ospitano metastasi offrono miscele di nutrienti distinte. Di conseguenza, alcune regioni privilegiano la demolizione degli zuccheri, altre contano maggiormente su glutammina o grassi, e questi schemi cambiano mentre il tumore cresce o affronta la terapia. Quando i trattamenti tagliano una fonte di combustibile, i tumori spesso passano a un’altra o fanno più affidamento sull’aiuto di fibroblasti e adipociti. Gli stessi cambiamenti metabolici possono inoltre alterare l’accensione o lo spegnimento dei geni tramite marcatori epigenetici, consolidando stati aggressivi o immunosoppressivi. Questa flessibilità rende difficile fermare il cancro bloccando una singola via.
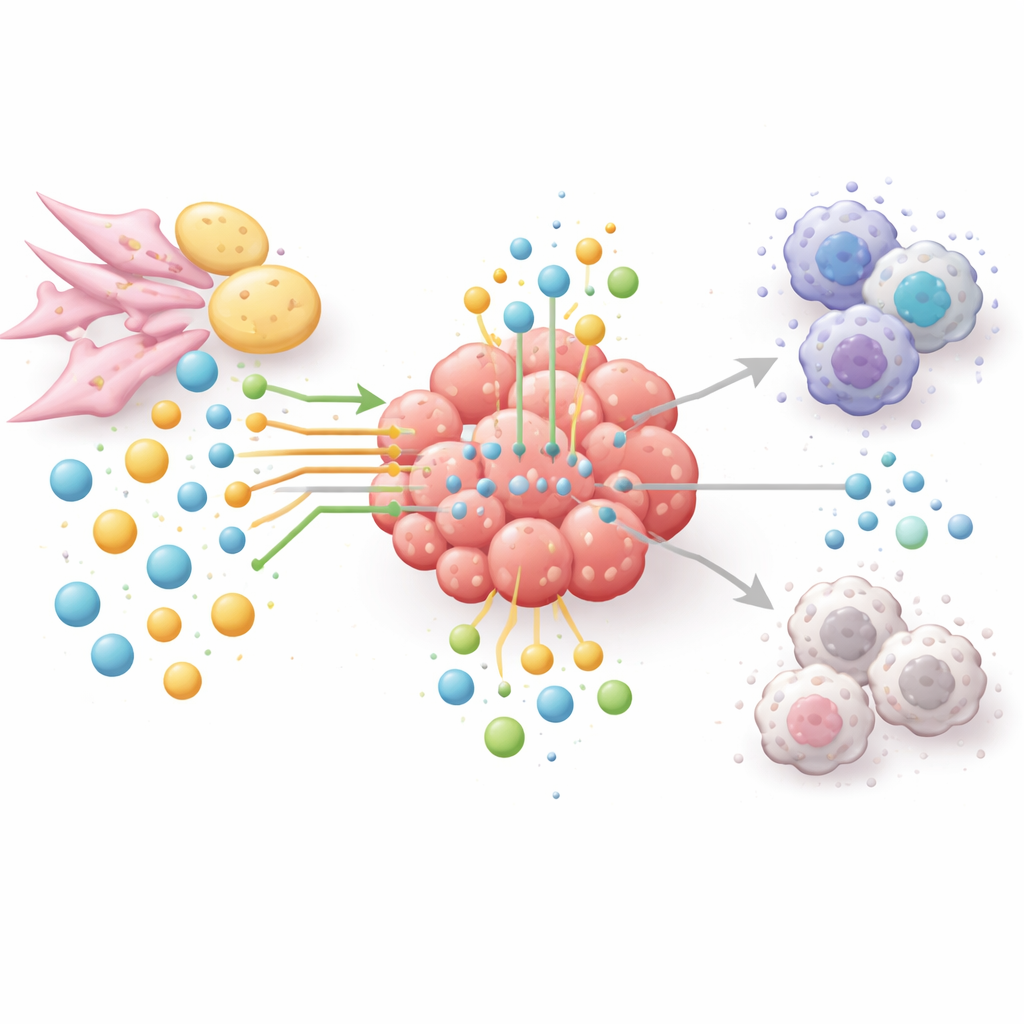
Nuovi modi per affamare il tumore, non il paziente
Poiché i percorsi degli aminoacidi e dei lipidi collegano crescita tumorale, fuga immunitaria e resistenza ai trattamenti, gli autori propongono un approccio basato sulle reti piuttosto che soluzioni “un farmaco per un enzima”. Le terapie sperimentali mirano ora a ridurre arginina o glutammina in tumori selezionati, bloccare enzimi della sintesi o della ossidazione dei grassi, o arrestare la degradazione del triptofano e i suoi prodotti immunosoppressivi. Molte di queste strategie vengono combinate con farmaci che agiscono sui checkpoint immunitari per indebolire il tumore e rivitalizzare le cellule T. Per scegliere le combinazioni e i pazienti giusti, il campo si sta rivolgendo alla metabolomica spaziale, alle biopsie liquide e all’intelligenza artificiale per mappare chi consuma cosa, dove e quando all’interno dei tumori. In termini semplici, l’articolo conclude che vincere contro il cancro richiederà non solo attaccare direttamente le cellule tumorali, ma anche riorganizzare l’intera rete di nutrienti che le protegge.
Citazione: Sung, Y., Kim, D.K., Kim, J.S. et al. Metabolic networks in the tumor microenvironment: roles of amino acid and lipid metabolism pathways in cancer progression and therapy. Exp Mol Med 58, 1128–1148 (2026). https://doi.org/10.1038/s12276-026-01697-0
Parole chiave: microambiente tumorale, metabolismo del cancro, aminoacidi, metabolismo dei lipidi, immunoterapia