Clear Sky Science · ar
الشبكات الأيضية في بيئة الورم الدقيقة: أدوار مسارات استقلاب الأحماض الأمينية والدهون في تقدم السرطان والعلاج
لماذا يهم حيّ الورم
السرطان لا ينمو في عزلة. إنه يعيش في حي مزدحم من خلايا داعمة، ومدافعين مناعيين وأوعية دموية، وكلها تتقاسم وتتقاتل على الوقود. يناقش هذا المقال كيف تعيد الأورام توصيل استخدام البروتينات والدهون — التي تتحلل إلى أحماض أمينية وليبيدات — ليس فقط داخل خلايا الورم، بل عبر محيطها بأكمله. يساعد فهم هذا الاقتصاد الخفي للمواد المغذية في تفسير سبب قدرة بعض الأورام على الهرب من الجهاز المناعي ومقاومة العلاج، ويشير إلى علاجات أكثر ذكاءً ودقة.
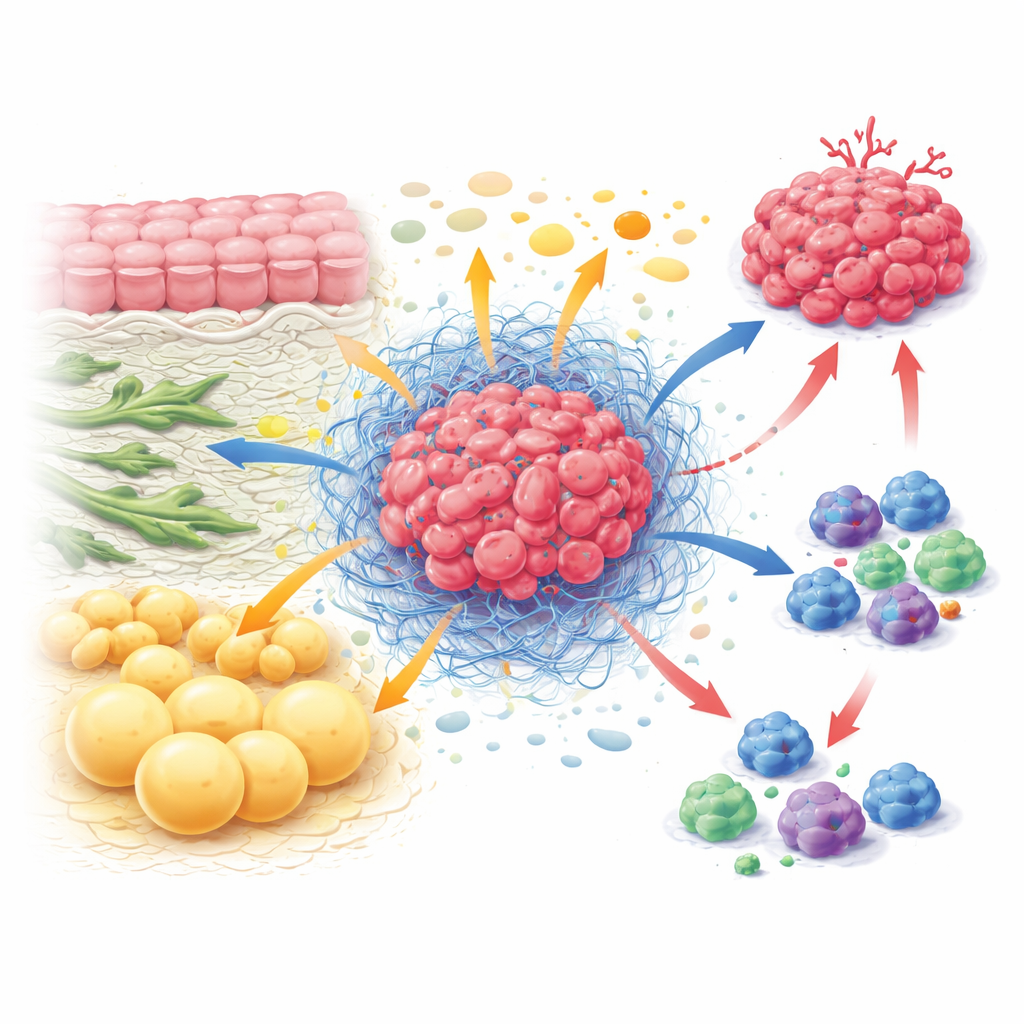
الاقتصاد الخفي داخل الورم
داخل الورم تتعايش خلايا السرطان مع الأرومات الليفية التي تشكل بنية النسيج، وخلايا مناعية تحاول الهجوم، وخلايا أوعية دموية وخلايا دهنية. معًا يشكلون بيئة الورم الدقيقة، نوعًا من النظام الإيكولوجي بقواعده الخاصة. بدلًا من عمل كل نوع خلية بمفرده، فهم يتبادلون ويتنافسون باستمرار على المغذيات. يمكن أن تزود الأرومات الليفية خلايا السرطان ببنات البناء مثل بعض الأحماض الأمينية، بينما تعمل أيضًا على تصلب النسيج المحيط بحيث لا تستطيع الخلايا المناعية الدخول بسهولة. تحتاج الخلايا المناعية، عندما تكون نشطة، إلى كميات كبيرة من الوقود للتكاثر والقتل، ومع ذلك غالبًا ما تجد نفسها محرومة لأن خلايا السرطان والخلايا الداعمة تحصل على أولوية الوصول. هذا التبادل المستمر على المغذيات يساعد الأورام على النمو بينما يضعف دفاعات الجسم.
حروب الوقود: الأحماض الأمينية كأسلحة
تسلط المراجعة الضوء على عدة أحماض أمينية رئيسية تعمل كطعام وإشارات في الوقت نفسه. الغلوتامين، والأرجينين، والتربتوفان والأحماض الأمينية متفرعة السلسلة ضرورية لكل من خلايا السرطان والخلايا المناعية. غالبًا ما تعزز الأورام أنظمة النقل والإنزيمات التي تُمكّنها من امتصاص هذه المغذيات، مما يترك القليل جدًا لخلايا T القاتلة والخلايا القاتلة الطبيعية. في الوقت نفسه، يمكن للخلايا الداعمة مثل الخلايا المكونة للنقي والأرومات الليفية أن تكسر عمدًا الأرجينين والتربتوفان، مولدة نواتج تحُدّ من الاستجابات المناعية وتشجع خلايا T المنظمة التي تتسامح مع الورم. في بعض المناطق المتخصصة، تتشارك الخلايا أيضًا الأحماض الأمينية لمساعدة السرطان على البقاء أمام العلاج، أو تعيد تدويرها من الأنسجة المتضررة، مكونة جيوبًا من المقاومة للعلاج الكيميائي والأدوية الموجَّهة.
الدهون كوقود، ودروع وإشارات
تلعب الليبيدات — الدهون والأحماض الدهنية والكوليسترول والجزيئات ذات الصلة — أدوارًا مهمة بالمثل في هذا النظام. تزيد خلايا السرطان كلًا من صناعة الدهون وحرقها، مستخدمة الدهون لبناء الأغشية وتخزين الطاقة ومقاومة الإجهاد. يمكن للخلايا الدهنية والأرومات الليفية المجاورة إطلاق أحماض دهنية تستوردها الأورام وتخزنها في قطرات دهنية، مستودعات صغيرة تحمي من الإجهاد السام والعديد من الأدوية. كذلك تدفع الظروف الخلوية الخلايا المناعية داخل الورم للاعتماد بشكل كبير على استقلاب الدهون. تستخدم خلايا T المنظمة وبعض البلعميات الأحماض الدهنية للبقاء وتبقى مثبطة، بينما تُجهد خلايا T القاتلة المشبعة. أيضاً تعمل رُسُل دهنية خاصة، مثل حمض الليزوفوسفاتيديك، على تحفيز نمو الورم، وتوجيه انتشار السرطان إلى أعضاء بعيدة، وطرد الخلايا المناعية من نواة الورم.
تغيير عبر المكان والزمان والعلاج
الاستقلاب داخل الورم ليس موحدًا. تتباين مستويات الأكسجين والمغذيات من الحافة الخارجية المشبعة إلى النواة الجائعة، وتوفر الأعضاء المختلفة التي تحتضن النقائل خلطات مغذية مميزة. نتيجة لذلك، تفضّل بعض المناطق حرق السكر، بينما تعتمد أخرى أكثر على الغلوتامين أو الدهون، وتتغير هذه الأنماط مع نمو الورم أو مواجهته للعلاج. عندما تقطع العلاجات مصدر وقود واحد، غالبًا ما تنتقل الأورام إلى مصدر آخر أو تعتمد أكثر على مساعدة الأرومات الليفية والخلايا الدهنية. يمكن لتلك التحولات الأيضية نفسها أن تغير أيضًا كيفية تشغيل أو إيقاف الجينات عبر علامات فوق جينية، مثبتة حالات عدوانية أو قابِلة لكبت المناعة. تجعل هذه المرونة من الصعب إيقاف السرطان عن طريق حظر مسار واحد فقط.
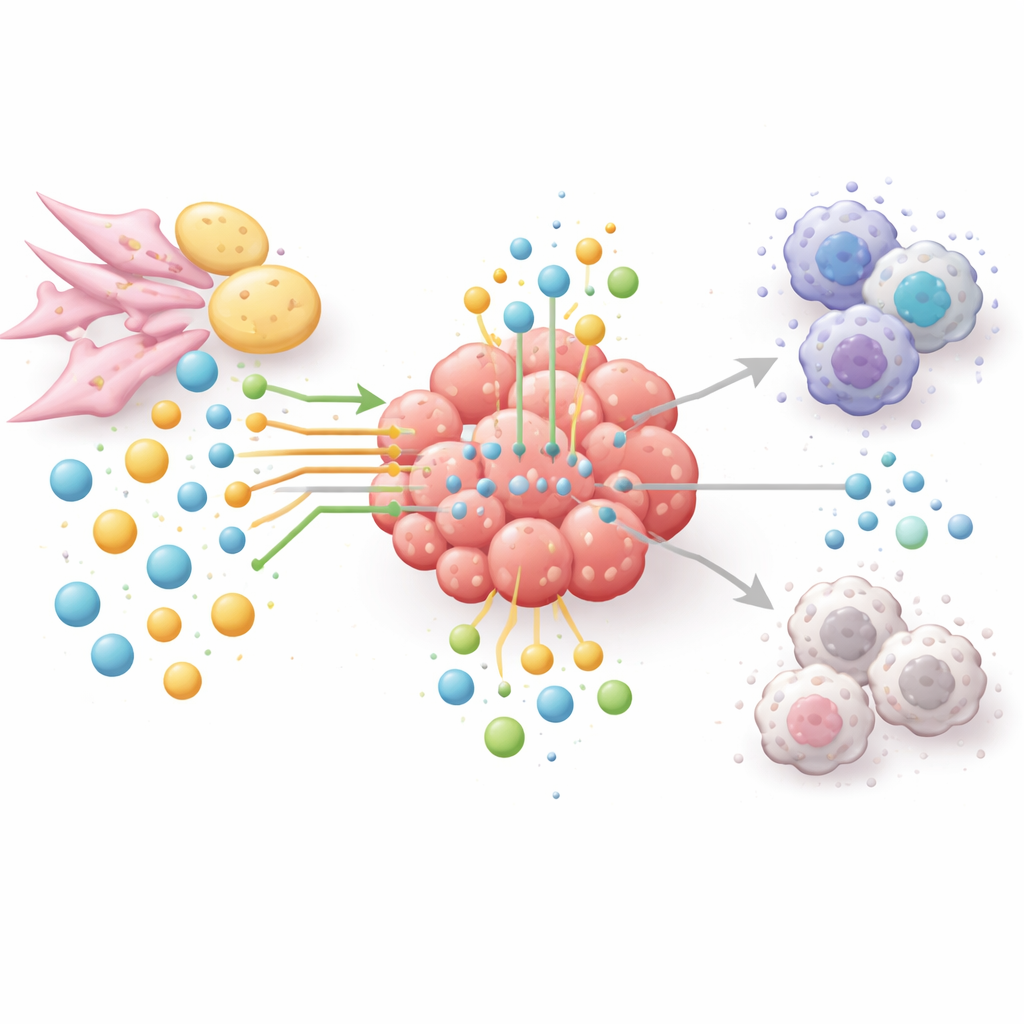
طرق جديدة لتجويع الورم دون تجويع المريض
نظرًا لأن مسارات الأحماض الأمينية والدهون تربط بين نمو الورم، وهروب المناعة ومقاومة العلاج، يجادل المؤلفون لصالح نهج شبكي بدلًا من حل دواءٍ واحدٍ لِإنزيمٍ واحد. تهدف العلاجات التجريبية الآن إلى خفض الأرجينين أو الغلوتامين في أورام مختارة بعناية، أو حجب إنزيمات صنع الدهون أو حرقها، أو إيقاف تكسير التربتوفان ومنتجاته المهيّجة للمناعة. يتم دمج العديد من هذه الاستراتيجيات مع أدوية نقاط التفتيش المناعية لإضعاف الورم وإعادة تنشيط خلايا T في الوقت نفسه. لاختيار التركيبات والمرضى المناسبين، يتجه المجال إلى الاستقلاب الفراغي، والخزعات السائلة والذكاء الاصطناعي لرسم خريطة من يأكل ماذا وأين ومتى داخل الأورام. بعبارة بسيطة، تستنتج المقالة أن الانتصار على السرطان سيتطلب ليس فقط مهاجمة خلايا الورم مباشرة، بل أيضًا إعادة توصيل شبكة المواد المغذية بأكملها التي تؤويها.
الاستشهاد: Sung, Y., Kim, D.K., Kim, J.S. et al. Metabolic networks in the tumor microenvironment: roles of amino acid and lipid metabolism pathways in cancer progression and therapy. Exp Mol Med 58, 1128–1148 (2026). https://doi.org/10.1038/s12276-026-01697-0
الكلمات المفتاحية: بيئة الورم الدقيقة, استقلاب السرطان, الأحماض الأمينية, استقلاب الدهون, العلاج المناعي