Clear Sky Science · de
Stoffwechsel-Netzwerke im Tumormikromilieu: Rollen von Aminosäure- und Lipidstoffwechselwegen bei Krebsprogression und Therapie
Warum die Nachbarschaft des Tumors wichtig ist
Krebs wächst nicht isoliert. Er lebt in einer belebten Nachbarschaft aus Stützzellen, Immunverteidigern und Blutgefäßen, die alle Treibstoff teilen und um ihn konkurrieren. Dieser Artikel untersucht, wie Krebszellen die Nutzung von Proteinen und Fetten – aufgeschlüsselt in Aminosäuren und Lipide – nicht nur innerhalb der Tumorzellen, sondern quer durch ihr gesamtes Umfeld umprogrammieren. Das Verständnis dieser verborgenen Nährstoffökonomie hilft zu erklären, warum manche Tumoren dem Immunsystem entkommen und Therapien widerstehen, und es weist den Weg zu intelligenteren, präziseren Behandlungsansätzen.
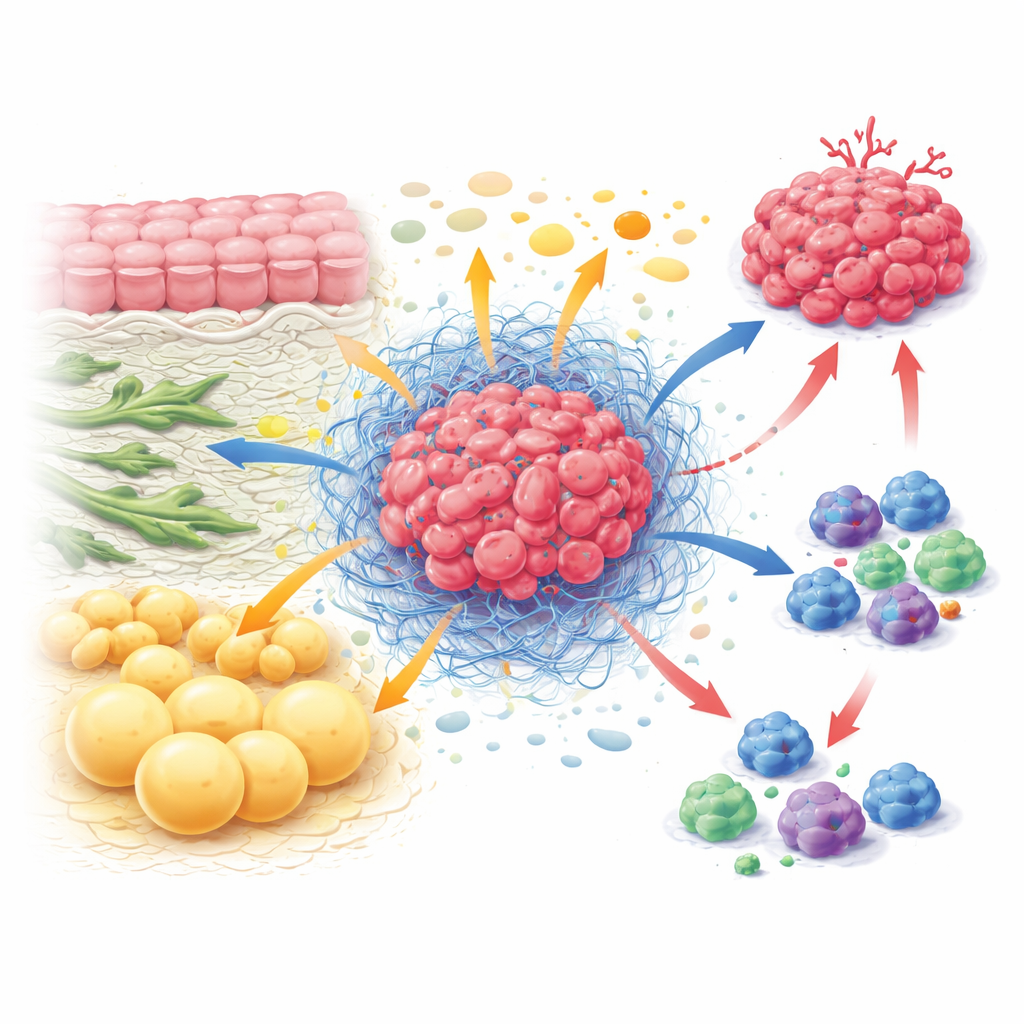
Die verborgene Ökonomie im Inneren eines Tumors
Innerhalb eines Tumors koexistieren Krebszellen mit Fibroblasten, die die Gewebsstruktur formen, mit Immunzellen, die Angriffe versuchen, mit Endothelzellen der Blutgefäße und mit Fettzellen. Gemeinsam bilden sie das Tumormikromilieu, eine Art Ökosystem mit eigenen Regeln. Anstatt dass jede Zellart allein arbeitet, tauschen sie konstant Nährstoffe aus und konkurrieren darum. Fibroblasten können Krebszellen mit Bausteinen wie bestimmten Aminosäuren versorgen und gleichzeitig das umgebende Gewebe versteifen, sodass Immunzellen schwer eindringen können. Aktive Immunzellen benötigen große Mengen an Treibstoff, um sich zu teilen und zu töten, finden sich jedoch häufig ausgehungert wieder, weil Krebs- und Stromazellen bevorzugt Zugang haben. Dieses ständige Ringen um Nährstoffe fördert das Tumorwachstum und schwächt zugleich die Abwehr des Körpers.
Treibstoffkriege: Aminosäuren als Waffen
Die Übersicht hebt mehrere Schlüsselaminosäuren hervor, die sowohl Nahrung als auch Signale sind. Glutamin, Arginin, Tryptophan und verzweigtkettige Aminosäuren sind für Krebs- und Immunzellen entscheidend. Tumoren verstärken häufig Transportsysteme und Enzyme, die ihnen erlauben, diese Nährstoffe aufzusaugen, sodass für Killer-T-Zellen und natürliche Killerzellen zu wenig übrig bleibt. Gleichzeitig können Stützzellen wie myeloide Zellen und Fibroblasten Arginin und Tryptophan gezielt abbauen und dabei Nebenprodukte erzeugen, die Immunantworten dämpfen und regulatorische T‑Zellen fördern, die den Tumor tolerieren. In manchen Nischen teilen Zellen auch Aminosäuren, um dem Krebs das Überleben unter Therapie zu erleichtern, oder recyceln sie aus geschädigtem Gewebe und schaffen so Resistenztaschen gegen Chemotherapie und zielgerichtete Medikamente.
Fett als Treibstoff, Schutz und Signal
Lipide – Fette, Fettsäuren, Cholesterin und verwandte Moleküle – spielen in diesem Ökosystem ebenso wichtige Rollen. Krebszellen steigern sowohl die Fettproduktion als auch den Fettabbau und nutzen Lipide zum Aufbau von Membranen, zur Energiespeicherung und zur Stressresistenz. Nahegelegene Fettzellen und Fibroblasten können Fettsäuren freisetzen, die Tumoren bereitwillig importieren und in Lipidtröpfchen einlagern, winzige Speicherdepots, die vor toxischem Stress und vielen Medikamenten schützen. Auch Immunzellen im Tumor werden zu einer starken Abhängigkeit vom Fettstoffwechsel gedrängt. Regulatorische T‑Zellen und bestimmte Makrophagen nutzen Fettsäuren, um zu überleben und unterdrückend zu bleiben, während überlastete Killer‑T‑Zellen erschöpfen. Besondere lipidbasierte Botenstoffe, wie Lysophosphatidinsäure, fördern weiter das Tumorwachstum, lenken die Ausbreitung von Krebs in entfernte Organe und weisen Immunzellen vom Tumorkern ab.
Veränderung über Raum, Zeit und Behandlung
Der Stoffwechsel in einem Tumor ist nicht einheitlich. Sauerstoff- und Nährstoffniveaus variieren vom gut versorgten äußeren Rand bis zum ausgehungerten Kern, und verschiedene Organe, die Metastasen beherbergen, bieten unterschiedliche Nährstoffmixe. Infolgedessen begünstigen manche Regionen die Zuckerverbrennung, andere verlassen sich stärker auf Glutamin oder Fette, und diese Muster verschieben sich, wenn der Tumor wächst oder einer Therapie ausgesetzt wird. Wenn Behandlungen eine Energiequelle abschneiden, schalten Tumoren oft auf eine andere um oder verlassen sich stärker auf Hilfe von Fibroblasten und Fettzellen. Dieselben metabolischen Verschiebungen können auch die Genregulation über epigenetische Markierungen verändern und aggressive oder immunsuppressive Zustände festigen. Diese Flexibilität erschwert es, Krebs allein durch Blockade eines einzelnen Wegs zu stoppen.
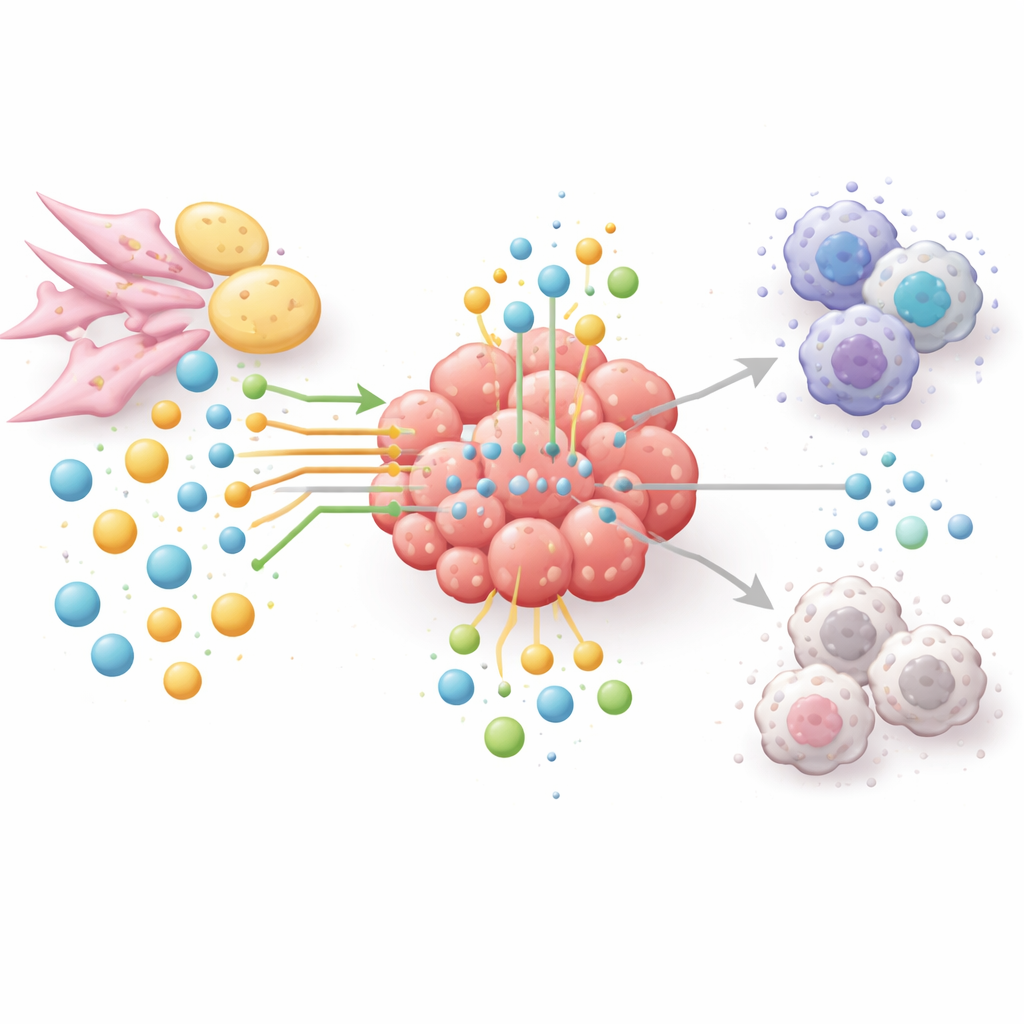
Neue Wege, den Tumor auszuhungern, ohne den Patienten zu schwächen
Da Aminosäure- und Lipidwege Tumorwachstum, Immunflucht und Therapieresistenz verbinden, plädieren die Autoren für einen netzwerkbasierten Ansatz statt Ein‑Medikament‑für‑Ein‑Enzym‑Lösungen. Experimentelle Therapien zielen inzwischen darauf ab, Arginin oder Glutamin in sorgfältig ausgewählten Tumoren zu senken, Enzyme der Fettbiosynthese oder des Fettabbaus zu blockieren oder den Tryptophanabbau und seine immundämpfenden Produkte zu stoppen. Viele dieser Strategien werden mit Immun-Checkpoint‑Medikamenten kombiniert, um den Tumor zu schwächen und gleichzeitig T‑Zellen wieder zu reaktivieren. Um die richtigen Kombinationen und Patienten auszuwählen, wendet sich das Feld räumlicher Metabolomik, Flüssigbiopsien und künstlicher Intelligenz zu, um zu kartieren, wer was, wo und wann in Tumoren konsumiert. Einfach ausgedrückt kommt der Artikel zu dem Schluss, dass der Sieg gegen Krebs nicht nur direkten Angriff auf Tumorzellen erfordert, sondern auch das Umpolen des gesamten Nährstoffnetzwerks, das sie schützt.
Zitation: Sung, Y., Kim, D.K., Kim, J.S. et al. Metabolic networks in the tumor microenvironment: roles of amino acid and lipid metabolism pathways in cancer progression and therapy. Exp Mol Med 58, 1128–1148 (2026). https://doi.org/10.1038/s12276-026-01697-0
Schlüsselwörter: Tumormikromilieu, Krebsstoffwechsel, Aminosäuren, Lipidstoffwechsel, Immuntherapie