Clear Sky Science · pl
Sieci metaboliczne w mikrośrodowisku guza: rola szlaków metabolizmu aminokwasów i lipidów w progresji nowotworu i terapii
Dlaczego sąsiedztwo guza ma znaczenie
Nowotwór nie rozwija się w izolacji. Istnieje w zatłoczonym otoczeniu komórek wsparcia, komórek układu odpornościowego i naczyń krwionośnych — wszystkie dzielą i rywalizują o paliwo. Artykuł ten bada, jak nowotwory przeprogramowują wykorzystanie białek i tłuszczów — rozkładanych na aminokwasy i lipidy — nie tylko wewnątrz komórek nowotworowych, lecz także w całym ich otoczeniu. Zrozumienie tej ukrytej gospodarki składników odżywczych pomaga wyjaśnić, dlaczego niektóre guzy wymykają się układowi odpornościowemu i opierają się leczeniu, oraz wskazuje drogę do mądrzejszych, bardziej precyzyjnych terapii.
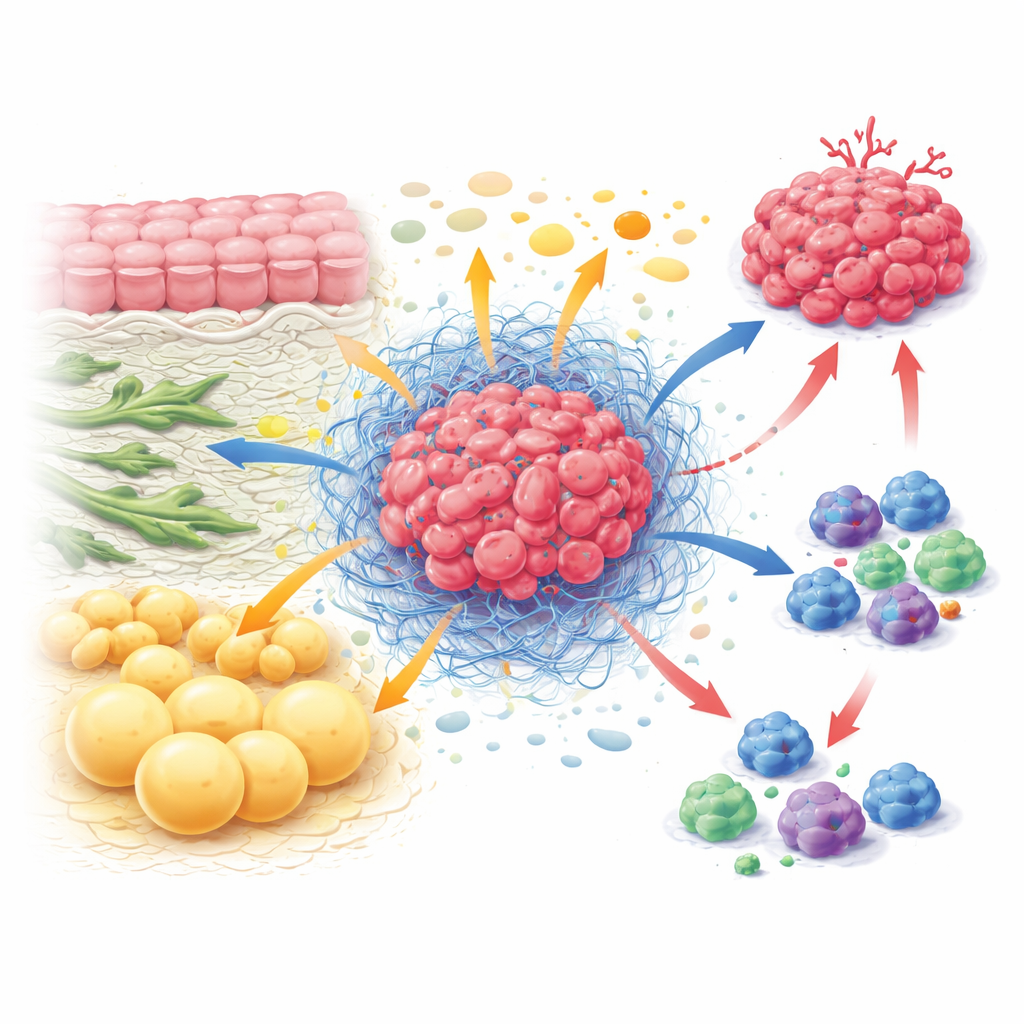
Ukryta gospodarka wewnątrz guza
W obrębie guza komórki nowotworowe współistnieją z fibroblastami kształtującymi strukturę tkanki, komórkami odpornościowymi próbującymi atakować, komórkami naczyń krwionośnych i adipocytami. Razem tworzą mikrośrodowisko guza — rodzaj ekosystemu z własnymi zasadami. Zamiast działać niezależnie, typy komórek nieustannie wymieniają się i rywalizują o składniki odżywcze. Fibroblasty mogą zasilać komórki nowotworowe blokami budulcowymi, takimi jak niektóre aminokwasy, jednocześnie usztywniając otaczającą tkankę, by komórki odpornościowe miały utrudniony dostęp. Komórki odpornościowe, gdy są aktywne, potrzebują dużych ilości paliwa do dzielenia się i zabijania komórek nowotworowych, jednak często głodują, bo nowotwór i komórki zrębu uzyskują priorytetowy dostęp. Ten ciągły popych i ciągnięć o składniki odżywcze sprzyja wzrostowi guza przy osłabianiu obrony organizmu.
Wojny o paliwo: aminokwasy jako broń
Przegląd wyróżnia kilka kluczowych aminokwasów pełniących rolę zarówno pożywienia, jak i sygnałów. Glutamina, arginina, tryptofan oraz aminokwasy rozgałęzione są niezbędne dla komórek nowotworowych i odpornościowych. Guzy często zwiększają systemy transportu i enzymy umożliwiające im wychwytywanie tych składników, pozostawiając zbyt mało dla komórek T zabójczych i komórek NK. Równocześnie komórki wsparcia, takie jak komórki mieloidalne i fibroblasty, mogą celowo rozkładać argininę i tryptofan, wytwarzając produkty uboczne, które tonują odpowiedź immunologiczną i sprzyjają komórkom T regulatorowym tolerującym guz. W niektórych niszach komórki dzielą się też aminokwasami, aby pomóc nowotworowi przetrwać leczenie, lub odzyskują je z uszkodzonej tkanki, tworząc enklawy odporne na chemioterapię i leki ukierunkowane.
Tłuszcz jako paliwo, tarcza i sygnał
Lipidy — tłuszcze, kwasy tłuszczowe, cholesterol i pokrewne cząsteczki — odgrywają równie istotne role w tym ekosystemie. Komórki nowotworowe zwiększają zarówno syntezę tłuszczów, jak i ich utlenianie, wykorzystując je do budowy błon, magazynowania energii i opierania się stresowi. Sąsiednie komórki tłuszczowe i fibroblasty mogą uwalniać kwasy tłuszczowe, które guzy chętnie importują i magazynują w kropelkach lipidowych — małych magazynach chroniących przed toksycznym stresem i wieloma lekami. Komórki odpornościowe w guzie też są kierowane ku dużemu poleganiu na metabolizmie tłuszczów. Komórki T regulatorowe i niektóre makrofagi używają kwasów tłuszczowych, by przetrwać i zachować supresyjny charakter, podczas gdy przeciążone komórki T zabójcze ulegają wyczerpaniu. Specjalne lipidowe przekaźniki, takie jak lizofosfatydowy kwas, dodatkowo stymulują wzrost guza, kierują przerzutami do odległych narządów i odpychają komórki odpornościowe od jądra guza.
Zmiany w przestrzeni, czasie i pod wpływem leczenia
Metabolizm w guzie nie jest jednolity. Poziomy tlenu i składników odżywczych wahają się od dobrze zaopatrzonej zewnętrznej krawędzi po głodowe jądro, a różne narządy goszczące przerzuty oferują odmienne mieszanki składników odżywczych. W rezultacie niektóre regiony preferują spalanie cukrów, inne polegają bardziej na glutaminie lub tłuszczach, a wzorce te zmieniają się wraz z rozrostem guza lub zastosowaniem terapii. Gdy leczenie odcina jedno paliwo, guzy często przełączają się na inne lub zwiększają zależność od pomocy fibroblastów i komórek tłuszczowych. Te same przesunięcia metaboliczne mogą również zmieniać aktywność genów przez modyfikacje epigenetyczne, utrwalając stany agresywne lub immunosupresyjne. Ta elastyczność utrudnia powstrzymanie nowotworu przez zablokowanie jednego szlaku.
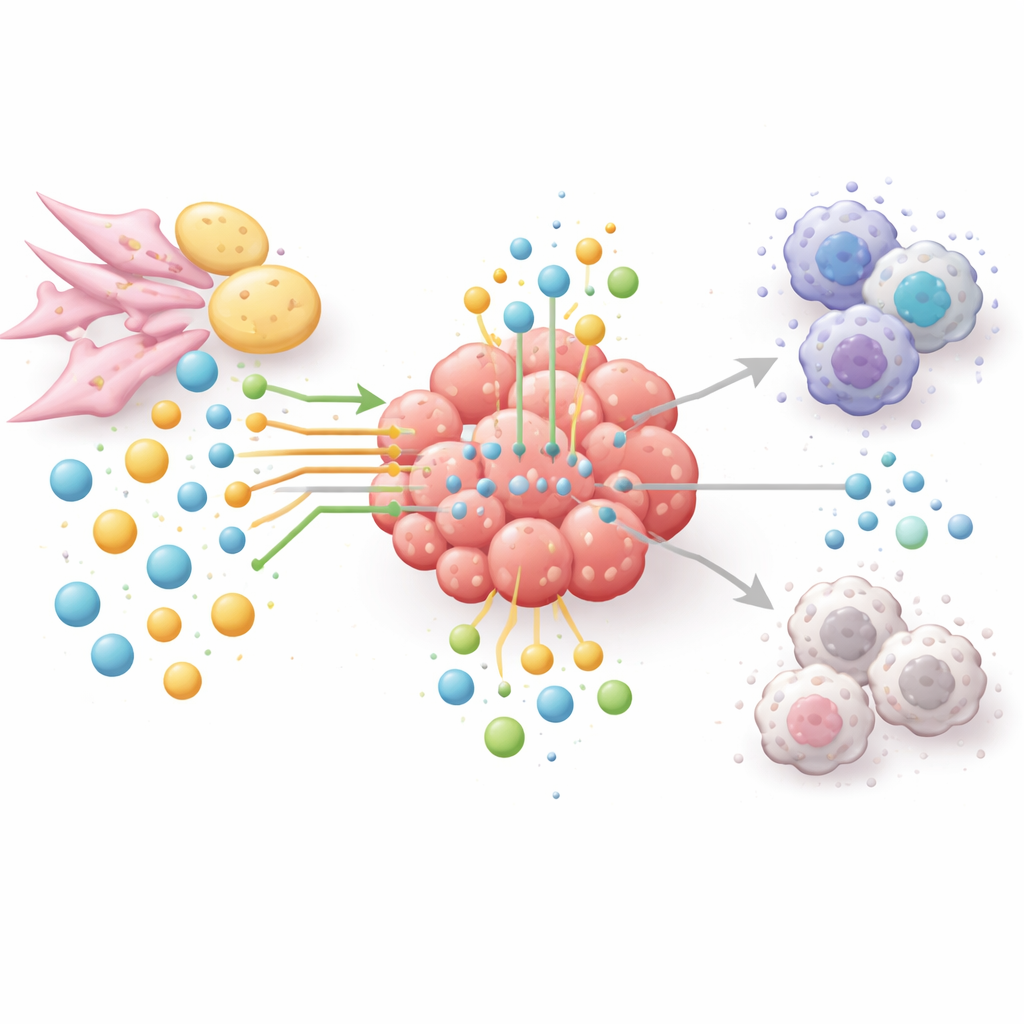
Nowe sposoby głodzenia guza, nie pacjenta
Ponieważ szlaki aminokwasowe i lipidowe łączą wzrost guza, ucieczkę przed układem odpornościowym i oporność na leczenie, autorzy opowiadają się za podejściem opartym na sieciach, a nie lekiem na jeden enzym. Terapie eksperymentalne dążą obecnie do obniżenia poziomu argininy lub glutaminy w starannie wybranych guzach, blokowania enzymów syntezujących lub utleniających tłuszcze, albo zatrzymania rozkładu tryptofanu i powstających w ten sposób immunosupresyjnych produktów. Wiele z tych strategii łączy się z lekami przeciwko punktom kontrolnym układu odpornościowego, by jednocześnie osłabić guz i reaktywować limfocyty T. Aby dobrać właściwe kombinacje i pacjentów, dziedzina ta sięga po metabolomikę przestrzenną, biopsje płynne i sztuczną inteligencję, by mapować, kto co, gdzie i kiedy konsumuje wewnątrz guzów. Mówiąc prościej, artykuł konkluduje, że zwycięstwo z rakiem będzie wymagać nie tylko ataku na komórki nowotworowe bezpośrednio, lecz także przeprogramowania całej sieci składników odżywczych, która je chroni.
Cytowanie: Sung, Y., Kim, D.K., Kim, J.S. et al. Metabolic networks in the tumor microenvironment: roles of amino acid and lipid metabolism pathways in cancer progression and therapy. Exp Mol Med 58, 1128–1148 (2026). https://doi.org/10.1038/s12276-026-01697-0
Słowa kluczowe: mikrośrodowisko guza, metabolizm nowotworu, aminokwasy, metabolizm lipidów, immunoterapia