Clear Sky Science · ru
Метаболические сети в микроокружении опухоли: роли путей обмена аминокислот и липидов в прогрессировании рака и терапии
Почему окружение опухоли имеет значение
Рак не растёт в изоляции. Он существует в оживлённом соседстве клеток поддержки, иммунных защитников и кровеносных сосудов, которые вместе делят и оспаривают доступ к «топливу». В этой статье рассматривается, как опухоли перенастраивают использование белков и жиров — распадающихся на аминокислоты и липиды — не только внутри раковых клеток, но и по всему их окружению. Понимание этой скрытой экономики питательных веществ помогает объяснить, почему некоторые опухоли ускользают от иммунной системы и сопротивляются лечению, и указывает путь к более умным, точечным терапиям.
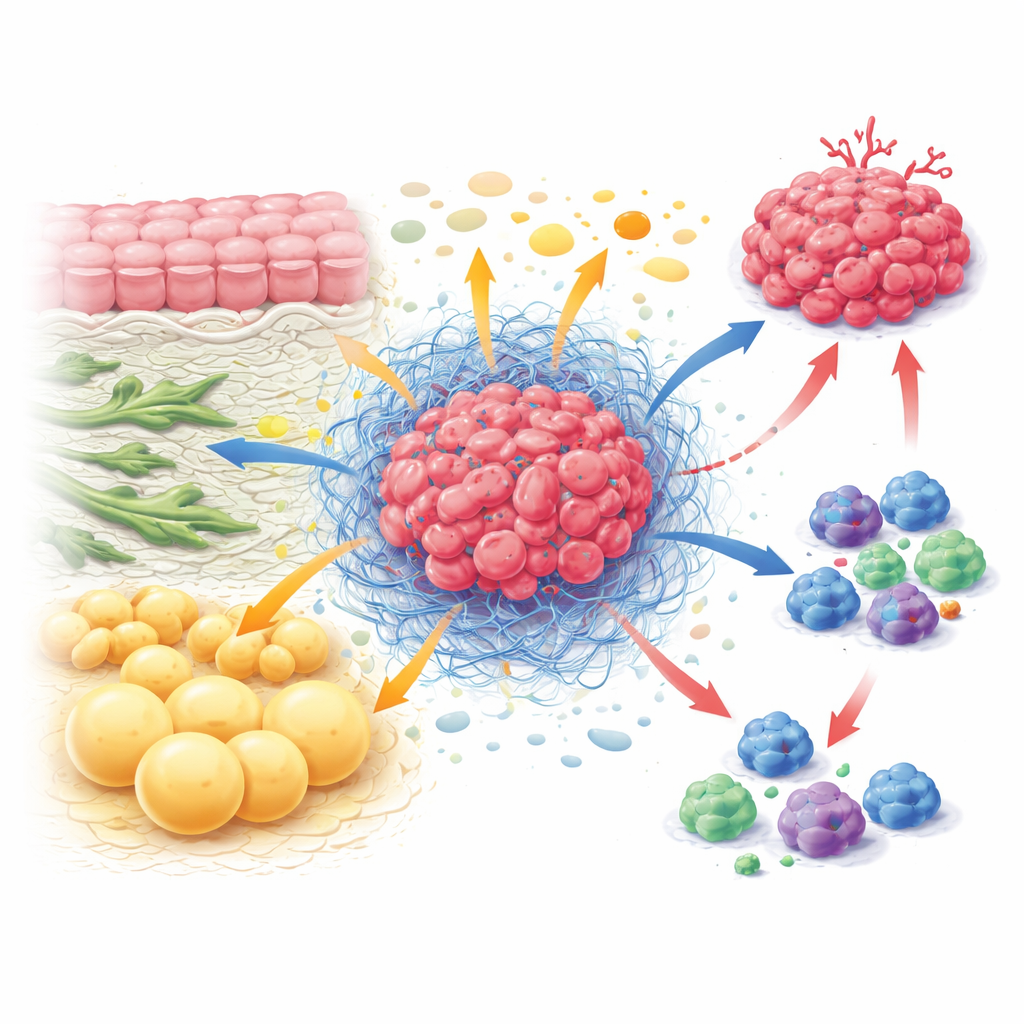
Скрытая экономика внутри опухоли
Внутри опухоли раковые клетки сосуществуют с фибробластами, формирующими структуру ткани, иммунными клетками, пытающимися атаковать, эндотелиальными клетками сосудов и адипоцитами. Вместе они образуют микроокружение опухоли — нечто вроде экосистемы со своими правилами. Вместо того чтобы каждый тип клеток действовал изолированно, они постоянно обмениваются и конкурируют за питательные вещества. Фибробласты могут подпитывать раковые клетки строительными блоками, такими как определённые аминокислоты, одновременно уплотняя окружающую ткань, чтобы иммунные клетки не могли легко проникнуть внутрь. Активные иммунные клетки нуждаются в больших объёмах энергии для деления и убийства, но часто оказываются обделёнными, поскольку раковые и стромальные клетки получают приоритетный доступ. Эта постоянная борьба за питательные вещества помогает опухолям расти и ослабляет защитные силы организма.
Войны за топливо: аминокислоты как оружие
Обзор выделяет несколько ключевых аминокислот, которые выступают одновременно и как пища, и как сигналы. Глутамин, аргинин, триптофан и разветвлённые аминокислоты критичны как для раковых, так и для иммунных клеток. Опухоли часто усиливают системы транспорта и ферменты, позволяющие им поглощать эти вещества, оставляя слишком мало для киллерных Т‑клеток и натуральных киллеров. В то же время клетки поддержки, такие как миелоидные клетки и фибробласты, могут целенаправленно разрушать аргинин и триптофан, образуя побочные продукты, которые подавляют иммунный ответ и стимулируют регуляторные Т‑клетки, терпимые к опухоли. В отдельных нишах клетки также обмениваются аминокислотами, чтобы помочь раку пережить лечение, или перерабатывают их из повреждённой ткани, создавая очаги устойчивости к химиотерапии и таргетным препаратам.
Жиры как топливо, щит и сигнал
Липиды — жиры, жирные кислоты, холестерин и родственные молекулы — играют не менее важную роль в этой экосистеме. Раковые клетки усиливают как синтез липидов, так и их окисление, используя жиры для строительства мембран, хранения энергии и сопротивления стрессу. Ближайшие адипоциты и фибробласты могут выделять жирные кислоты, которые опухоли легко импортируют и откладывают в липидных каплях — малых депо, защищающих от токсического стресса и многих лекарств. Иммунные клетки в опухоли также смещаются в сторону сильной зависимости от липидного обмена. Регуляторные Т‑клетки и определённые макрофаги используют жирные кислоты для выживания и сохранения супрессивного фенотипа, тогда как перегруженные киллерные Т‑клетки истощаются. Особые липидные медиаторы, такие как лизофосфатидная кислота, дополнительно стимулируют рост опухоли, направляют её метастазирование в отдалённые органы и отталкивают иммунные клетки от ядра опухоли.
Изменения по пространству, времени и лечению
Метаболизм в опухоли неоднороден. Уровни кислорода и питательных веществ варьируют от хорошо снабжаемого внешнего края до истощённого ядра, а различные органы, принимающие метастазы, предлагают разные смеси нутриентов. В результате одни области предпочитают сжигание сахаров, другие больше полагаются на глутамин или жиры, и эти схемы изменяются по мере роста опухоли или под давлением терапии. Когда лечение перекрывает один вид топлива, опухоли часто переключаются на другой или сильнее зависят от помощи фибробластов и адипоцитов. Те же метаболические сдвиги могут также менять включение или выключение генов через эпигенетические метки, закрепляя агрессивные или иммуноподавляющие состояния. Эта гибкость затрудняет подавление рака при блокировании единственного пути.
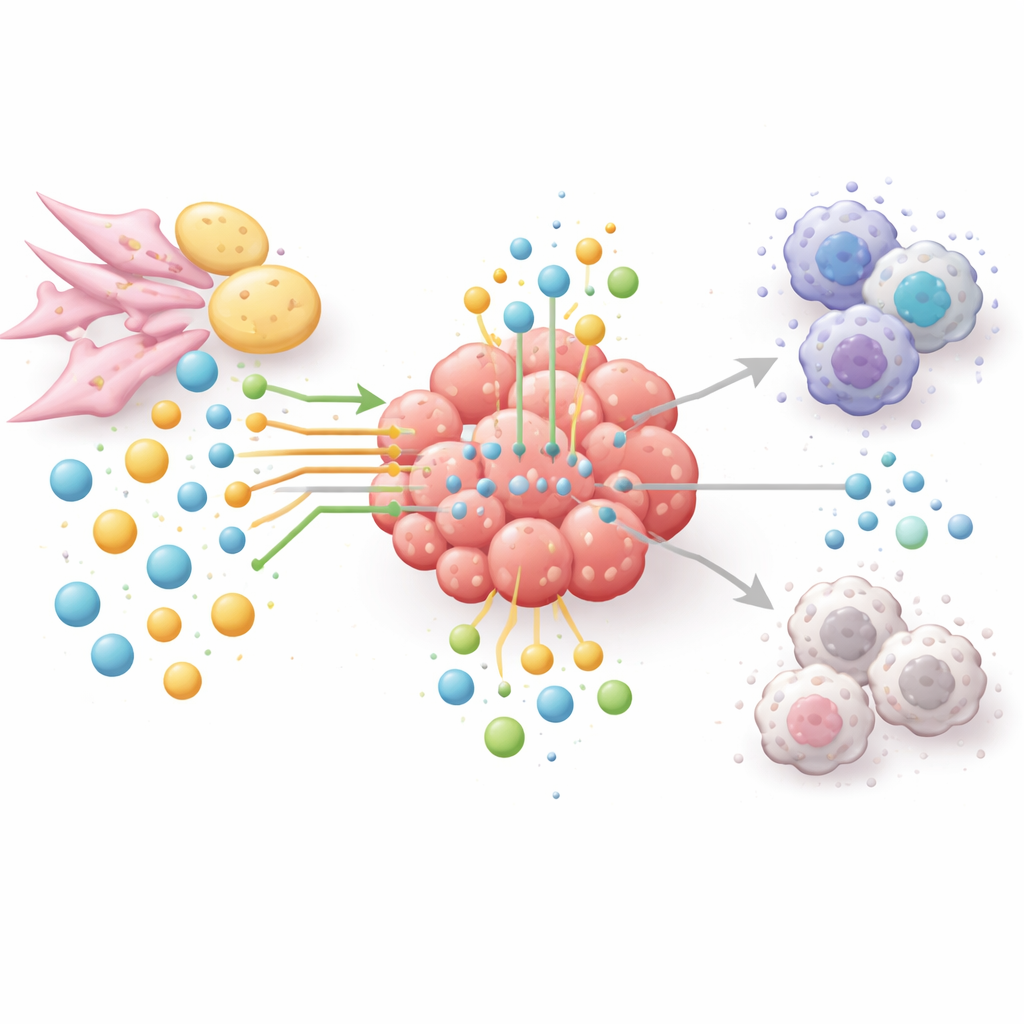
Новые способы истощать опухоль, а не пациента
Поскольку пути аминокислотного и липидного обмена связывают рост опухоли, уход от иммунитета и устойчивость к лечению, авторы выступают за сетевой подход, а не за стратегию «один препарат — один фермент». Экспериментальные терапии сейчас направлены на снижение уровней аргинина или глутамина в тщательно отобранных опухолях, блокирование ферментов синтеза или окисления липидов, либо подавление распада триптофана и его иммуносупрессивных продуктов. Многие из этих стратегий комбинируют с препаратами, блокирующими иммунные контрольные точки, чтобы одновременно ослабить опухоль и восстановить энергию Т‑клеткам. Чтобы подобрать правильные комбинации и пациентов, область обращается к пространственной метаболомике, жидкостным биопсиям и искусственному интеллекту для картирования того, кто что ест, где и когда внутри опухоли. Проще говоря, статья делает вывод: для победы над раком потребуется не только прямая атака на раковые клетки, но и перенастройка всей сети питательных веществ, которая их укрывает.
Цитирование: Sung, Y., Kim, D.K., Kim, J.S. et al. Metabolic networks in the tumor microenvironment: roles of amino acid and lipid metabolism pathways in cancer progression and therapy. Exp Mol Med 58, 1128–1148 (2026). https://doi.org/10.1038/s12276-026-01697-0
Ключевые слова: опухолевое микроокружение, метаболизм рака, аминокислоты, липидный обмен, иммунотерапия