Clear Sky Science · nl
Metabole netwerken in de tumor-micro-omgeving: rollen van aminozuur- en lipidenmetabolisme in kankerprogressie en therapie
Waarom de buurt van de tumor ertoe doet
Kanker groeit niet geïsoleerd. Het leeft in een drukke omgeving van ondersteunende cellen, immuunverdedigers en bloedvaten, die allemaal brandstof delen en ervoor concurreren. Dit artikel onderzoekt hoe tumoren het gebruik van eiwitten en vetten — afgebroken tot respectievelijk aminozuren en lipiden — herschakelen, niet alleen binnen tumorcellen maar door het hele omliggende weefsel. Inzicht in deze verborgen voedings-economie verklaart waarom sommige tumoren het immuunsysteem ontlopen en therapieresistent worden, en wijst op slimmere, meer precieze behandelstrategieën.
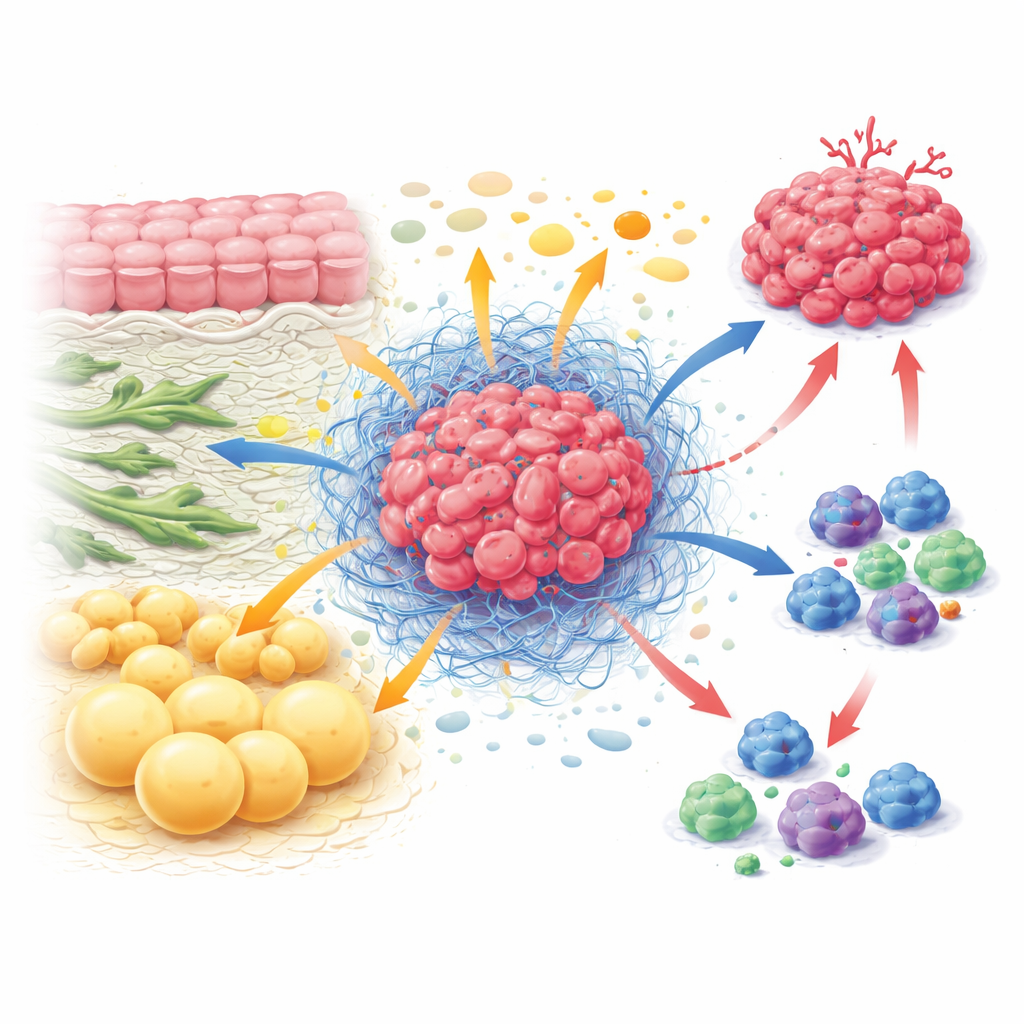
De verborgen economie binnen een tumor
Binnen een tumor bestaan kankercellen naast fibroblasten die de weefselstructuur vormen, immuuncellen die proberen aan te vallen, bloedvatcellen en vetcellen. Samen vormen ze de tumor-micro-omgeving, een soort ecosysteem met eigen regels. In plaats van dat elk celtype op zichzelf werkt, ruilen en concurreren ze voortdurend om nutriënten. Fibroblasten kunnen kankercellen voeden met bouwstoffen zoals bepaalde aminozuren, en tegelijkertijd het omliggende weefsel verstrakken zodat immuuncellen minder gemakkelijk binnenkomen. Actieve immuuncellen hebben veel brandstof nodig om te delen en te doden, maar ze worden vaak uitgehongerd omdat kankercellen en stromale cellen prioriteit geven aan toegang. Deze voortdurende strijd om nutriënten helpt tumoren groeien terwijl de verdediging van het lichaam verzwakt.
Brandstofoorlogen: aminozuren als wapens
De review belicht verschillende belangrijke aminozuren die zowel voedsel als signalen zijn. Glutamine, arginine, tryptofaan en vertakte-keten aminozuren zijn cruciaal voor zowel kankercellen als immuuncellen. Tumoren versterken vaak transporters en enzymen waarmee ze deze nutriënten opslorpen, waardoor er te weinig overblijft voor killer T-cellen en natural killer-cellen. Tegelijkertijd kunnen ondersteunende cellen zoals myeloïde cellen en fibroblasten arginine en tryptofaan afbreken, waardoor bijproducten ontstaan die immuunreacties dempen en regulatorische T-cellen bevorderen die de tumor tolereren. In sommige niches delen cellen ook aminozuren om kanker te helpen therapie te overleven, of recyclen ze deze uit beschadigd weefsel, waardoor pockets van resistentie tegen chemotherapie en gerichte middelen ontstaan.
Vet als brandstof, schild en signaal
Lipiden — vetten, vetzuren, cholesterol en verwante moleculen — vervullen even belangrijke rollen in dit ecosysteem. Kankercellen verhogen zowel vetproductie als vetverbranding, gebruiken vetten om membranen te bouwen, energie op te slaan en stress te weerstaan. Nabije vetcellen en fibroblasten kunnen vetzuren vrijgeven die tumoren snel importeren en opslaan in lipidedruppels, kleine opslagdepots die beschermen tegen toxische stress en veel geneesmiddelen. Immuuncellen in de tumor worden eveneens naar een sterke afhankelijkheid van vetmetabolisme geduwd. Regulatorische T-cellen en bepaalde macrofagen gebruiken vetzuren om te overleven en onderdrukkend te blijven, terwijl overbelaste killer T-cellen uitgeput raken. Speciale lipideboodschappers, zoals lysofosfatidazuur, stimuleren bovendien tumorgroei, begeleiden uitzaaiing naar verre organen en houden immuuncellen uit de tumorkern weg.
Verandering over ruimte, tijd en behandeling
Metabolisme in een tumor is niet uniform. Zuurstof- en nutriëntenniveaus variëren van de goed gevoede buitenrand tot de uitgehongerde kern, en verschillende organen die metastasen huisvesten bieden verschillende nutriëntmixen. Daardoor geven sommige regio’s de voorkeur aan suikerverbranding, anderen vertrouwen meer op glutamine of vetten, en deze patronen verschuiven naarmate de tumor groeit of therapie ondergaat. Wanneer behandelingen één brandstof afsluiten, schakelen tumoren vaak over op een andere of vertrouwen meer op hulp van fibroblasten en vetcellen. Dezelfde metabole verschuivingen kunnen ook veranderen hoe genen aan- of uitgezet worden via epigenetische markeringen, waardoor agressieve of immuunonderdrukkende toestanden verankerd raken. Deze flexibiliteit maakt het lastig kanker te stoppen door slechts één pad te blokkeren.
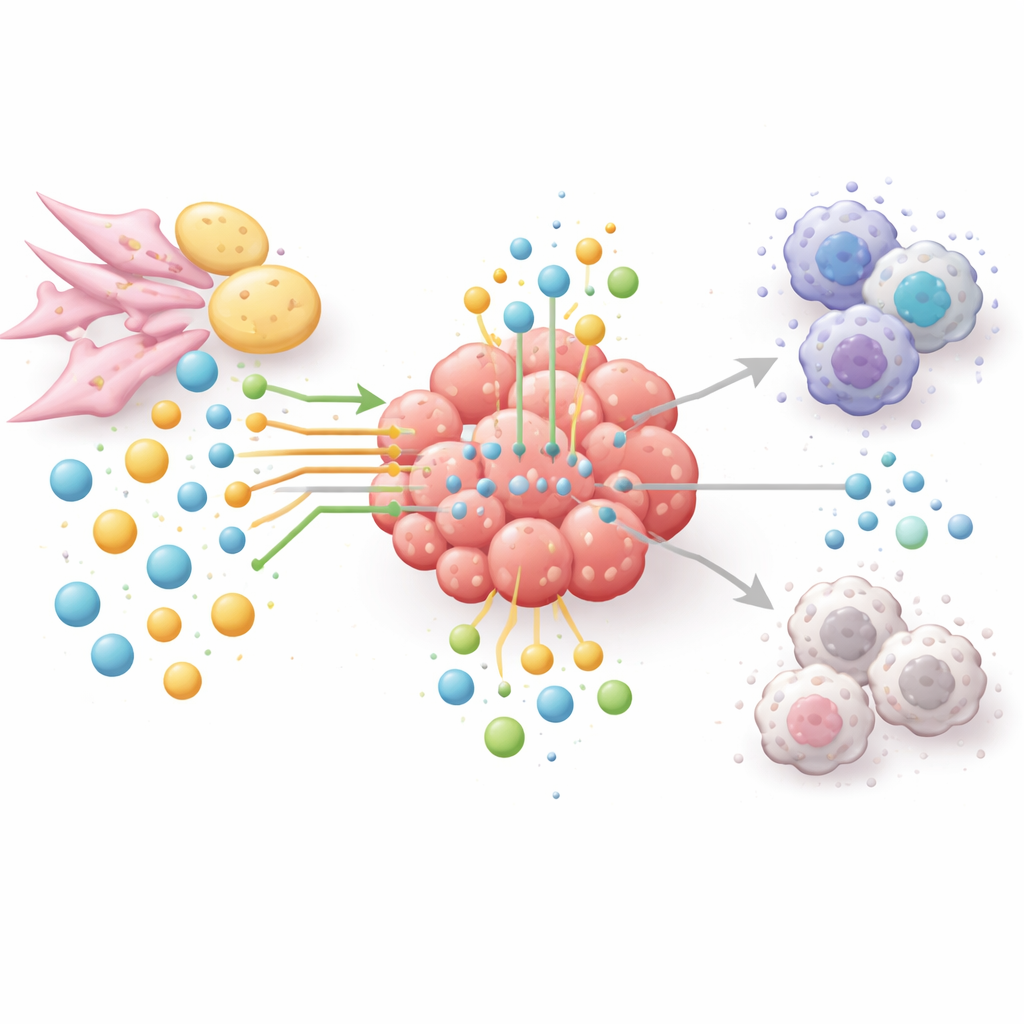
Nieuwe manieren om de tumor uit te hongeren, niet de patiënt
Aangezien aminozuur- en lipidenroutes tumorgroei, immuunontsnapping en therapieresistentie koppelen, pleiten de auteurs voor een netwerkgerichte aanpak in plaats van één-medicijn-voor-één-enzym oplossingen. Experimentele therapieën proberen nu arginine of glutamine te verlagen in zorgvuldig gekozen tumoren, vet-aanmaak of vet-verbrandingsenzymen te blokkeren, of de afbraak van tryptofaan en diens immuun-dempendende producten te stoppen. Veel van deze strategieën worden gecombineerd met immuuncheckpointmiddelen om zowel de tumor te verzwakken als T-cellen opnieuw energie te geven. Om de juiste combinaties en patiënten te kiezen, wendt het veld zich tot ruimtelijke metabolomica, vloeibare biopsieën en kunstmatige intelligentie om in kaart te brengen wie wat eet, waar en wanneer binnen tumoren. Simpel gezegd concludeert het artikel dat winnen van kanker niet alleen vereist dat tumorcellen direct worden aangevallen, maar ook dat het hele voedingsnetwerk dat hen beschermt wordt herschikt.
Bronvermelding: Sung, Y., Kim, D.K., Kim, J.S. et al. Metabolic networks in the tumor microenvironment: roles of amino acid and lipid metabolism pathways in cancer progression and therapy. Exp Mol Med 58, 1128–1148 (2026). https://doi.org/10.1038/s12276-026-01697-0
Trefwoorden: tumor micro-omgeving, kankermetabolisme, aminozuren, lipidenmetabolisme, immunotherapie