Clear Sky Science · fr
Réseaux métaboliques dans le microenvironnement tumoral : rôles des voies du métabolisme des acides aminés et des lipides dans la progression du cancer et la thérapie
Pourquoi le voisinage de la tumeur compte
Le cancer ne se développe pas en isolation. Il vit dans un voisinage animé composé de cellules de soutien, de défenseurs immunitaires et de vaisseaux sanguins, qui partagent et se disputent les ressources. Cet article explore comment les tumeurs reconfigurent l’utilisation des protéines et des graisses — décomposées en acides aminés et lipides — non seulement à l’intérieur des cellules tumorales, mais à travers tout leur environnement. Comprendre cette économie cachée des nutriments aide à expliquer pourquoi certaines tumeurs échappent au système immunitaire et résistent aux traitements, et oriente vers des thérapies plus intelligentes et plus ciblées.
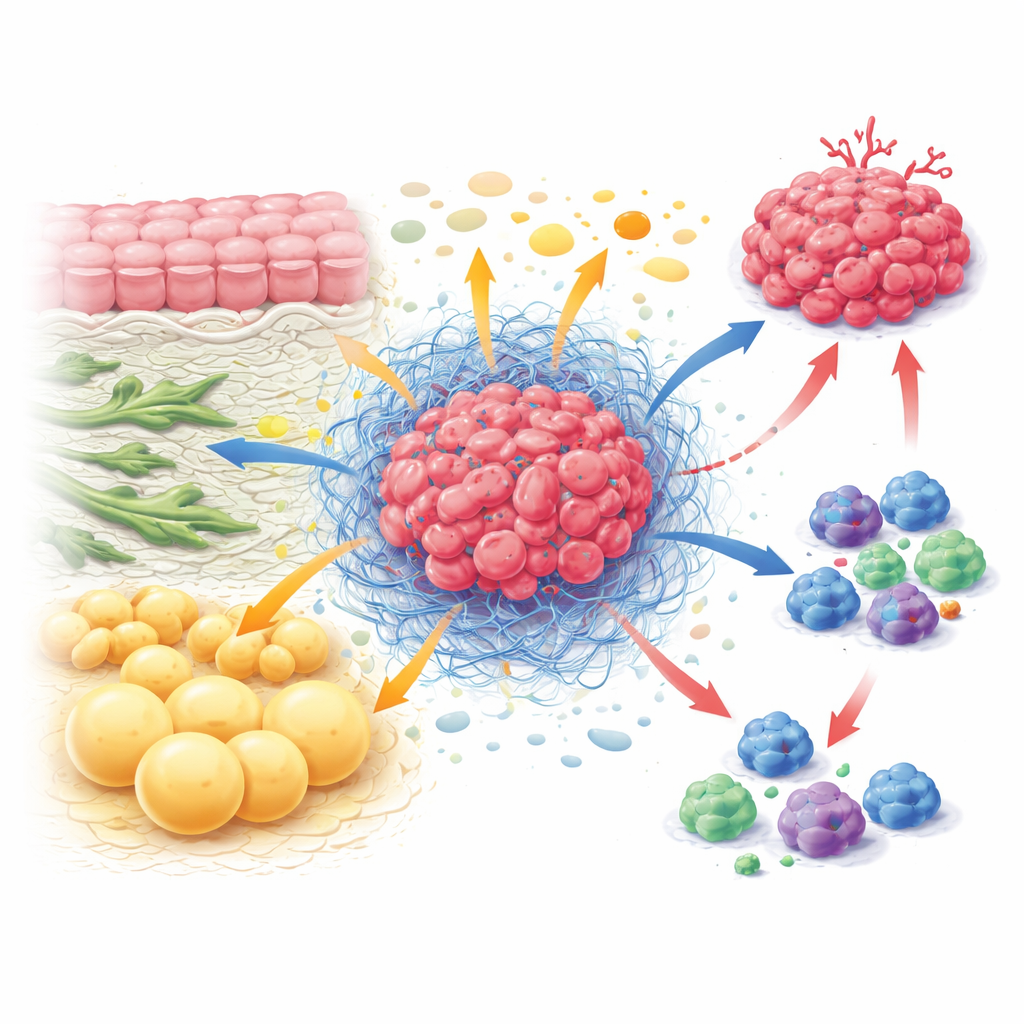
L’économie cachée à l’intérieur d’une tumeur
À l’intérieur d’une tumeur, les cellules cancéreuses coexistent avec des fibroblastes qui façonnent la structure tissulaire, des cellules immunitaires qui tentent d’attaquer, des cellules vasculaires et des adipocytes. Ensemble, ils forment le microenvironnement tumoral, une sorte d’écosystème avec ses propres règles. Plutôt que de fonctionner isolément, les différents types cellulaires échangent et se concurrencent constamment pour les nutriments. Les fibroblastes peuvent alimenter les cellules cancéreuses en éléments constitutifs comme certains acides aminés, tout en rigidifiant le tissu environnant pour empêcher l’entrée des cellules immunitaires. Les cellules immunitaires, lorsqu’elles sont actives, ont besoin de grandes quantités d’énergie pour se diviser et tuer, mais elles se retrouvent souvent affamées parce que les cellules tumorales et stromales accèdent prioritairement aux ressources. Cette lutte permanente pour les nutriments favorise la croissance tumorale tout en affaiblissant les défenses de l’organisme.
Guerres de carburant : les acides aminés comme armes
La revue met en évidence plusieurs acides aminés clés qui jouent à la fois le rôle d’aliments et de signaux. La glutamine, l’arginine, le tryptophane et les acides aminés à chaîne ramifiée sont cruciaux pour les cellules cancéreuses comme pour les cellules immunitaires. Les tumeurs amplifient souvent les systèmes de transport et les enzymes qui leur permettent d’absorber ces nutriments, laissant trop peu aux cellules T cytotoxiques et aux cellules NK. Parallèlement, des cellules de soutien comme les myéloïdes et les fibroblastes peuvent dégrader intentionnellement l’arginine et le tryptophane, générant des sous-produits qui calment les réponses immunitaires et favorisent les cellules T régulatrices tolérantes à la tumeur. Dans certains niches, les cellules partagent aussi des acides aminés pour aider la tumeur à survivre au traitement, ou les recyclent à partir de tissus endommagés, créant des poches de résistance à la chimiothérapie et aux thérapies ciblées.
Les lipides comme carburant, bouclier et messagers
Les lipides — graisses, acides gras, cholestérol et molécules apparentées — jouent des rôles tout aussi importants dans cet écosystème. Les cellules tumorales augmentent à la fois la production et l’oxydation des lipides, utilisant les graisses pour construire des membranes, stocker de l’énergie et résister au stress. Les adipocytes et les fibroblastes voisins peuvent libérer des acides gras que les tumeurs importent et logent dans des gouttelettes lipidiques, de minuscules réservoirs qui protègent contre le stress toxique et de nombreux médicaments. Les cellules immunitaires au sein de la tumeur sont aussi poussées vers une forte dépendance au métabolisme lipidique. Les cellules T régulatrices et certains macrophages utilisent les acides gras pour survivre et rester suppressifs, tandis que les cellules T tueuses surchargées s’épuisent. Des messagers lipidiques spéciaux, tels que la lysophosphatidique, stimulent en outre la croissance tumorale, dirigent la dissémination vers des organes distants et repoussent les cellules immunitaires du cœur tumoral.
Variation dans l’espace, le temps et sous traitement
Le métabolisme au sein d’une tumeur n’est pas uniforme. Les niveaux d’oxygène et de nutriments varient de la périphérie bien nourrie au noyau affamé, et les différents organes qui hébergent des métastases offrent des mélanges nutritifs distincts. En conséquence, certaines régions favorisent la glycolyse, d’autres dépendent davantage de la glutamine ou des lipides, et ces profils évoluent à mesure que la tumeur croît ou subit un traitement. Quand les thérapies coupent une source d’énergie, les tumeurs basculent souvent vers une autre ou s’appuient davantage sur l’aide des fibroblastes et des adipocytes. Ces mêmes changements métaboliques peuvent aussi modifier l’expression génique via des marques épigénétiques, verrouillant des états agressifs ou immunosuppresseurs. Cette flexibilité complique l’efficacité d’une stratégie qui viserait une seule voie.
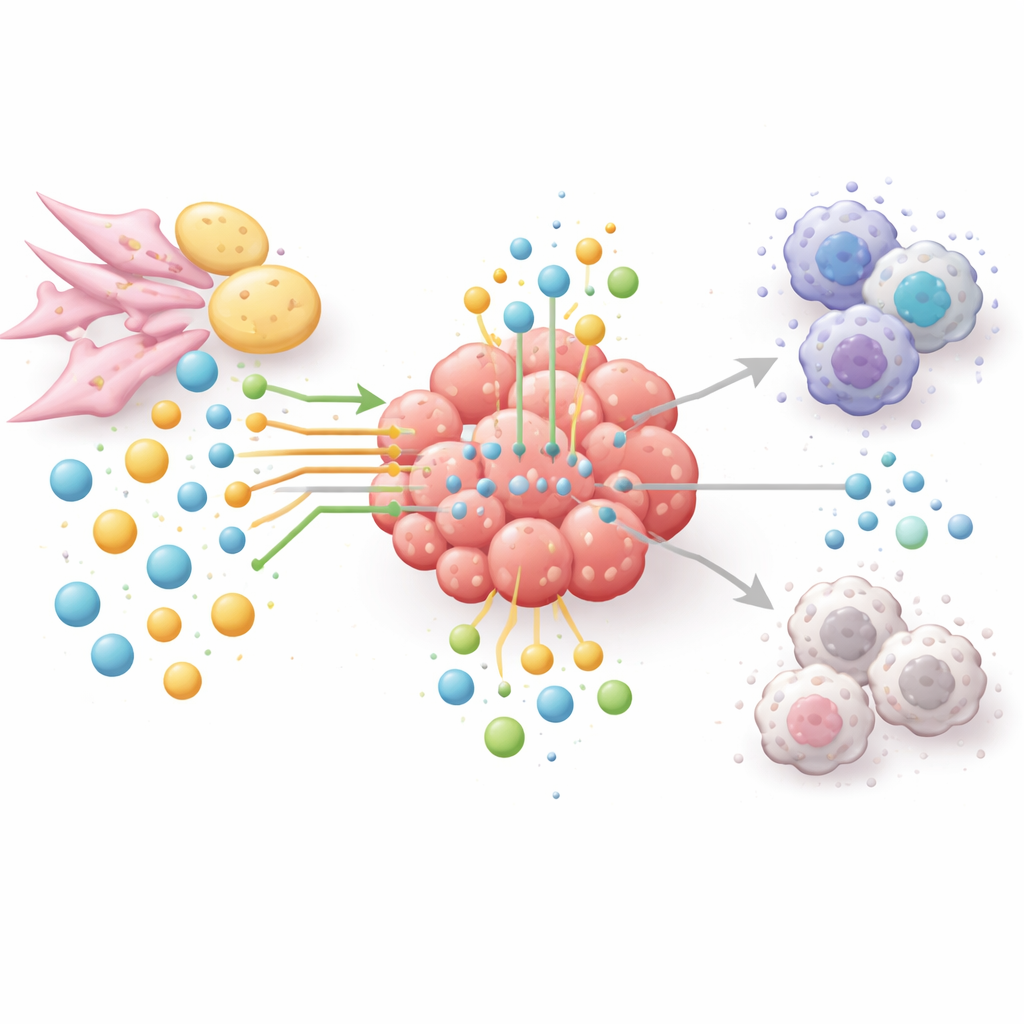
De nouvelles façons d’affamer la tumeur, sans affamer le patient
Parce que les voies des acides aminés et des lipides relient croissance tumorale, évasion immunitaire et résistance thérapeutique, les auteurs préconisent une approche basée sur les réseaux plutôt que des solutions un-médicament-pour-une-enzyme. Des thérapies expérimentales cherchent désormais à diminuer l’arginine ou la glutamine dans des tumeurs soigneusement sélectionnées, bloquer les enzymes de synthèse ou d’oxydation des lipides, ou interrompre la dégradation du tryptophane et ses produits immunodéprimants. Beaucoup de ces stratégies sont combinées avec des inhibiteurs de points de contrôle immunitaires pour affaiblir la tumeur tout en ré-énergisant les cellules T. Pour choisir les bonnes combinaisons et les bons patients, le domaine se tourne vers la métabolomique spatiale, les biopsies liquides et l’intelligence artificielle afin de cartographier qui consomme quoi, où et quand à l’intérieur des tumeurs. En termes simples, l’article conclut que gagner la lutte contre le cancer exigera non seulement d’attaquer directement les cellules tumorales, mais aussi de reconfigurer le réseau nutritif entier qui les protège.
Citation: Sung, Y., Kim, D.K., Kim, J.S. et al. Metabolic networks in the tumor microenvironment: roles of amino acid and lipid metabolism pathways in cancer progression and therapy. Exp Mol Med 58, 1128–1148 (2026). https://doi.org/10.1038/s12276-026-01697-0
Mots-clés: microenvironnement tumoral, métabolisme du cancer, acides aminés, métabolisme des lipides, immunothérapie