Clear Sky Science · he
רשתות מטבוליות במיקרו-סביבה של הגידול: תפקידים של מסלולי חומצות אמינו וליפידים בהתפתחות סרטן וטיפוליו
מדוע השכונה של הגידול חשובה
סרטן לא גדל בבדידות. הוא מתקיים בשכונה עמוסה של תאים תומכים, מגיני מערכת החיסון וכלי דם, שכולם חולקים ומתחרים על דלק. מאמר זה בוחן כיצד גידולים משנים את השימוש בחלבונים ושומנים — מפורקים לחומצות אמינו וליפידים — לא רק בתוך תאי הגידול אלא ברחבי כל סביבתם. הבנת כלכלת המזון המוסתרת הזו מסבירה מדוע חלק מהגידולים בורחים ממערכת החיסון ומפתחים עמידות לטיפול, ומסמנת דרכים לטיפולים חכמים ומדויקים יותר.
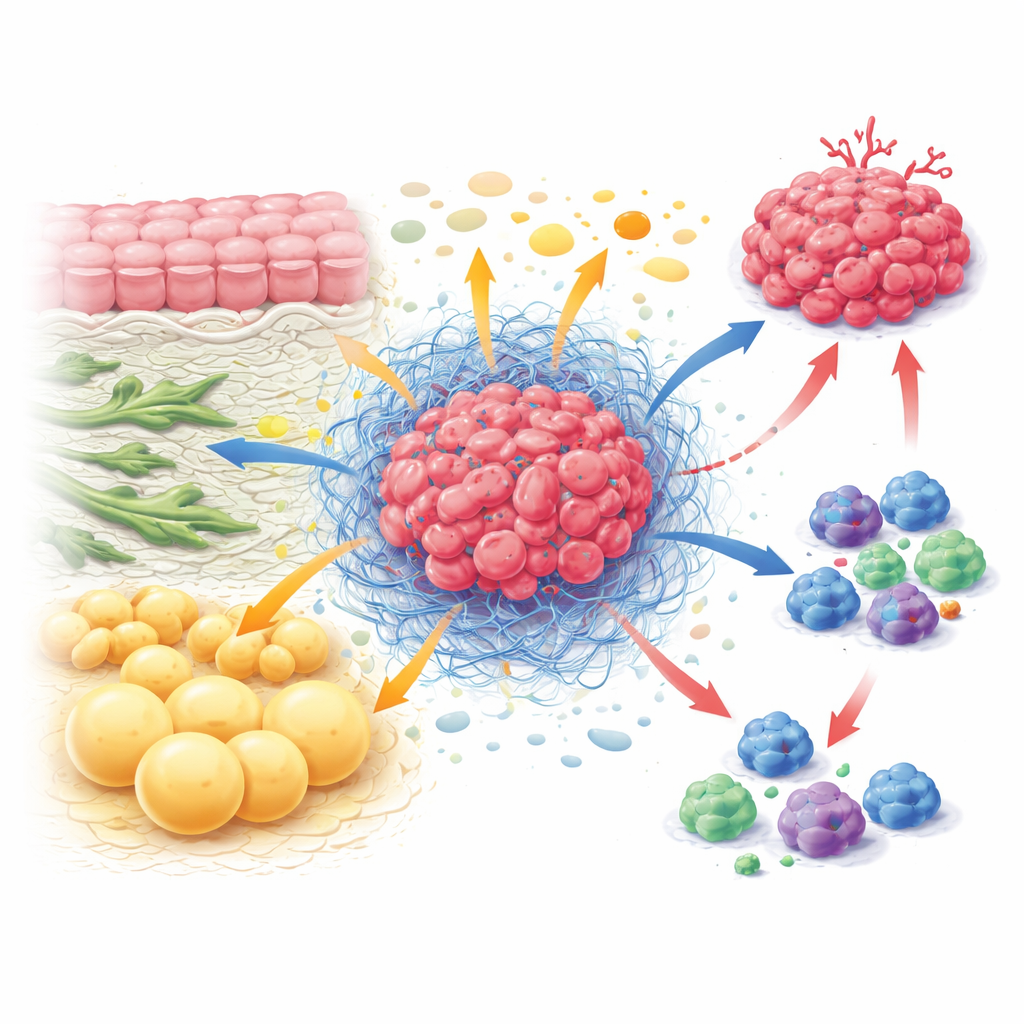
כלכלה נסתרת בתוך הגידול
בתוך הגידול תאי סרטן שותפים קיום עם פיברובלסטים שעוצבים את מבנה הרקמה, תאי מערכת החיסון שמנסים לתקוף, תאים מכלי הדם ותאי שומן. יחד הם יוצרים את המיקרו-סביבה של הגידול — סוג של מערכת אקולוגית עם החוקים שלה. במקום שכל סוג תא יפעל בנפרד, הם סוחרים ומתחרים כל הזמן על מזון. פיברובלסטים יכולים להזין את תאי הסרטן בבוני-מבנה כמו חומצות אמינו מסוימות, ובמקביל להקשיח את הרקמה כך שתאי החיסון לא יוכלו להיכנס בקלות. תאי חיסון, כשהם פעילים, זקוקים לכמויות גדולות של דלק כדי להתחלק ולחסל, אך לעתים קרובות הם מצאו עצמם מוקפאים מרעב כי תאי הסרטן והתאים הסטראומליים מקבלים עדיפות בגישה. הדחיקה הזו והמאבק על המזון מסייעים לגידולים לגדול בעוד הם מחלישים את ההגנות של הגוף.
מלחמות על דלק: חומצות אמינו ככלי נשק
הסקירה מדגישה מספר חומצות אמינו מרכזיות המשמשות גם כמזון וגם כאותות. גלוטמין, ארגינין, טריפטופן וחומצות אמינו מסועפות חשובות הן לתאי סרטן והן לתאי חיסון. גידולים לעתים מגבירים מערכות הובלה ומערכות אנזימטיות שמאפשרות להם לספוג את החומרים המזינים האלה, ולהשאיר כמות לא מספקת לתאי T קטלניים ולתאי טבעיים קטלניים (NK). במקביל, תאים תומכים כמו תאים מיילואידים ופיברובלסטים יכולים לפרק בכוונה ארגינין וטריפטופן, וליצור מוצאי-פעולה שמרגיעים תגובות חיסוניות ומעודדים תאי T רגולטוריים שמסגלים סובלנות לגידול. בנישות מסוימות, תאים גם חולקים חומצות אמינו כדי לעזור לסרטן לשרוד טיפול, או ממחזרים אותן מרקמות פגועות, וכך נוצרים כיסי עמידות לכימותרפיה ותרופות ממוקדות.
שומן כדלק, כמגן וכאות
ליפידים — שומנים, חומצות שומן, כולסטרול ומולקולות קשורות — מגלמים תפקידים חשובים לא פחות במערכת האקולוגית הזו. תאי סרטן מגדילים הן ייצור שומן והן שריפת שומן, משתמשים בשומנים לבניית ממברנות, לאחסן אנרגיה ולהתנגד ללחץ. תאי שומן ופיברובלסטים בקרבת מקום יכולים לשחרר חומצות שומן שהגידול מייבא בקלות ושם בתוך טיפות ליפידיות — מאגרים זעירים שמגנים מפני הלחץ הרעיל והרבה תרופות. גם תאי חיסון בגידול נדחפים לתלות כבדה במטבוליזם של שומנים. תאי T רגולטוריים וסוגים מסוימים של מאקרופאגים משתמשים בחומצות שומן כדי לשרוד ולהישאר מדכאים, בעוד תאי T קטלניים המוצפים הופכים לעייפים. שליחים ליפידיים מיוחדים, כמו ליזופוספטידית חומצה (lysophosphatidic acid), מעודדים עוד יותר צמיחת גידול, מנווטים את הפצת הסרטן לאיברים מרוחקים ודוחפים תאי חיסון מחוץ לגרעין הגידול.
שינוי במרחב, בזמן ובטיפול
המטבוליזם בגידול איננו אחיד. רמות חמצן וחומרים מזינים משתנות מהחלק החיצוני המטופל היטב ועד לליבת הגידול הרעבה, ואיברים שונים המארחים גרורות מציעים תערובות מזון נבדלות. כתוצאה מכך, אזורים מסוימים מעדיפים שריפת סוכר, אזורים אחרים מסתמכים יותר על גלוטמין או שומנים, ותבניות אלה משתנות ככל שהגידול גדל או עומד בפני טיפול. כשטיפולים חותכים מקור דלק אחד, גידולים לעתים קרובות עוברים לאחר או מסתמכים יותר על עזרת פיברובלסטים ותאי שומן. אותן הזזות מטבוליות יכולות גם לשנות כיצד גנים נדלקים או כבויים באמצעות סימנים אפיגנטיים, מה שמנע מהמצב להפוך תוקפני או מדכא-חיסון. גמישות זו מקשה על עצירת סרטן על ידי חסימת מסלול יחיד.
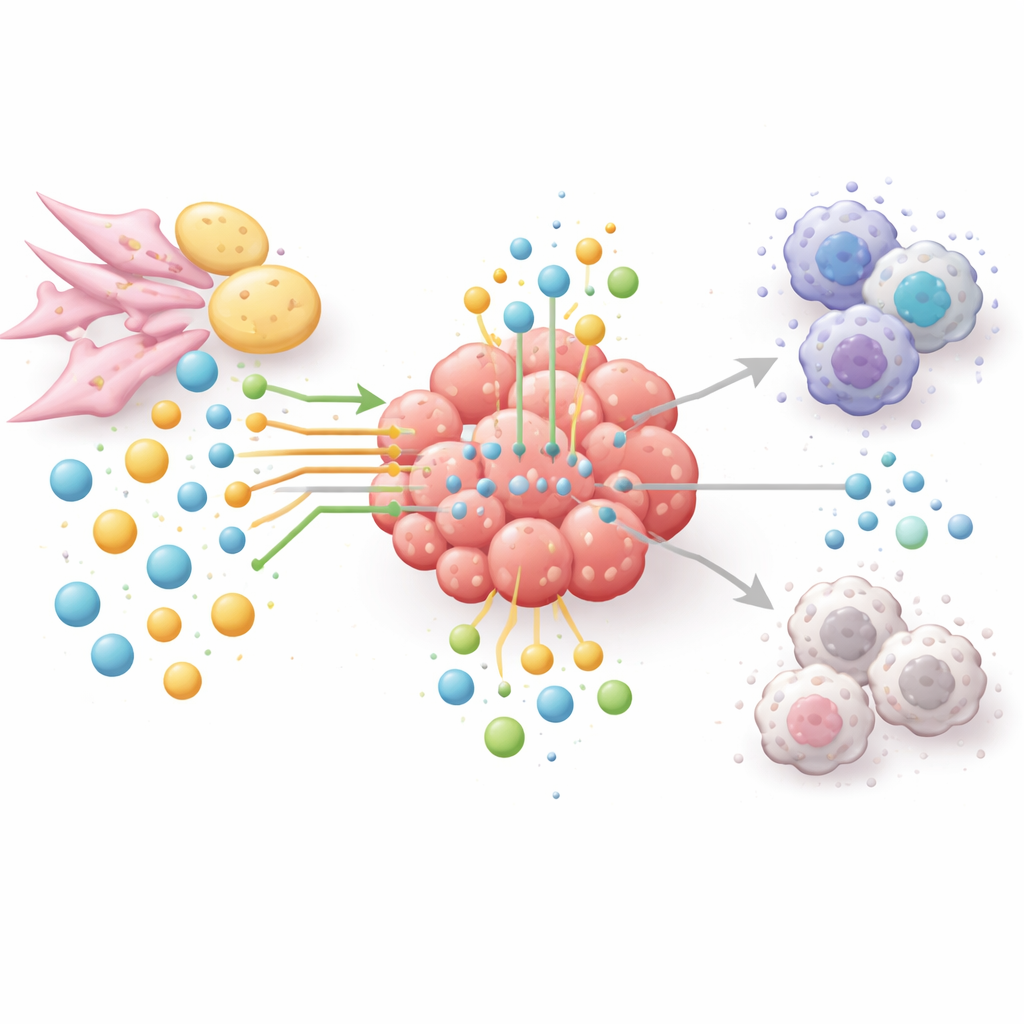
דרכים חדשות להרעיב את הגידול, לא את המטופל
מכיוון שמסלולי חומצות אמינו וליפידים מקשרים בין גדילת הגידול, בריחת חיסון ועמידות לטיפול, המחברים טוענים לגישה מבוססת רשת במקום פתרונות של תרופה אחת עבור אנזים אחד. ניסויים טיפוליים כיום שואפים להפחית ארגינין או גלוטמין בגידולים שנבחרו בקפידה, לחסום אנזימים ליצירת שומן או לפרוק שומן, או לעצור את פירוק הטריפטופן ואת תוצריו המדכאים חיסונית. רבות מהאסטרטגיות האלו משולבות עם תרופות נחיתות חסימות צומת חיסון כדי להחליש את הגידול ולתת כוח מחדש לתאי T. כדי לבחור את הצירופים והמטופלים המתאימים, התחום פונה למטבולומיקה מרחבית, ביופסיות נוזליות ובינה מלאכותית כדי למפות מי אוכל מה, היכן ומתי בתוך הגידולים. בפשטות, המאמר מסכם שניצחון על הסרטן ידרוש לא רק מתקפה ישירה על תאי הגידול, אלא גם שכתוב רשת המזונות כולה שמגנה עליהם.
ציטוט: Sung, Y., Kim, D.K., Kim, J.S. et al. Metabolic networks in the tumor microenvironment: roles of amino acid and lipid metabolism pathways in cancer progression and therapy. Exp Mol Med 58, 1128–1148 (2026). https://doi.org/10.1038/s12276-026-01697-0
מילות מפתח: מיקרו-סביבה של הגידול, מטבוליזם של סרטן, חומצות אמינו, מטבוליזם של ליפידים, אימונותרפיה