Clear Sky Science · tr
Tümör mikroçevresindeki metabolik ağlar: kanser progresyonu ve tedavisinde amino asit ile lipid metabolizma yollarının rolleri
Tümörün Komşuluğu Neden Önemli?
Kanser izole bir şekilde büyümez. Destek hücreleri, bağışıklık savunucuları ve kan damarlarıyla dolu yoğun bir mahallede yaşar; hepsi yakıt üzerinde paylaşır ve çatışır. Bu makale, kanserlerin protein ve yağ kullanımını—amino asitler ve lipidler olarak ayrılan—sadece tümör hücrelerinin içinde değil, tüm çevre boyunca nasıl yeniden düzenlediğini inceliyor. Bu besinlerin gizli ekonomisini anlamak, bazı tümörlerin neden bağışıklık sisteminden kaçtığını ve tedaviye direnç gösterdiğini açıklar ve daha akıllı, daha kesin tedavilere işaret eder.
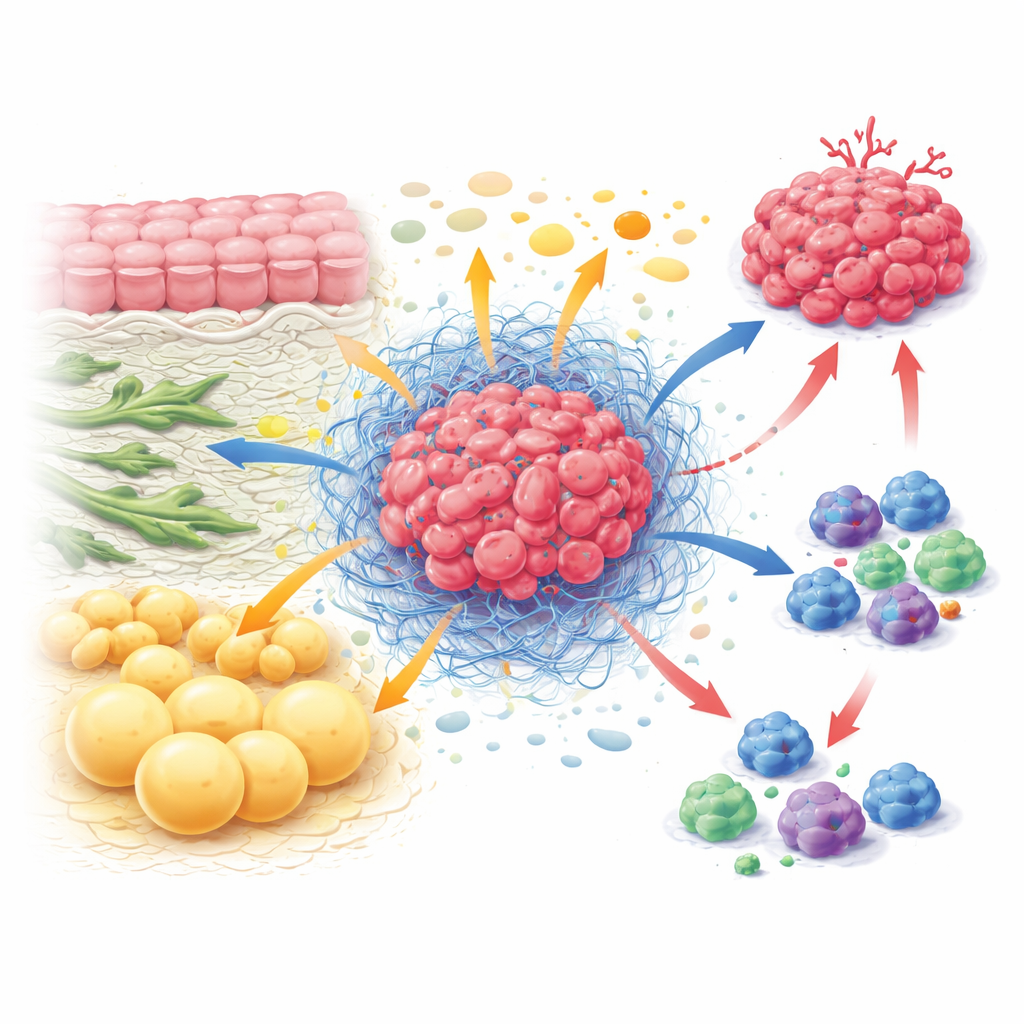
Tümör İçindeki Gizli Ekonomi
Bir tümörün içinde, kanser hücreleri doku yapısını şekillendiren fibroblastlar, saldırmaya çalışan bağışıklık hücreleri, damar hücreleri ve yağ hücreleri ile bir arada bulunur. Birlikte onlar kendi kuralları olan bir tür ekosistem olan tümör mikroçevresini oluştururlar. Her hücre tipi tek başına çalışmak yerine, sürekli olarak besinleri takas eder ve bunlar için rekabet eder. Fibroblastlar belirli amino asitler gibi yapı taşlarıyla kanser hücrelerini besleyebilirken, bağışıklık hücrelerinin kolayca girmesini engelleyecek şekilde çevre dokuyu sertleştirebilir. Aktif olduklarında bağışıklık hücreleri bölünüp öldürebilmek için büyük miktarda yakıta ihtiyaç duyarlar; buna rağmen genellikle kanser ve stromal hücreler öncelikli erişim sağladığı için aç kalırlar. Besinler üzerindeki bu sürekli çekişme, tümörlerin büyümesine yardımcı olurken vücudun savunmasını zayıflatır.
Yakıt Savaşları: Amino Asitler Birer Silah
Derleme, hem besin hem de sinyal görevi gören birkaç kilit amino asidi vurguluyor. Glutamin, arjinin, triptofan ve dallı zincirli amino asitler hem kanser hücreleri hem de bağışıklık hücreleri için kritik önemdedir. Tümörler sıklıkla bu besinleri emmelerine olanak veren taşıma sistemlerini ve enzimleri artırır; geride öldürücü T hücreleri ve doğal öldürücü hücreler için çok az kalır. Aynı zamanda miyeloid hücreler ve fibroblastlar gibi destek hücreleri arjinin ve triptofanu kasıtlı olarak parçalayarak bağışıklık yanıtlarını yatıştıran ve tümöre tolerans gösteren düzenleyici T hücrelerini teşvik eden yan ürünler üretebilir. Bazı nişlerde hücreler kanserin tedaviye direnmesine yardımcı olmak için amino asitleri paylaşır ya da hasarlı dokulardan geri dönüştürür; bu da kemoterapi ve hedefe yönelik ilaçlara karşı direnç cepleri oluşturur.
Yağ: Yakıt, Kalkan ve Sinyal
Lipidler—yağlar, yağ asitleri, kolesterol ve ilişkili moleküller—bu ekosistemde eşit derecede önemli roller oynar. Kanser hücreleri hem yağ üretimini hem de yağ yakımını artırır; yağları zarlar oluşturmak, enerji depolamak ve strese karşı direnç sağlamak için kullanırlar. Yakınlardaki yağ hücreleri ve fibroblastlar, tümörlerin kolayca alıp lipid damlacıklarına yerleştirdiği yağ asitlerini serbest bırakabilir; bu küçük depolar toksik stresten ve birçok ilaçtan koruma sağlar. Tümördeki bağışıklık hücreleri de yağ metabolizmine ağır bir bağımlılığa itilir. Düzenleyici T hücreleri ve belirli makrofajlar yağ asitlerini kullanarak hayatta kalır ve baskılayıcı kalırken, aşırı yüklenmiş öldürücü T hücreleri tükenmiş hale gelir. Lizofosfatidik asit gibi özel lipid haberci moleküller, tümör büyümesini daha da uyarmak, kanserin uzak organlara yayılmasını yönlendirmek ve bağışıklık hücrelerini tümör merkezinden uzaklaştırmak için etki gösterir.
Mekân, Zaman ve Tedaviyle Değişen Bir Manzara
Tümördeki metabolizma tekdüze değildir. Oksijen ve besin düzeyleri iyi beslenmiş dış çevreden açlıktan bunalmış çekirdeğe kadar değişir ve metastazlara ev sahipliği yapan farklı organlar farklı besin karışımları sunar. Sonuç olarak bazı bölgeler şeker yakımını tercih ederken, diğerleri daha çok glutamin veya yağlara dayanır ve bu desenler tümör büyüdükçe ya da tedaviyle karşılaştıkça kayar. Tedaviler bir yakıtı kesince, tümörler genellikle başka birine geçer veya fibroblastlar ve yağ hücrelerinin desteğine daha çok güvenir. Aynı metabolik değişimler, epigenetik işaretler yoluyla hangi genlerin açılıp kapandığını da etkileyerek agresif veya bağışıklık-baskılayıcı durumları sabitleyebilir. Bu esneklik, tek bir yolu bloke ederek kanseri durdurmayı zorlaştırır.
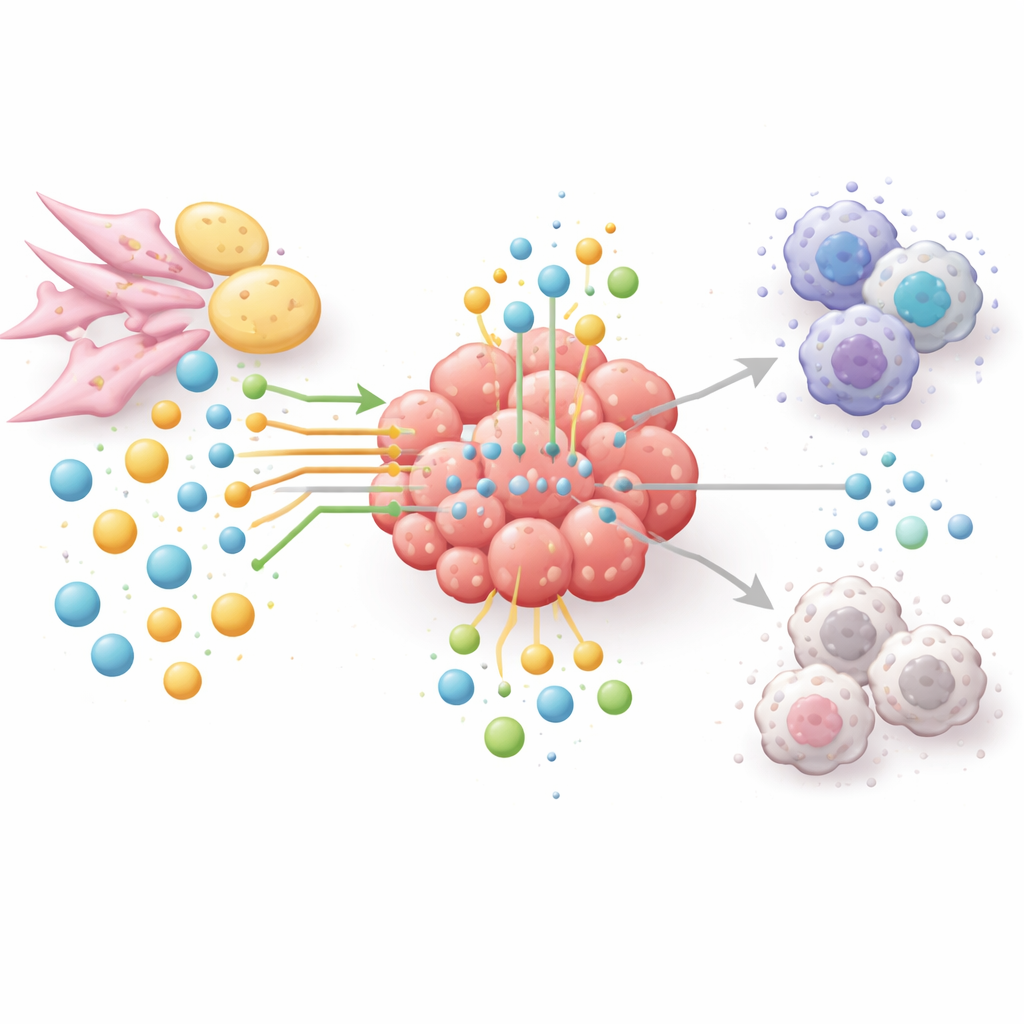
Tümörü Değil Hastayı Aç Bırakmadan Yıldırmanın Yeni Yolları
Amino asit ve lipid yolları tümör büyümesi, bağışıklıktan kaçış ve tedavi direnci arasında bağ kurduğundan, yazarlar tek ilaç-te Tek enzim çözümlerinden ziyade ağ tabanlı bir yaklaşımı savunuyor. Deneysel tedaviler artık dikkatle seçilmiş tümörlerde arjinin veya glutamini düşürmeyi, yağ yapımını veya yağ yakımını sağlayan enzimleri engellemeyi ya da triptofandan parçalanmayı ve onun bağışıklığı söndüren ürünlerini kapatmayı hedefliyor. Bu stratejilerin birçoğu tümörü zayıflatmak ve T hücrelerini yeniden canlandırmak için immün kontrol noktası ilaçlarıyla birleştiriliyor. Doğru kombinasyonları ve hastaları seçmek için alan, kim nerede ve ne zaman ne yiyor haritasını çıkarmak adına mekânsal metabolomik, sıvı biyopsiler ve yapay zekâya yöneliyor. Basit ifadeyle makale, kansere karşı kazanmanın sadece tümör hücrelerine doğrudan saldırmak değil, onları barındıran tüm besin ağını yeniden yapılandırmak gerektireceği sonucuna varıyor.
Atıf: Sung, Y., Kim, D.K., Kim, J.S. et al. Metabolic networks in the tumor microenvironment: roles of amino acid and lipid metabolism pathways in cancer progression and therapy. Exp Mol Med 58, 1128–1148 (2026). https://doi.org/10.1038/s12276-026-01697-0
Anahtar kelimeler: tümör mikroçevresi, kanser metabolizması, amino asitler, lipid metabolizması, immünoterapi