Clear Sky Science · zh
仿生肽自组装:与生物大分子接口以调控细胞信号传导
构建微小结构以与细胞对话
在每个细胞内部,无数分子碰撞、结合并解离,产生维持生命所需的信号。本文综述探讨了如何设计非常短的蛋白片段——肽,使其自发地组织成微小形态,附着于细胞组分并有针对性地调节这些信号。通过学习并模仿自然的策略,科学家希望构建智能材料,能够有选择性地杀死癌细胞、纠正错误信号或以远高于现有药物的精确度递送基因治疗。
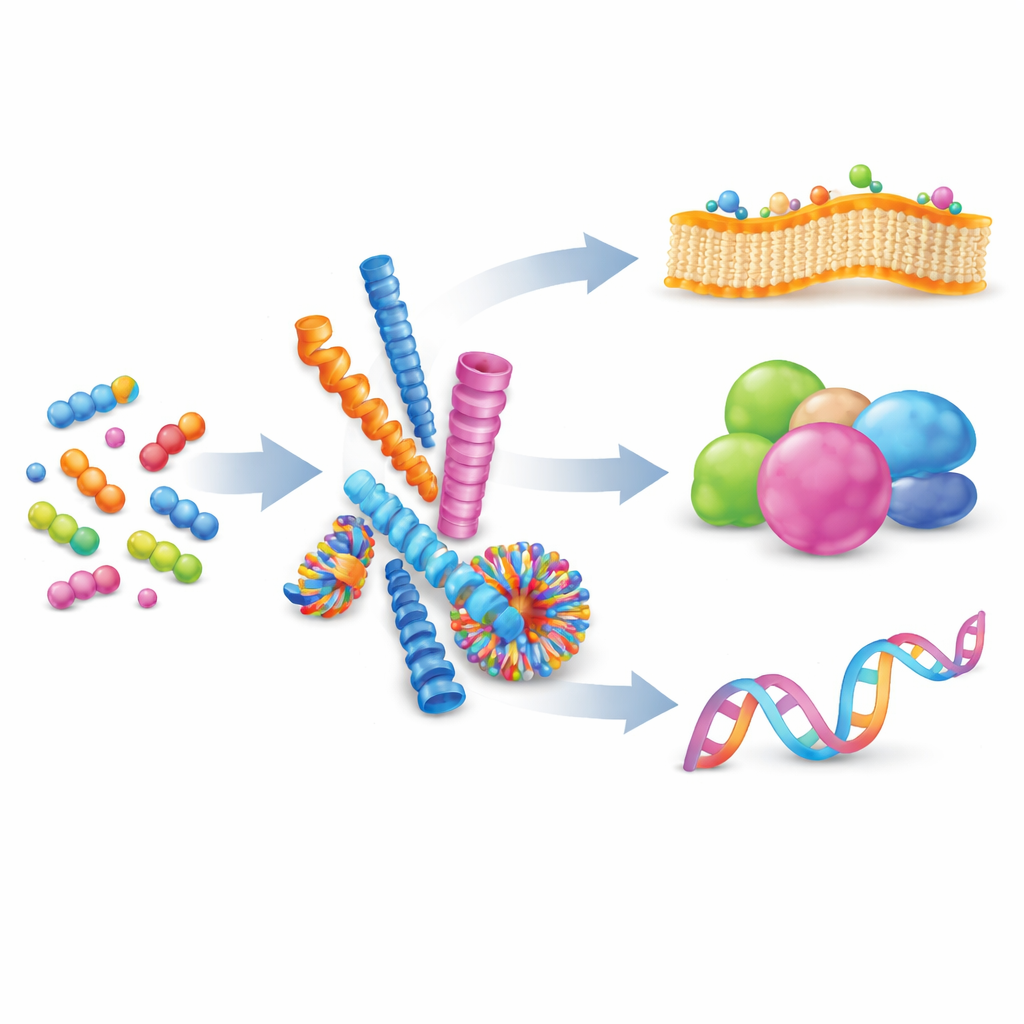
从游离分子到有序纳米结构
作者首先解释了超分子自组装:一种许多小分子通过温和相互吸引而无需形成永久化学键就能组织成更大结构的过程。通过平衡电荷、氢键以及芳香环间的堆积等作用力,化学家可以诱导肽形成纳米纤维、球体、管或囊泡。这些形态并非静态;其构件可以出入交换,使组装体具可逆性和适应性。当许多弱相互作用在共同表面上同时发生时,会产生“多价性”,这是一种能显著增强原本微弱结合事件的强有力方式,类似于多个微小挂钩同时抓住一个表面。
借用自然的剧本
自然已经依赖自组装来执行复杂任务。蛋白质从简单的氨基酸链折叠成复杂的三维构型,暴露出可与其他蛋白质、DNA或膜结合的广阔接触面。这些接触通常分布在大面积上,使细胞能快速且可逆地开关信号。受此启发,研究者现在设计人工肽来模仿此类界面。与聚合物、脂类或DNA框架相比,肽系统提供了一个理想平衡点:它们具有生物相容性、化学多样性,并能在单个氨基酸水平上实现精确控制,从而可细致调节形状、电荷和结合行为。本文重点讨论这些人工肽组装体如何用于作用于三大目标:细胞膜、蛋白质和核酸。
从膜向内重布细胞网络
文章的一个主要主题是利用肽自组装直接作用于细胞膜,尤其是线粒体、溶酶体、内质网和高尔基体等关键细胞器的膜。肽可以被修饰以带有定位基团,引导它们到达特定细胞器,在那里局部环境——如酸性、膜电位或酶活性——触发其在膜表面组装成纳米纤维或颗粒。例如在粒线体中,某些设计在细胞内分散时无害,但一旦被该细胞器的负电位浓缩,就会聚集成刚性纤维。这些纤维可以刺穿或破坏双层膜,崩溃能量梯度,释放细胞色素c,并激活程序性细胞死亡途径,这对于攻击肿瘤细胞具有价值。
将降解隔室变为控制中枢
溶酶体常被简单地视为细胞的回收中心,而在此则被重新塑造成决定生死的开关板。被设计为感知溶酶体酸性pH或驻留酶的肽,仅在被细胞吞噬并运入该隔室后才会组装。组装后,它们的纳米结构可以削弱溶酶体膜,使如胱天蛋白酶等消化酶泄漏并触发细胞死亡。其他肽系统被设计为在精心选择的阶段从溶酶体逃逸,帮助将治疗货物如核酸运入细胞内部。将类似策略应用于内质网和高尔基体可以调节“应激”反应或扰乱蛋白分拣通路,再次以可控方式引导细胞走向自毁。
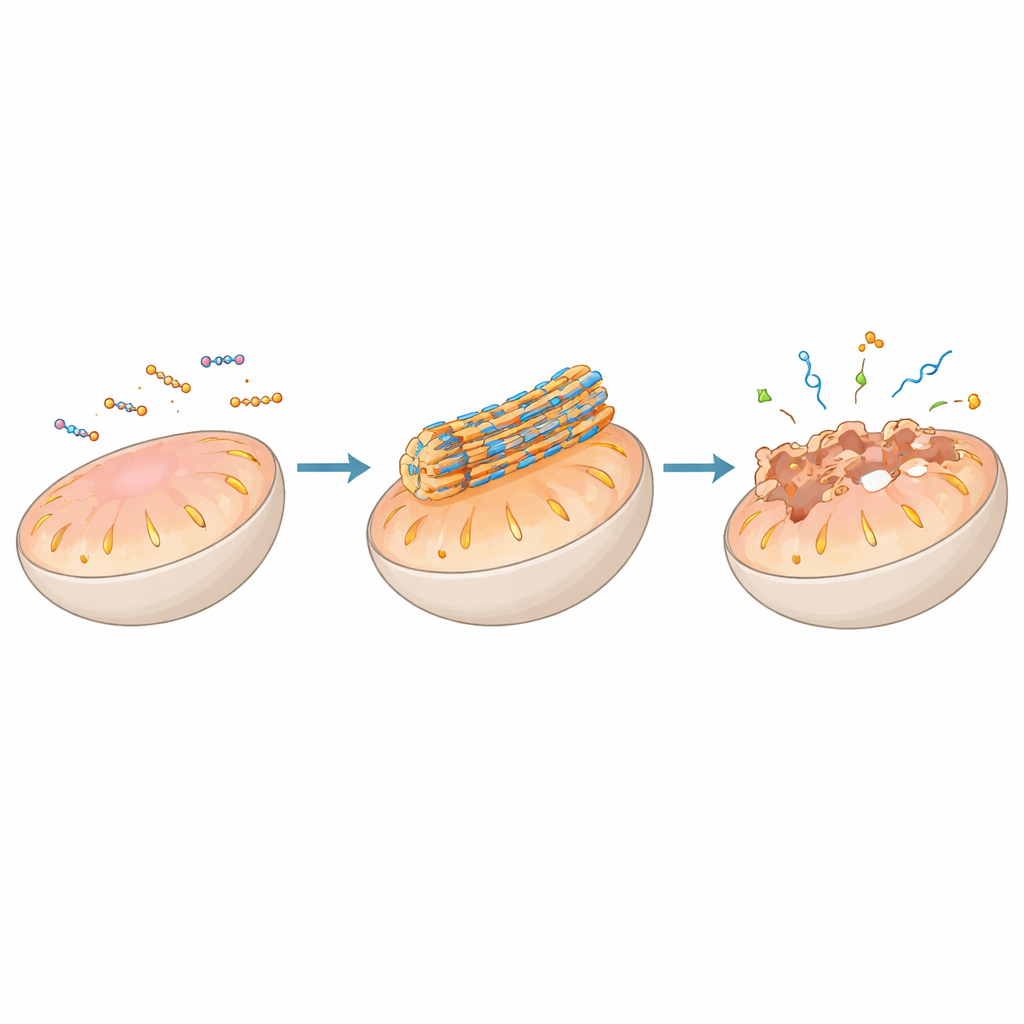
用肽支架引导蛋白与基因
除了膜之外,肽组装体还可以夹持蛋白或核酸,重塑整个信号网络。有些组装体对天然蛋白结合片段的模仿非常成功,以至于它们能塞入曾被认为难以药物化的蛋白–蛋白界面,释放线粒体中的促死信号或阻断细胞表面的生长信号。其他则与抗体或受体共同组装,使其聚集、被标记送往溶酶体降解,或增强免疫对癌细胞的识别。当与DNA或RNA结合时,带正电的肽能将遗传物质压缩成紧凑颗粒或类液滴,易于进入细胞并在适当的时间和地点释放货物,从而实现基因沉默或激活。在某些情况下,肽–RNA液滴表现得像人工“凝聚体”,呼应细胞在危机时自然形成以管理RNA的应激颗粒。
这些微小构建者为何重要
综述的结论是,仿生肽自组装为以分子级精度重塑细胞行为提供了灵活的工具箱。由于这些系统对局部触发器作出响应并能自我重组,它们原则上可以区分病变细胞与健康细胞,仅在需要之处发挥作用——通过打孔能量工厂、扰乱回收中心、沉默有害基因或重新点燃免疫攻击。作者认为,随着成像、建模和设计方法的改进,这些微小构建者可能从实验室的奇趣之物演进为新一代适应性药物,使用与细胞相同的结构语言进行“对话”。
引用: Kim, D., Park, G., Seu, MS. et al. Biomimetic peptide self-assembly: interfacing with biomacromolecules to regulate cellular signaling. Exp Mol Med 58, 1038–1052 (2026). https://doi.org/10.1038/s12276-026-01691-6
关键词: 肽自组装, 细胞信号传导, 纳米医学, 靶向细胞器治疗, 超分子生物材料