Clear Sky Science · pl
Biomimetyczne samozorganizowanie peptydów: interfejs z biomakromolekułami w celu regulacji sygnalizacji komórkowej
Budowanie maleńkich struktur, które komunikują się z komórkami
W każdej komórce niezliczone cząsteczki zderzają się, wiążą i rozdzielają, tworząc sygnały podtrzymujące życie. Ten przegląd bada, jak bardzo krótkie fragmenty białek, zwane peptydami, można zaprojektować tak, by spontanicznie porządkowały się w drobne kształty, które przyczepiają się do komponentów komórkowych i delikatnie kierują tymi sygnałami w pożądanych kierunkach. Poprzez naśladowanie strategii natury naukowcy dążą do tworzenia inteligentnych materiałów, które selektywnie zabijają komórki nowotworowe, korygują wadliwą sygnalizację lub precyzyjniej dostarczają terapie genowe niż współczesne leki.
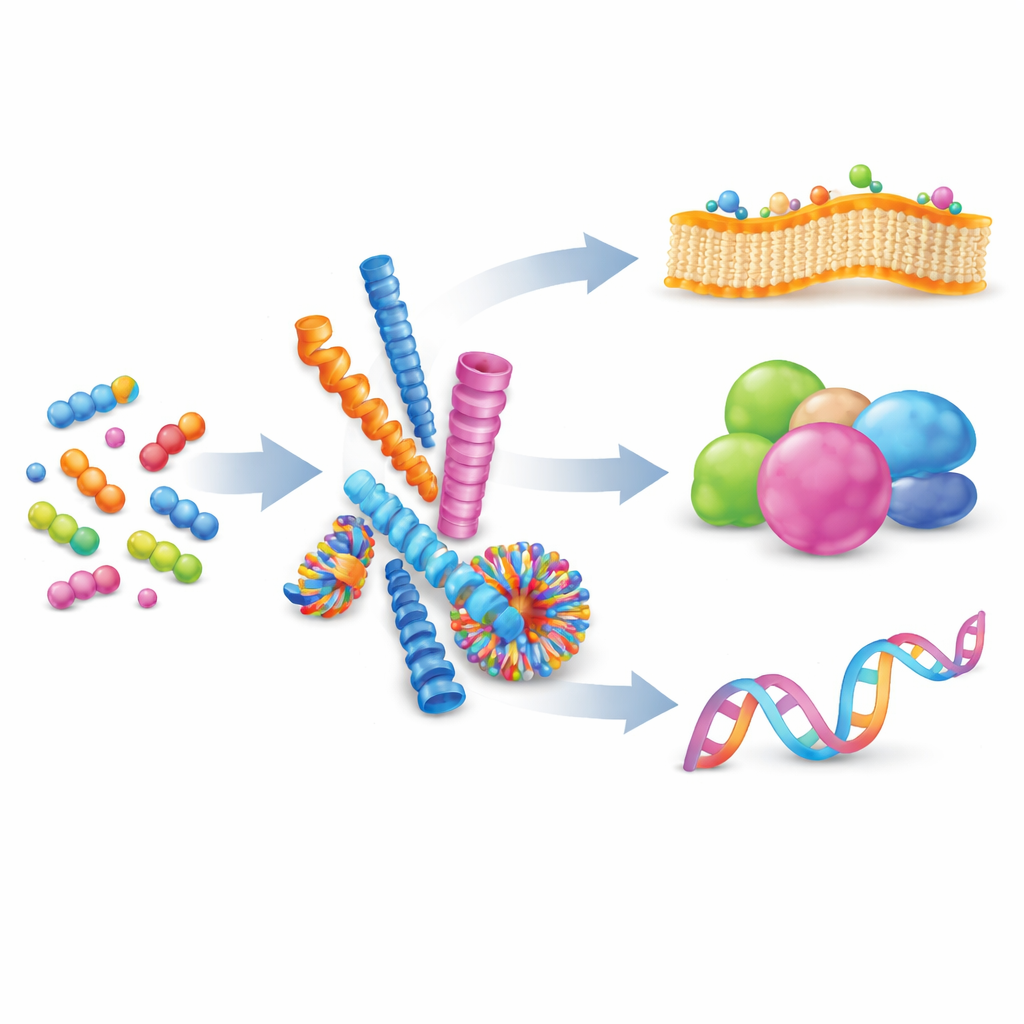
Od luźnych cząsteczek do zorganizowanych nanostruktur
Autorzy zaczynają od wyjaśnienia supramolekularnego samozorganizowania: procesu, w którym wiele małych cząsteczek słabo się przyciąga i organizuje w większe struktury bez tworzenia trwałych wiązań chemicznych. Poprzez wyważenie sił takich jak ładunek, wiązania wodorowe czy oddziaływania sprzężeń pierścieni aromatycznych, chemicy mogą skłonić peptydy do tworzenia nanowłókien, sfer, rur lub pęcherzy. Te kształty nie są statyczne; ich cegiełki mogą się wymieniać, co czyni zespoły odwracalnymi i adaptacyjnymi. Gdy wiele słabych oddziaływań zachodzi jednocześnie na wspólnej powierzchni, tworzy się „multiewalencja” — potężny sposób wzmocnienia inaczej słabego wiązania, podobnie jak wiele małych haczyków chwytających powierzchnię naraz.
Pobieranie kart z instrukcji natury
Natura już polega na samozorganizowaniu przy wykonywaniu złożonych zadań. Białka składają się z prostych łańcuchów aminokwasów, które składają się w skomplikowane, trójwymiarowe formy, odsłaniając szerokie powierzchnie kontaktu wiążące inne białka, DNA lub błony. Te kontakty, często rozłożone na dużych powierzchniach, pozwalają komórkom szybko i odwracalnie przełączać sygnalizację. Zainspirowani tym, badacze projektują teraz sztuczne peptydy imitujące takie interfejsy. W porównaniu z polimerami, lipidami czy rusztowaniami DNA, układy peptydowe oferują korzystny kompromis: są biokompatybilne, chemicznie różnorodne i precyzyjne na poziomie pojedynczych aminokwasów, co pozwala na dokładne strojenie kształtu, ładunku i właściwości wiążących. Ten przegląd koncentruje się na tym, jak te syntetyczne zespoły peptydowe wykorzystuje się do oddziaływania z trzema głównymi celami: błonami komórkowymi, białkami i kwasami nukleinowymi.
Przeprogramowywanie komórki od błony do wnętrza
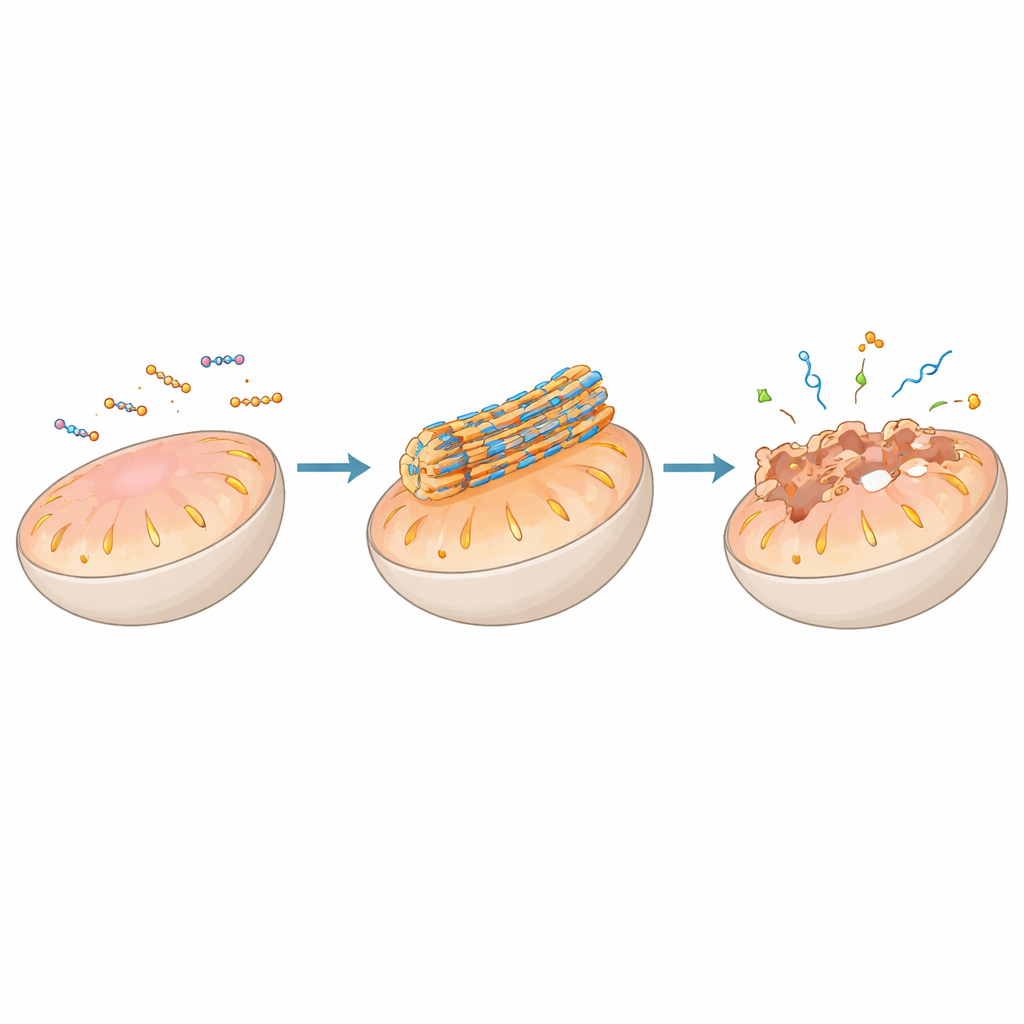
Głównym wątkiem artykułu jest stosowanie samozorganizowania peptydów do działania bezpośrednio na błonach komórkowych, zwłaszcza błonach kluczowych organelli, takich jak mitochondria, lizosomy, retikulum endoplazmatyczne i aparat Golgiego. Peptydy mogą być ozdobione grupami kierującymi, które prowadzą je do konkretnego organellum, gdzie lokalne warunki — takie jak kwasowość, potencjał elektryczny czy aktywność enzymatyczna — wyzwalają ich składanie w nanowłókna lub cząstki na powierzchni błony. W mitochondriach, na przykład, niektóre projekty są nieszkodliwe w stanie rozproszonym w komórce, lecz agregują w sztywne włókna po skoncentrowaniu przez ujemne napięcie organellum. Włókna te mogą przebić lub destabilizować podwójną błonę, niwecząc gradient energetyczny, uwalniając cytochrom c i uruchamiając programowaną śmierć komórki — mechanizm cenny w atakowaniu komórek nowotworowych.
Przekształcanie degradacyjnych compartmentów w centra kontroli
Lizosomy, często uważane jedynie za komórkowe ośrodki recyklingu, są tu przedstawione jako centralne panele decyzyjne dotyczące życia i śmierci. Peptydy zaprojektowane do wykrywania kwasowego pH lizosomu lub obecnych tam enzymów mogą składać się dopiero po zostaniu pochłonięte przez komórkę i przetransportowane do tego kompartmentu. Po złożeniu ich nanostruktury mogą osłabić błonę lizosomalną, umożliwiając wyciek enzymów trawiennych, takich jak katepsyny, które wywołują śmierć komórki. Inne systemy peptydowe zaprojektowano tak, by uciekały z lizosomów na starannie dobranych etapach, pomagając dostarczyć terapeutyczny ładunek, taki jak kwasy nukleinowe, do wnętrza komórki. Podobne strategie stosowane wobec retikulum endoplazmatycznego i aparatu Golgiego pozwalają badaczom zwiększać odpowiedzi na „stres” lub zaburzać sortowanie białek, ponownie kierując komórki w stronę kontrolowanej autodestrukcji.
Ukierunkowywanie białek i genów za pomocą szkieletów peptydowych
Ponad błony, zespoły peptydowe mogą zaciskać się na białkach lub kwasach nukleinowych i przekształcać całe sieci sygnałowe. Niektóre struktury naśladują naturalne segmenty wiążące białka tak dobrze, że wklinają się w interfejsy białko–białko, które wcześniej uważano za nieuleczalne, uwalniając sygnały pro‑apoptotyczne w mitochondriach lub blokując sygnały wzrostu na powierzchni komórek. Inne współskładają się z przeciwciałami lub receptorami, grupując je, znakując do usunięcia w lizosomach lub wzmacniając rozpoznanie nowotworu przez układ odpornościowy. W połączeniu z DNA lub RNA, naładowane dodatnio peptydy kondensują materiał genetyczny w kompaktowe cząstki lub płynne krople, które przenikają do komórek i uwalniają ładunek we właściwym czasie i miejscu, umożliwiając wyciszanie lub aktywację genów. W niektórych przypadkach peptydowo‑RNA’owe krople zachowują się jak sztuczne „kondensaty”, przypominające grudki stresowe, które komórki naturalnie tworzą, by zarządzać RNA podczas kryzysów.
Dlaczego ci mali budowniczowie mają znaczenie
W podsumowaniu przegląd stwierdza, że biomimetyczne samozorganizowanie peptydów oferuje elastyczny zestaw narzędzi do przekształcania zachowania komórek z precyzją na poziomie molekularnym. Ponieważ te systemy reagują na lokalne wyzwalacze i potrafią się przebudowywać, mogą w zasadzie odróżniać komórki chore od zdrowych i działać tylko tam, gdzie to potrzebne — przez przebijanie „fabryk energii”, zakłócanie centrów recyklingu, wyciszanie szkodliwych genów lub ponowne uruchamianie odpowiedzi immunologicznej. Autorzy argumentują, że w miarę postępów w obrazowaniu, modelowaniu i metodach projektowania, ci mali budowniczowie mogą ewoluować z ciekawostek laboratoryjnych w nową generację adaptacyjnych leków, które mówią tym samym strukturalnym językiem co sama komórka.
Cytowanie: Kim, D., Park, G., Seu, MS. et al. Biomimetic peptide self-assembly: interfacing with biomacromolecules to regulate cellular signaling. Exp Mol Med 58, 1038–1052 (2026). https://doi.org/10.1038/s12276-026-01691-6
Słowa kluczowe: samozorganizowanie peptydów, sygnalizacja komórkowa, nanomedycyna, terapia ukierunkowana na organelle, supramolekularne biomateriały