Clear Sky Science · ja
生体模倣ペプチドの自己組織化:生体高分子と接し細胞シグナルを制御する
微小構造を作って細胞と対話する
すべての細胞内部で、無数の分子が衝突し、結合し、解離することで私たちの生命を支えるシグナルが生まれます。本総説は、ペプチドと呼ばれる非常に短いタンパク質断片がどのように設計され、自発的に微小な形状へと整列し、細胞構成要素に結びついてそのシグナルを有益な方向へと促すかを探ります。自然の戦略を模倣することを学ぶことで、研究者はがん細胞を選択的に死に導いたり、誤ったシグナルを訂正したり、遺伝子治療を現在の薬よりも遥かに高精度で届けるスマートな材料を構築することを目指しています。
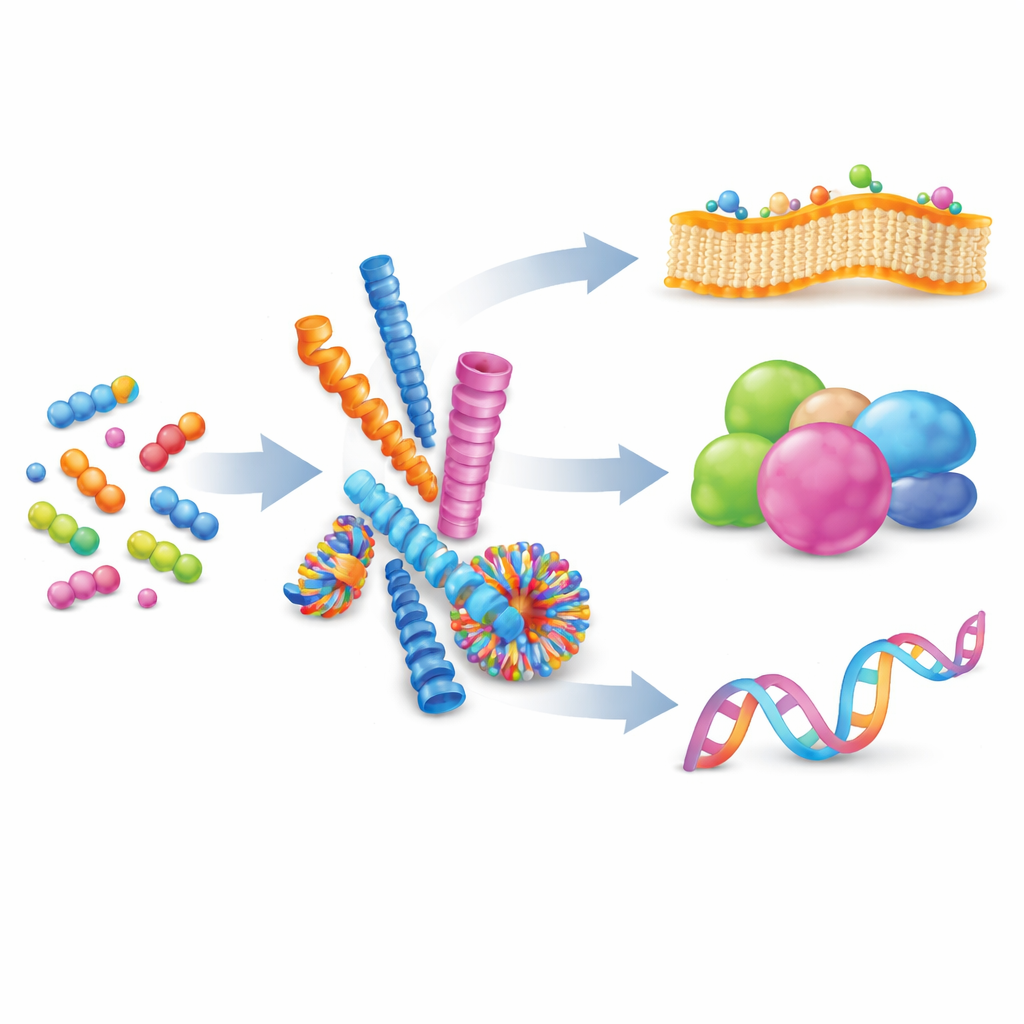
緩やかな分子から組織化されたナノ構造へ
著者らはまず超分子自己組織化を解説します。これは多くの小さな分子が弱い引力によって互いに惹き寄せられ、永久的な化学結合を形成せずにより大きな構造へと組織化される過程です。電荷、酸素や窒素による水素結合、平面環同士の積み重なりなどの力のバランスをとることで、化学者はペプチドをナノファイバー、球状体、チューブ、ベシクルへと導くことができます。これらの形は静的ではなく、その構成要素は出入りを繰り返し、集合体は可逆的で適応的になります。多くの弱い相互作用が共通の表面で同時に起きると“多価性”が生まれ、複数の小さなフックが同時に面をつかむように、もともと弱い結合を強化する強力な手段となります。
自然のプレイブックを借りる
自然は既に自己組織化に頼って複雑な機能を実現しています。タンパク質はアミノ酸の単純な鎖から三次元の精巧な立体構造へと折りたたまれ、他のタンパク質、DNA、あるいは膜と結合する広い接触面を露出します。これらの接触はしばしば大きな表面に広がっており、細胞がシグナルを迅速かつ可逆的にオン/オフできるようにします。この着想を得て、研究者はそのような界面を模倣する人工ペプチドを設計しています。高分子、脂質、DNAフレームワークと比べて、ペプチド系は生体適合性が高く、化学的多様性に富み、個々のアミノ酸レベルで精密に設計できるという利点があり、形状、電荷、結合挙動を精密に調整できます。本総説は、これらの人工ペプチド集合体が主に関与する三つの標的—細胞膜、タンパク質、核酸—に焦点を当てています。
膜から内側へ細胞の配線を変える
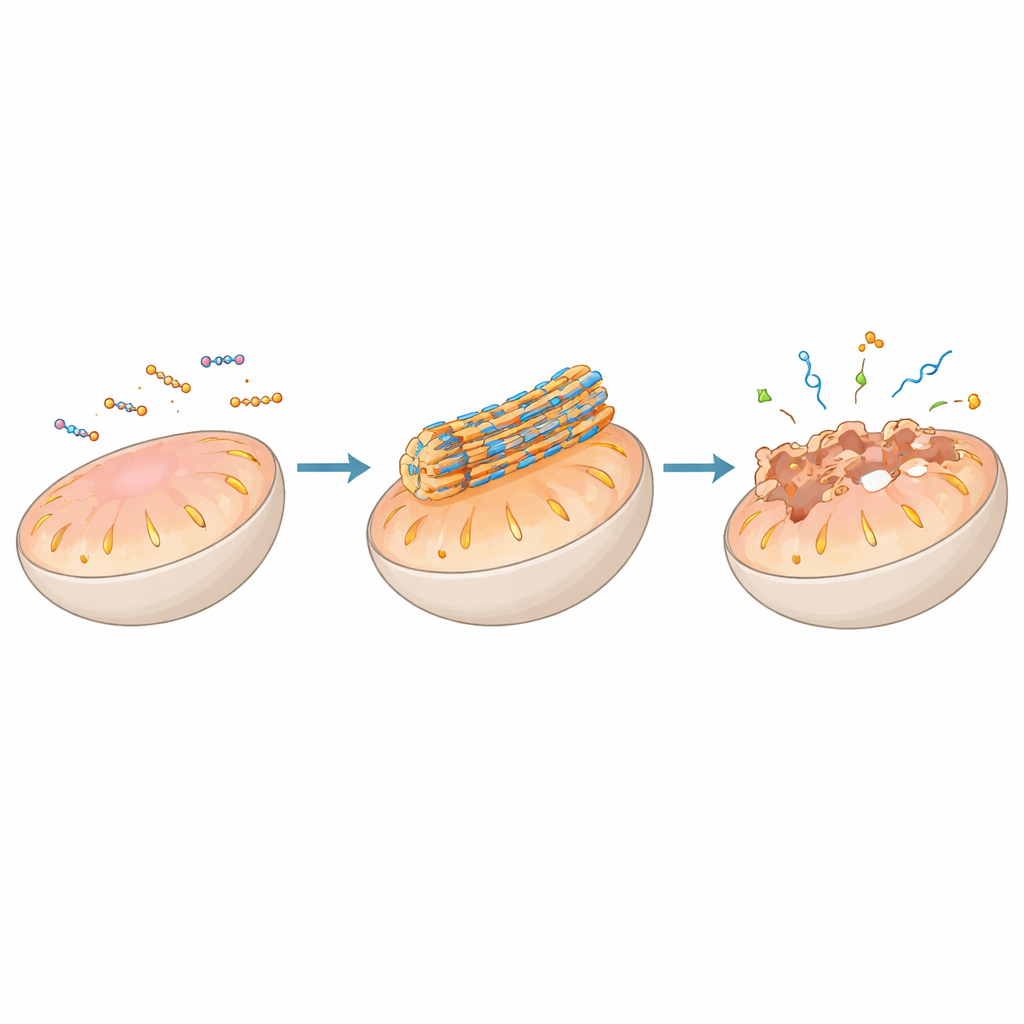
本稿の主要なテーマの一つは、ペプチド自己組織化を用いて細胞膜、特にミトコンドリア、リソソーム、小胞体、ゴルジ体といった重要なオルガネラの膜に直接作用することです。ペプチドは特定のオルガネラへ誘導する標的化モチーフで飾ることができ、局所条件—酸性度、電位、酵素活性など—がそれらを膜表面でナノファイバーや粒子へと組み立てさせます。例えばミトコンドリアでは、ある設計のペプチドは細胞内で分散している状態では無害ですが、オルガネラの負の電位によって濃縮されると硬いフィブリルに凝集します。これらのフィブリルは二重膜を穿孔または不安定化させ、電気化学的勾配を崩し、シトクロムcを放出してプログラムされた細胞死経路を活性化し、腫瘍細胞攻撃に有用です。
分解コンパートメントを制御ハブに変える
しばしば単なる細胞のリサイクルセンターと見なされるリソソームは、ここでは生死の判断を下すスイッチボードとして再解釈されます。リソソームの酸性pHや常在酵素を感知するよう設計されたペプチドは、細胞に取り込まれてこのコンパートメントへ輸送された後にのみ組み立てを始めます。一旦組み立てると、そのナノ構造はリソソーム膜を弱め、カテプシンなどの消化酵素を漏出させて細胞死を誘導します。別のペプチド系はリソソームから選択的段階で脱出するよう設計され、核酸などの治療ペイロードを細胞内部へ運ぶ手助けをします。同様の戦略を小胞体やゴルジ体に適用することで、“ストレス”応答を高めたりタンパク質仕分けのトラフィックを攪乱したりして、制御された形で細胞を自己破壊へと導くことが可能です。
ペプチド足場でタンパク質と遺伝子を導く
膜を越えて、ペプチド集合体はタンパク質や核酸に締め付けるように結合し、全体のシグナル伝達ネットワークを再構築できます。中には天然のタンパク質結合セグメントを極めて巧妙に模倣し、かつては創薬が困難と考えられたタンパク質–タンパク質インターフェースに楔を打ち込み、ミトコンドリア内の死の信号を解放したり、細胞表面の増殖シグナルを遮断したりするものがあります。ほかのものは抗体や受容体と共組み立てしてそれらをクラスター化し、リソソームでの除去へ標的化したり、がん細胞に対する免疫認識を高めたりします。DNAやRNAと組み合わせると、正に帯電したペプチドは遺伝物質を凝縮してコンパクトな粒子や液滴様の構造を作り、細胞に侵入して適切な時と場所で内容物を放出し、遺伝子サイレンシングや活性化を可能にします。場合によっては、ペプチド–RNAの液滴は人工的な“凝縮体”のように振る舞い、細胞が危機時に自然に形成するストレス顆粒を想起させます。
なぜこれらの微小な構築体が重要なのか
総説は、生体模倣ペプチドの自己組織化が分子レベルの精度で細胞挙動を変える柔軟なツールキットを提供すると結論付けています。これらのシステムは局所トリガーに応答し自らを再編成できるため、原理的には病んだ細胞を健康な細胞から区別し、エネルギーを作る工場を穿孔したりリサイクルセンターを攪乱したり、有害な遺伝子を沈黙させたり、免疫攻撃を再活性化したりと、必要な場所でのみ作用することが可能です。著者らは、イメージング、モデリング、設計手法が進歩するにつれて、これらの微小な構築体が研究室の好奇心から、細胞自身と同じ構造言語で語る新世代の適応型医薬へと進化し得ると論じています。
引用: Kim, D., Park, G., Seu, MS. et al. Biomimetic peptide self-assembly: interfacing with biomacromolecules to regulate cellular signaling. Exp Mol Med 58, 1038–1052 (2026). https://doi.org/10.1038/s12276-026-01691-6
キーワード: ペプチド自己組織化, 細胞シグナル伝達, ナノメディシン, オルガネラ標的療法, 超分子生体材料