Clear Sky Science · de
Biomimetische Peptid-Selbstorganisation: Schnittstelle zu Biomakromolekülen zur Regulierung zellulärer Signalübertragung
Kleine Strukturen bauen, um mit Zellen zu kommunizieren
Innerhalb jeder Zelle stoßen zahllose Moleküle zusammen, binden sich und lösen sich wieder — daraus entstehen die Signale, die uns am Leben erhalten. Diese Übersichtsarbeit untersucht, wie sehr kurze Proteinfragmente, sogenannte Peptide, so entworfen werden können, dass sie sich spontan zu winzigen Formen organisieren, die an Zellbestandteile andocken und diese Signale in nützliche Richtungen lenken. Indem sie die Strategien der Natur nachahmen, wollen Forscher intelligente Materialien entwickeln, die Krebszellen selektiv abtöten, fehlerhafte Signalwege korrigieren oder genetische Therapien mit deutlich höherer Präzision als heutige Wirkstoffe liefern.
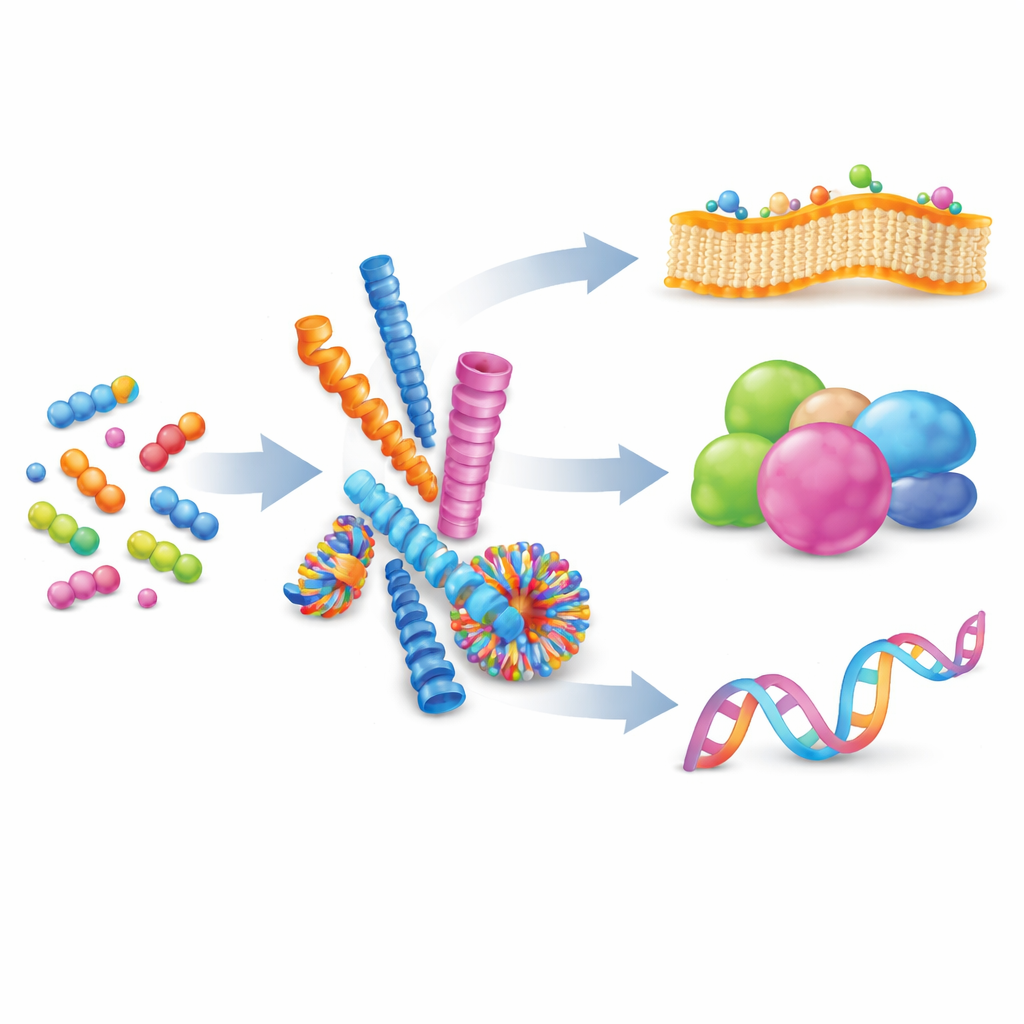
Von lockeren Molekülen zu organisierten Nanostrukturen
Die Autoren beginnen mit einer Erläuterung der supramolekularen Selbstorganisation: ein Prozess, bei dem viele kleine Moleküle sich schwach anziehen und sich ohne permanente chemische Bindungen zu größeren Strukturen ordnen. Durch das Austarieren von Kräften wie Ladung, Wasserstoffbrücken und Stapelungen zwischen flachen Ringen können Chemiker Peptide dazu bringen, Nanofasern, Kugeln, Röhren oder Vesikel zu bilden. Diese Formen sind nicht statisch; ihre Bausteine können sich ein- und auslagern, was die Assemblies reversibel und anpassungsfähig macht. Wenn viele schwache Wechselwirkungen auf einer gemeinsamen Oberfläche zusammenkommen, entsteht »Multivalenz«, ein kraftvolles Mittel, ansonsten schwache Bindungsereignisse zu verstärken — ähnlich wie mehrere winzige Haken, die gleichzeitig an einer Oberfläche greifen.
Aus dem Spielbuch der Natur schöpfen
Die Natur nutzt Selbstorganisation bereits zur Steuerung komplexer Aufgaben. Proteine falten sich aus einfachen Aminosäureketten in komplexe dreidimensionale Formen und präsentieren breite Kontaktflächen, die an andere Proteine, DNA oder Membranen binden. Diese Kontakte, oft über große Flächen verteilt, erlauben es Zellen, Signalübertragung schnell und reversibel ein- und auszuschalten. Davon inspiriert entwerfen Forscher nun künstliche Peptide, die solche Schnittstellen nachahmen. Im Vergleich zu Polymeren, Lipiden oder DNA-Rahmen bieten Peptidsysteme einen guten Kompromiss: sie sind biokompatibel, chemisch vielfältig und auf Ebene einzelner Aminosäuren präzise, sodass Form, Ladung und Bindungsverhalten fein abgestimmt werden können. Diese Übersicht konzentriert sich darauf, wie diese künstlichen Peptid‑Assemblies drei Hauptziele ansprechen: Zellmembranen, Proteine und Nukleinsäuren.
Die Zelle von der Membran aus neu verdrahten
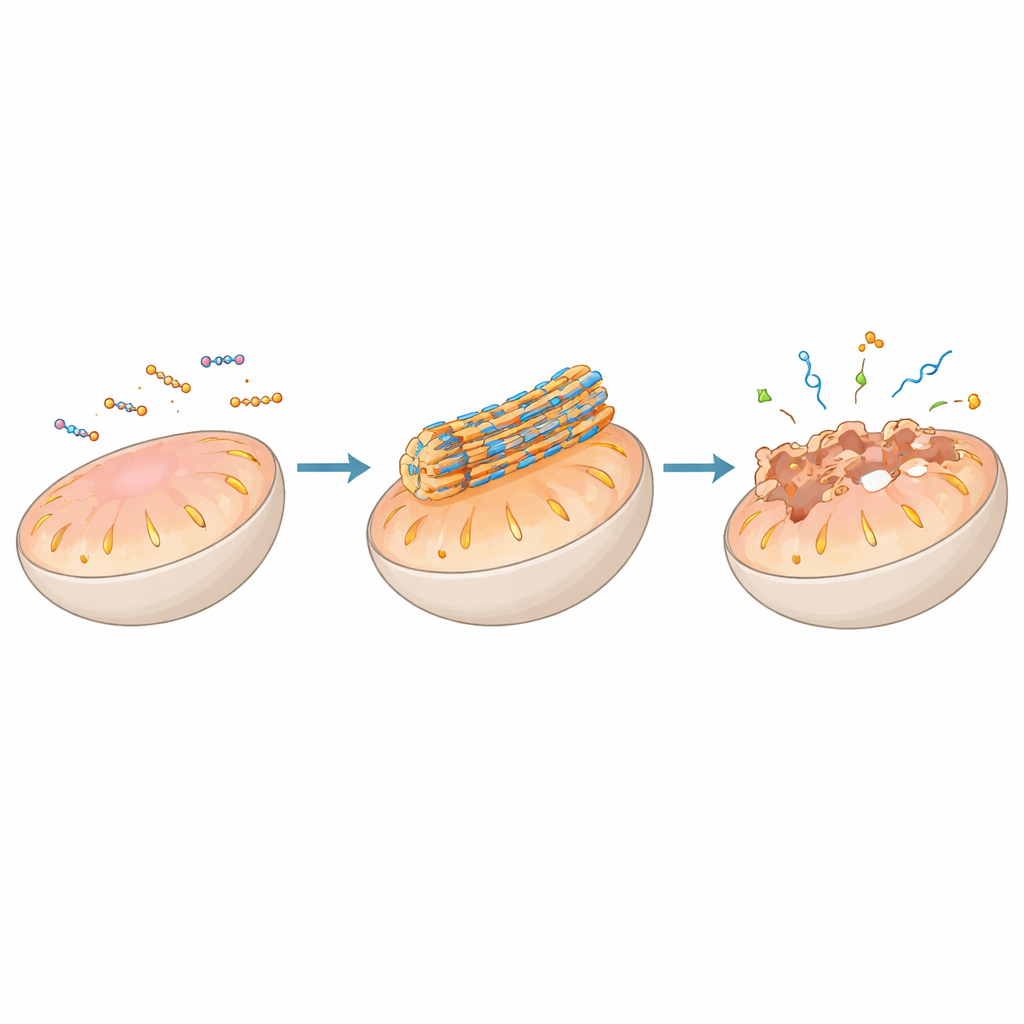
Ein zentrales Thema des Artikels ist die direkte Wirkung von Peptid‑Selbstorganisation auf Zellmembranen, insbesondere die von Schlüsselorganellen wie Mitochondrien, Lysosomen, dem endoplasmatischen Retikulum und dem Golgi‑Apparat. Peptide können mit Zielgruppen versehen werden, die sie zu einem bestimmten Organell lenken, wo lokale Bedingungen — etwa Säuregrad, elektrische Potentiale oder Enzymaktivität — ihr Assemblieren zu Nanofasern oder Partikeln an der Membran auslösen. In Mitochondrien bleiben bestimmte Entwürfe beispielsweise harmlos, solange sie im Zellinneren verteilt sind, aggregieren aber zu steifen Fasern, sobald die negative Spannung des Organells sie konzentriert. Diese Fasern können die Doppelmembran durchstechen oder destabilisieren, den Energiegradienten zusammenbrechen lassen, Cytochrom c freisetzen und programmierte Zelltodwege aktivieren — ein nützlicher Mechanismus zur Bekämpfung von Tumorzellen.
Abbaukompartimente zu Kontrollzentren umfunktionieren
Lysosomen, oft schlicht als zelluläre Recyclingzentren betrachtet, werden hier als Schaltstellen für Entscheidungen über Leben und Tod neu gedacht. Peptide, die so konstruiert sind, dass sie den sauren pH‑Wert oder die dort ansässigen Enzyme der Lysosomen erkennen, können erst nach Aufnahme in die Zelle und Transport in dieses Kompartiment assemblieren. Nach der Assemblierung können ihre Nanostrukturen die lysosomale Membran schwächen, sodass Verdauungsenzyme wie Cathepsine auslaufen und Zelltod auslösen. Andere Peptidsysteme sind so ausgelegt, dass sie in wohlüberlegten Stadien aus Lysosomen entkommen und therapeutische Fracht wie Nukleinsäuren in das Zellinnere transportieren. Ähnliche Strategien, angewandt auf endoplasmatisches Retikulum und Golgi, erlauben es Forschern, Stressantworten zu verstärken oder Protein‑Sortierprozesse zu stören und so Zellen kontrolliert in Richtung Selbstzerstörung zu lenken.
Proteine und Gene mit Peptidgerüsten lenken
Über Membranen hinaus können Peptid‑Assemblies an Proteine oder Nukleinsäuren klammern und ganze Signalnetzwerke umgestalten. Manche Assemblies ahmen natürliche Proteinbindungssegmente so gut nach, dass sie in Protein–Protein‑Schnittstellen eindringen, die früher als undruggable galten, und so pro‑Tod‑Signale in Mitochondrien freisetzen oder Wachstumssignale an Zelloberflächen blockieren. Andere koassemblieren mit Antikörpern oder Rezeptoren, um diese zu klustern, zum Abbau in Lysosomen zu markieren oder die Immunerkennung von Tumorzellen zu verstärken. In Kombination mit DNA oder RNA kondensieren positiv geladene Peptide genetisches Material zu kompakten Partikeln oder flüssigkeitsähnlichen Tropfen, die in Zellen eindringen und ihre Fracht zur richtigen Zeit und am richtigen Ort freisetzen können — was Genstilllegung oder -aktivierung ermöglicht. In bestimmten Fällen verhalten sich Peptid–RNA‑Tropfen wie künstliche »Kondensate« und erinnern an Stressgranula, die Zellen natürlicherweise zur RNA‑Verwaltung in Krisenzeiten bilden.
Warum diese kleinen Baumeister zählen
Die Übersichtsarbeit kommt zu dem Schluss, dass biomimetische Peptid‑Selbstorganisation ein flexibles Instrumentarium bietet, um zelluläres Verhalten mit molekularer Präzision umzugestalten. Da diese Systeme auf lokale Auslöser reagieren und sich selbst reorganisieren können, sind sie prinzipiell in der Lage, kranke Zellen von gesunden zu unterscheiden und nur dort aktiv zu werden, wo es nötig ist — etwa indem sie Löcher in Energieproduktionsstätten reißen, Recyclingzentren stören, schädliche Gene stilllegen oder Immunangriffe wieder entfachen. Die Autoren argumentieren, dass diese kleinen Baumeister mit besseren Bildgebungs-, Modellierungs- und Designmethoden von Laborneugkeiten zu einer neuen Generation adaptiver Medikamente heranreifen könnten, die dieselbe strukturelle Sprache wie die Zelle selbst sprechen.
Zitation: Kim, D., Park, G., Seu, MS. et al. Biomimetic peptide self-assembly: interfacing with biomacromolecules to regulate cellular signaling. Exp Mol Med 58, 1038–1052 (2026). https://doi.org/10.1038/s12276-026-01691-6
Schlüsselwörter: Peptid-Selbstorganisation, Zelluläre Signalübertragung, Nanomedizin, Organellen‑gezielte Therapie, supramolekulare Biomaterialien