Clear Sky Science · it
Auto-assemblaggio di peptidi biomimetici: interfacciarsi con biomacromolecole per regolare la segnalazione cellulare
Costruire piccole strutture per comunicare con le cellule
All'interno di ogni cellula, innumerevoli molecole si scontrano, si legano e si separano, generando i segnali che ci mantengono in vita. Questa recensione esplora come pezzi molto corti di proteine, chiamati peptidi, possano essere progettati per organizzarsi spontaneamente in forme minute che si agganciano ai componenti cellulari e indirizzano quei segnali in direzioni utili. Imparando a imitare le strategie della natura, gli scienziati sperano di costruire materiali intelligenti in grado di uccidere selettivamente le cellule tumorali, correggere segnali difettosi o veicolare terapie genetiche con una precisione molto maggiore rispetto ai farmaci odierni.
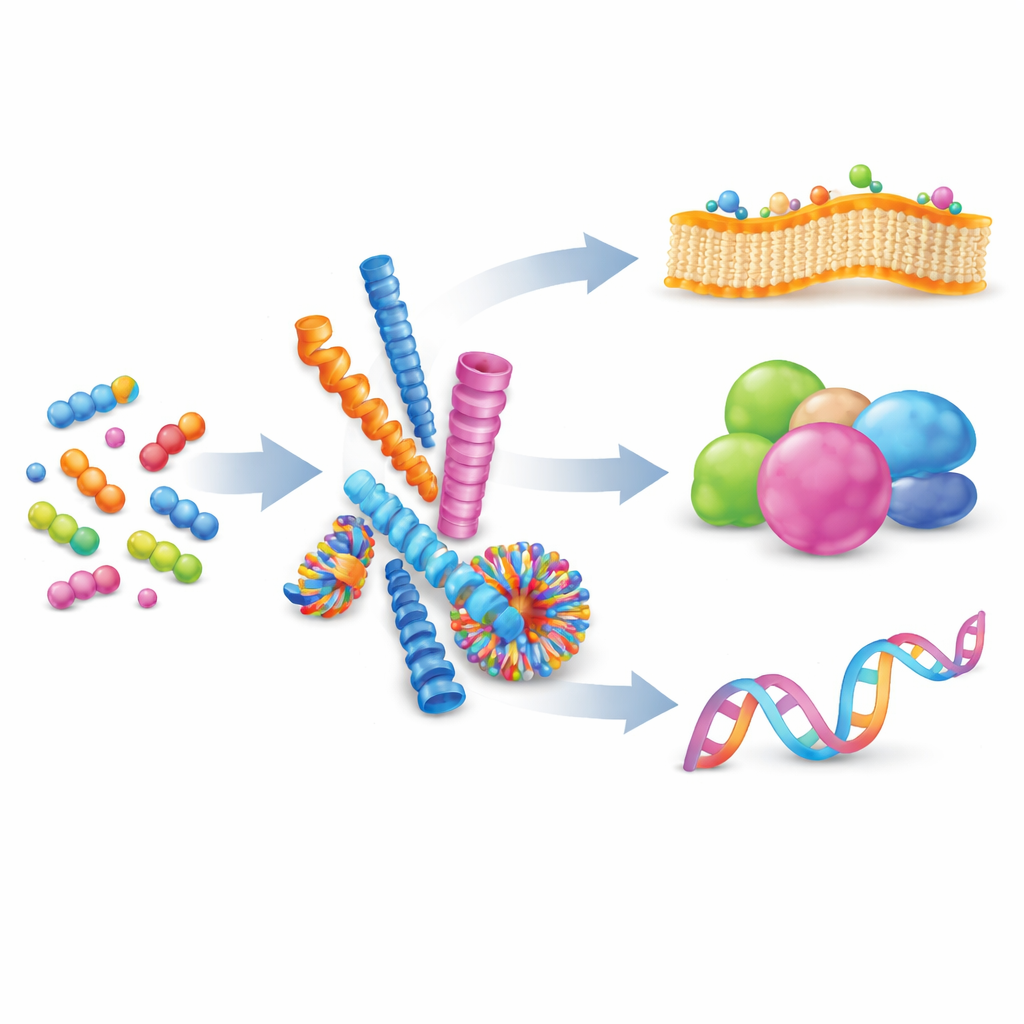
Da molecole disperse a nanostrutture organizzate
Gli autori iniziano spiegando l'auto-assemblaggio supramolecolare: un processo in cui molte piccole molecole si attraggono dolcemente e si organizzano in strutture più grandi senza formare legami chimici permanenti. Bilanciando forze come carica, legami a idrogeno e impilamento tra anelli planari, i chimici possono indurre i peptidi a formare nanofibre, sfere, tubi o vescicole. Queste forme non sono statiche; i loro mattoni costitutivi possono scambiarsi dentro e fuori, rendendo gli assemblaggi reversibili e adattabili. Quando molte interazioni deboli avvengono insieme su una superficie condivisa, creano una “multivalenza”, un modo potente per rafforzare eventi di legame altrimenti fragili, proprio come più piccoli ganci che afferrano contemporaneamente una superficie.
Pescare dal repertorio della natura
La natura si affida già all'auto-assemblaggio per svolgere compiti complessi. Le proteine si piegano da semplici catene di amminoacidi in forme tridimensionali intricate, esponendo ampie aree di contatto che si legano ad altre proteine, al DNA o alle membrane. Questi contatti, spesso estesi su grandi superfici, permettono alle cellule di accendere e spegnere la segnalazione in modo rapido e reversibile. Ispirati a ciò, i ricercatori progettano ora peptidi artificiali che imitano tali interfacce. Rispetto a polimeri, lipidi o matrici di DNA, i sistemi peptidici offrono un equilibrio vantaggioso: sono biocompatibili, chimicamente diversificabili e precisi a livello del singolo amminoacido, permettendo una messa a punto accurata di forma, carica e comportamento di legame. Questa recensione si concentra su come questi assemblaggi peptidici di sintesi vengano utilizzati per interagire con tre bersagli principali: membrane cellulari, proteine e acidi nucleici.
Riprogrammare la cellula partendo dalla membrana
Un tema centrale dell'articolo è l'uso dell'auto-assemblaggio peptidico per agire direttamente sulle membrane cellulari, in particolare su quelle di organelli chiave come mitocondri, lisosomi, reticolo endoplasmatico e apparato del Golgi. I peptidi possono essere decorati con gruppi di targeting che li guidano verso un organello specifico, dove condizioni locali — come acidità, potenziale elettrico o attività enzimatica — li inducono ad assemblarsi in nanofibre o particelle sulla superficie della membrana. Nei mitocondri, per esempio, alcuni progetti rimangono innocui quando dispersi nella cellula ma si aggregano in fibre rigide una volta concentrati dal potenziale negativo dell'organello. Queste fibre possono forare o destabilizzare la doppia membrana, facendo crollare il gradiente energetico, rilasciando citocromo c e attivando vie di morte cellulare programmata utili per attaccare le cellule tumorali.
Trasformare compartimenti degradativi in centri di controllo
I lisosomi, spesso pensati semplicemente come centri di riciclo cellulare, vengono qui reinterpretati come quadri di comando per decisioni di vita o morte. Peptidi ingegnerizzati per rilevare il pH acido del lisosoma o enzimi residenti possono assemblarsi solo dopo essere stati ingeriti dalla cellula e instradati in questo compartimento. Una volta assemblate, le loro nanostrutture possono indebolire la membrana lisosomiale, permettendo agli enzimi digestivi come le catepsine di fuoriuscire e innescare la morte cellulare. Altri sistemi peptidici sono progettati per sfuggire dai lisosomi in stadi accuratamente scelti, aiutando a trasportare carichi terapeutici come acidi nucleici nell'interno della cellula. Strategie simili applicate a reticolo endoplasmatico e apparato del Golgi consentono ai ricercatori di aumentare le risposte di “stress” o disturbare il traffico di smistamento delle proteine, indirizzando ancora una volta le cellule verso l'autodistruzione in modo controllato.
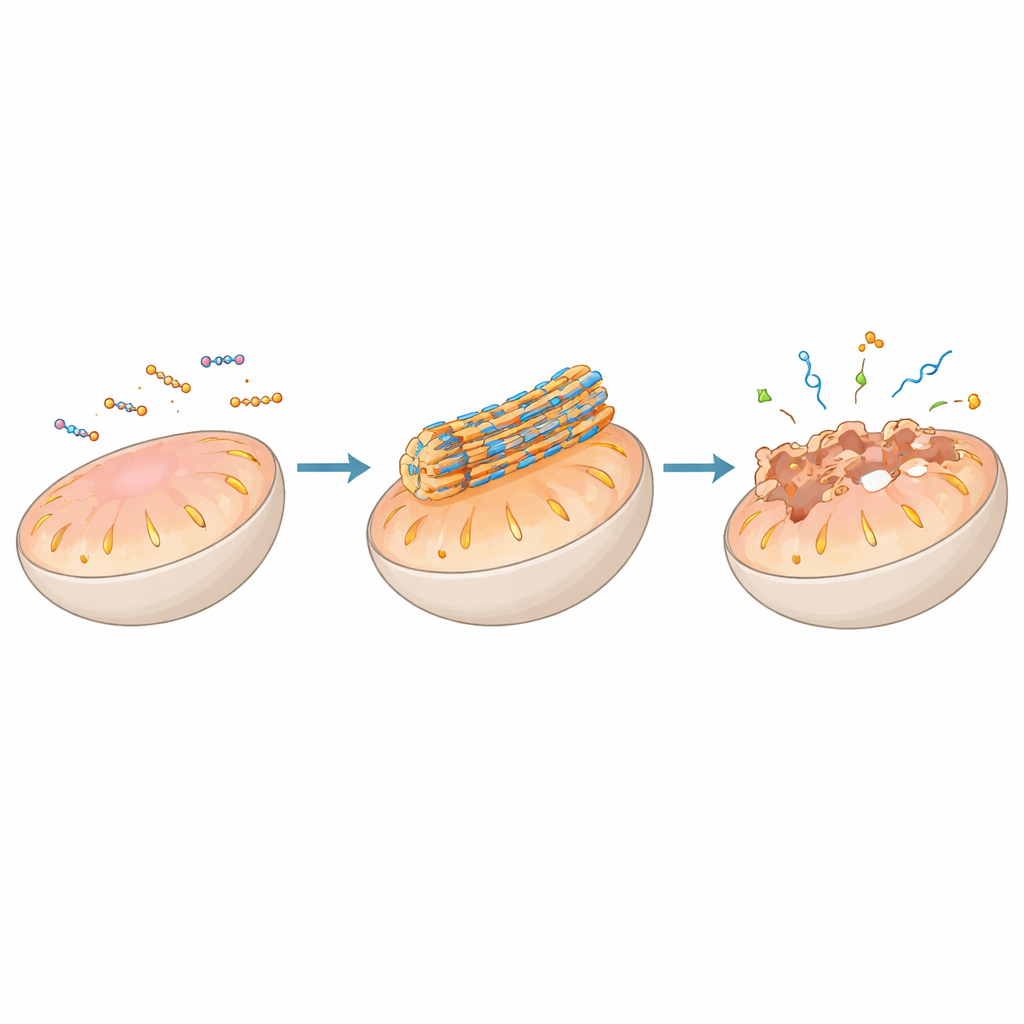
Guidare proteine e geni con impalcature peptidiche
Oltre alle membrane, gli assemblaggi peptidici possono aggrapparsi a proteine o acidi nucleici e rimodellare intere reti di segnalazione. Alcuni assemblaggi imitano così bene segmenti naturali leganti le proteine che si insinuano in interfacce proteina–proteina un tempo considerate impossibili da colpire con farmaci, liberando segnali pro-morte nei mitocondri o bloccando segnali di crescita sulla superficie cellulare. Altri co-assemblano con anticorpi o recettori per raggrupparli, segnalarli per la rimozione nei lisosomi o potenziare il riconoscimento immunitario delle cellule tumorali. Quando combinati con DNA o RNA, peptidi carichi positivamente condensano il materiale genetico in particelle compatte o in goccioline di tipo liquido che penetrano nelle cellule e rilasciano il carico al momento e nel luogo opportuni, permettendo il silenziamento o l'attivazione genica. In alcuni casi, le goccioline peptide–RNA si comportano come “condensati” artificiali, richiamando i grani di stress che le cellule formano naturalmente per gestire l'RNA durante le crisi.
Perché questi piccoli costruttori sono importanti
La recensione conclude che l'auto-assemblaggio biomimetico di peptidi offre una cassetta degli attrezzi flessibile per rimodellare il comportamento cellulare con precisione a livello molecolare. Poiché questi sistemi rispondono a trigger locali e possono riorganizzarsi, in principio possono distinguere le cellule malate da quelle sane e agire solo dove necessario — perforando le fabbriche di energia, disturbando i centri di riciclo, silenziando geni dannosi o riaccendendo l'attacco immunitario. Gli autori sostengono che, man mano che migliorano metodi di imaging, modellizzazione e progettazione, questi piccoli costruttori potrebbero evolvere da curiosità di laboratorio a una nuova generazione di medicine adattive che parlano lo stesso linguaggio strutturale della cellula stessa.
Citazione: Kim, D., Park, G., Seu, MS. et al. Biomimetic peptide self-assembly: interfacing with biomacromolecules to regulate cellular signaling. Exp Mol Med 58, 1038–1052 (2026). https://doi.org/10.1038/s12276-026-01691-6
Parole chiave: auto-assemblaggio di peptidi, segnalazione cellulare, nanomedicina, terapia mirata agli organelli, biomateriali supramolecolari