Clear Sky Science · es
Autosíntesis de péptidos biomiméticos: interacción con biomacromoléculas para regular la señalización celular
Construir estructuras minúsculas para comunicarse con las células
Dentro de cada célula, innumerables moléculas se encuentran, se unen y se disocian, generando las señales que nos mantienen con vida. Esta revisión explora cómo fragmentos muy cortos de proteínas, llamados péptidos, pueden diseñarse para organizarse espontáneamente en formas diminutas que se adhieren a componentes celulares y modulan esas señales en direcciones útiles. Al aprender a imitar las propias estrategias de la naturaleza, los científicos esperan construir materiales inteligentes que puedan destruir selectivamente células cancerosas, corregir señalización defectuosa o entregar terapias génicas con mucha más precisión que los fármacos actuales.
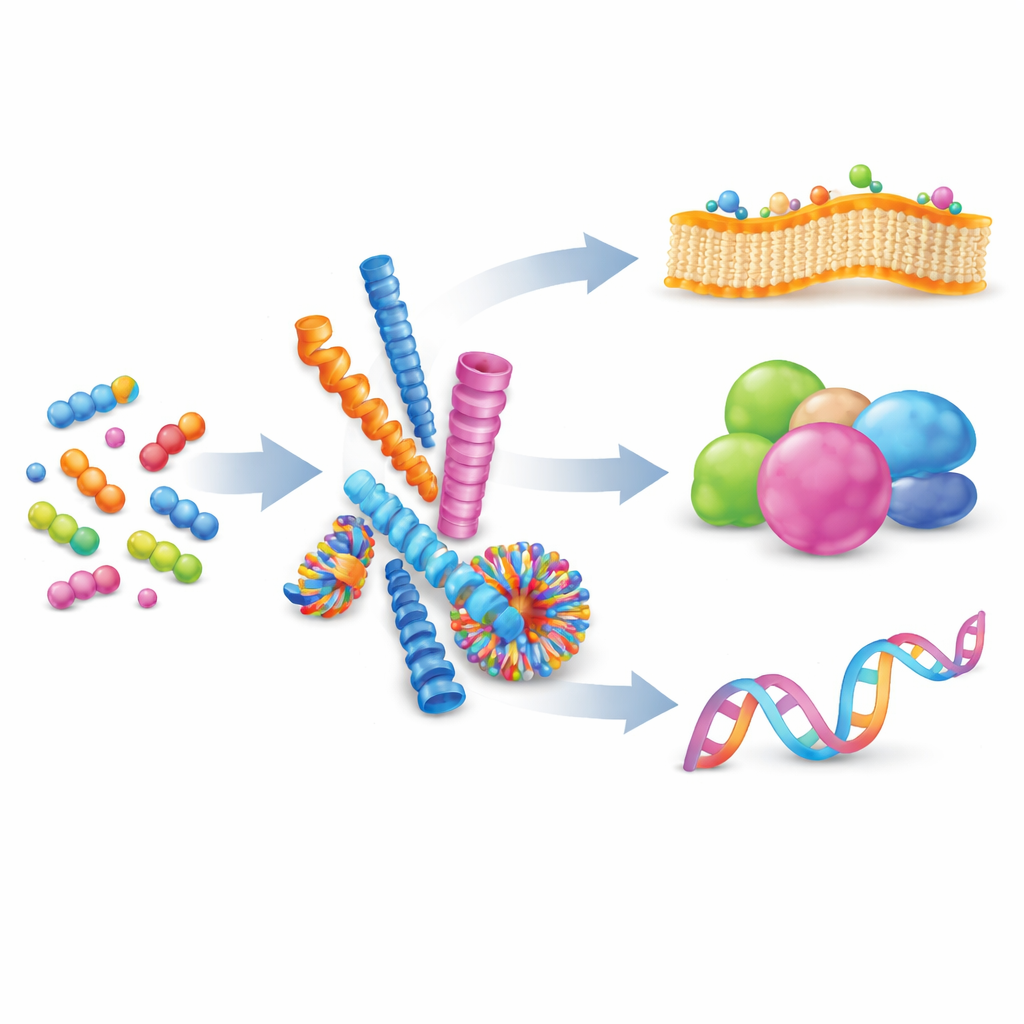
De moléculas sueltas a nanoestructuras organizadas
Los autores comienzan explicando la autosíntesis supramolecular: un proceso en el que muchas moléculas pequeñas se atraen suavemente entre sí y se organizan en estructuras mayores sin formar enlaces químicos permanentes. Al equilibrar fuerzas como la carga, los puentes de hidrógeno y el apilamiento entre anillos planos, los químicos pueden inducir a los péptidos a formar nanofibras, esferas, tubos o vesículas. Estas formas no son estáticas; sus bloques constructores pueden intercambiarse, haciendo que los ensamblajes sean reversibles y adaptables. Cuando muchas interacciones débiles ocurren juntas sobre una superficie compartida, crean “multivalencia”, una manera poderosa de reforzar interacciones de unión por lo demás frágiles, como si múltiples ganchos diminutos agarraran una superficie al mismo tiempo.
Tomando prestado el manual de la naturaleza
La naturaleza ya depende de la autosíntesis para llevar a cabo tareas complejas. Las proteínas se pliegan desde cadenas simples de aminoácidos en formas tridimensionales intrincadas, exponiendo amplias áreas de contacto que se unen a otras proteínas, ADN o membranas. Estos contactos, a menudo extendidos por grandes superficies, permiten a las células activar y desactivar la señalización de manera rápida y reversible. Inspirados en esto, los investigadores diseñan ahora péptidos artificiales que imitan tales interfaces. En comparación con polímeros, lípidos o andamios de ADN, los sistemas peptídicos ofrecen un punto intermedio ventajoso: son biocompatibles, químicamente diversos y precisos a nivel del aminoácido individual, lo que permite un ajuste fino de la forma, la carga y el comportamiento de unión. Esta revisión se centra en cómo estos ensamblajes peptídicos sintéticos se usan para dirigirse a tres objetivos principales: membranas celulares, proteínas y ácidos nucleicos.
Reconectar la célula desde la membrana hacia dentro
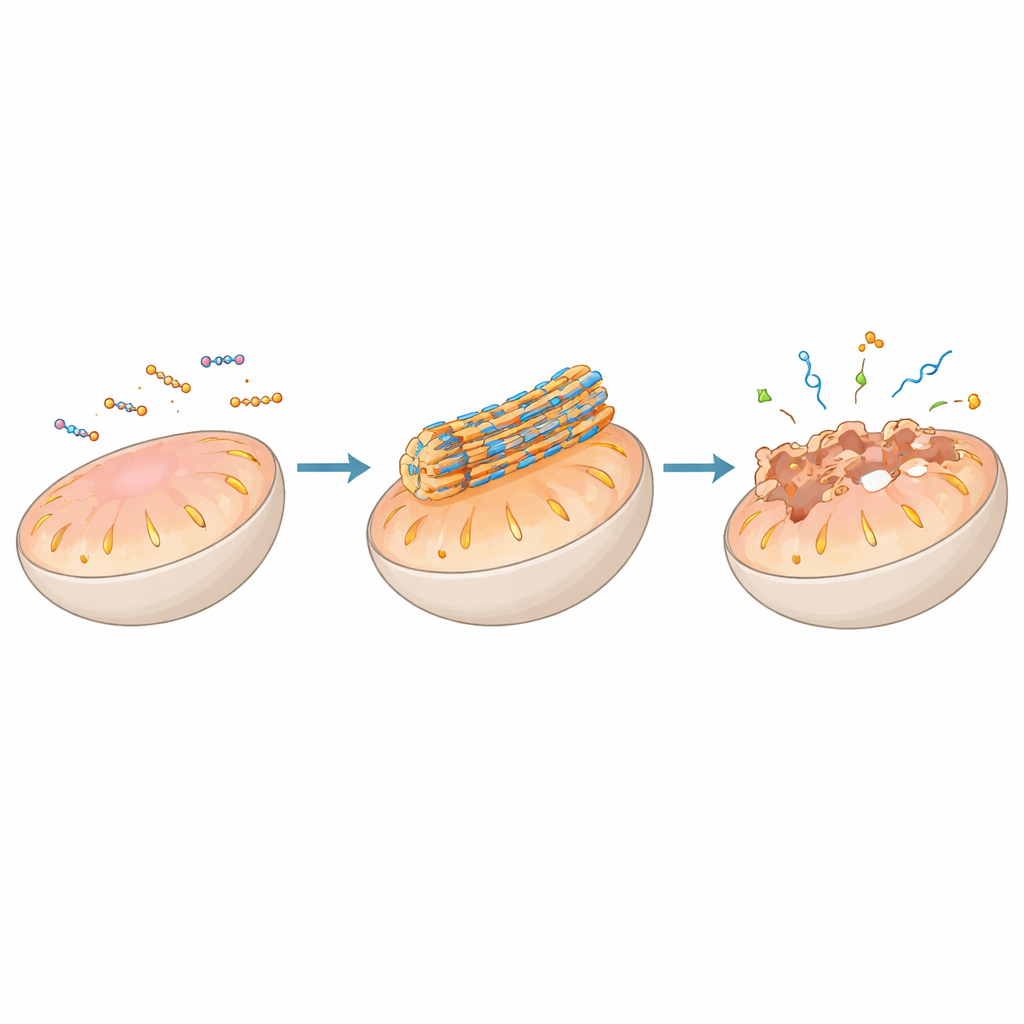
Un tema principal del artículo es el uso de la autosíntesis de péptidos para actuar directamente sobre las membranas celulares, en particular las de orgánulos clave como las mitocondrias, lisosomas, retículo endoplásmico y aparato de Golgi. Los péptidos pueden decorarse con grupos de direccionamiento que los guían a un orgánulo específico, donde las condiciones locales —como acidez, potencial eléctrico o actividad enzimática— desencadenan su ensamblaje en nanofibras o partículas sobre la superficie de la membrana. En las mitocondrias, por ejemplo, ciertos diseños permanecen inofensivos mientras están dispersos en la célula, pero se agregan en fibras rígidas una vez concentrados por el voltaje negativo del orgánulo. Estas fibras pueden perforar o desestabilizar la membrana doble, colapsando el gradiente energético, liberando citocromo c y activando vías de muerte celular programada que son útiles para atacar células tumorales.
Convertir compartimentos degradativos en centros de control
Los lisosomas, a menudo considerados simplemente centros de reciclaje celular, se presentan aquí como paneles de control para decisiones de vida o muerte. Péptidos diseñados para detectar el pH ácido lisosomal o enzimas residentes pueden ensamblarse solo después de ser internalizados por la célula y traficados a este compartimento. Una vez ensambladas, sus nanoestructuras pueden debilitar la membrana lisosomal, permitiendo que enzimas digestivas como las catepsinas se filtren y desencadenen la muerte celular. Otros sistemas peptídicos están concebidos para escapar de los lisosomas en etapas cuidadosamente elegidas, ayudando a transportar cargas terapéuticas como ácidos nucleicos al interior de la célula. Estrategias similares aplicadas al retículo endoplásmico y al aparato de Golgi permiten a los investigadores aumentar las respuestas de “estrés” o perturbar el tráfico de clasificación de proteínas, orientando de nuevo a las células hacia la autodestrucción de forma controlada.
Guiar proteínas y genes con andamios peptídicos
Más allá de las membranas, los ensamblajes peptídicos pueden sujetar proteínas o ácidos nucleicos y remodelar redes de señalización enteras. Algunos ensamblajes imitan segmentos naturales de unión a proteínas tan bien que se insertan en interfaces proteína–proteína antes consideradas intratables por fármacos, liberando señales pro‑muerte en mitocondrias o bloqueando señales de crecimiento en la superficie celular. Otros se coensamblan con anticuerpos o receptores para agruparlos, marcarlos para su eliminación en lisosomas o potenciar el reconocimiento inmune de células cancerosas. Cuando se combinan con ADN o ARN, péptidos cargados positivamente condensan material genético en partículas compactas o en gotas de aspecto líquido que penetran en las células y liberan su carga en el momento y lugar adecuados, posibilitando el silenciamiento o la activación génica. En ciertos casos, las gotas péptido–ARN se comportan como “condensados” artificiales, emulando los gránulos de estrés que las células forman naturalmente para gestionar ARN durante crisis.
Por qué importan estos diminutos constructores
La revisión concluye que la autosíntesis peptídica biomimética ofrece una caja de herramientas flexible para remodelar el comportamiento celular con precisión a escala molecular. Dado que estos sistemas responden a desencadenantes locales y pueden reorganizarse, en principio pueden distinguir células enfermas de las sanas y actuar solo donde se necesite: perforando fábricas de energía, perturbando centros de reciclaje, silencian genes dañinos o reavivando ataques inmunitarios. Los autores sostienen que, a medida que mejoren los métodos de imagen, modelado y diseño, estos diminutos constructores podrían evolucionar de curiosidades de laboratorio a una nueva generación de medicinas adaptivas que hablen el mismo lenguaje estructural que la propia célula.
Cita: Kim, D., Park, G., Seu, MS. et al. Biomimetic peptide self-assembly: interfacing with biomacromolecules to regulate cellular signaling. Exp Mol Med 58, 1038–1052 (2026). https://doi.org/10.1038/s12276-026-01691-6
Palabras clave: autosíntesis de péptidos, señalización celular, nanomedicina, terapia dirigida a orgánulos, biomateriales supramoleculares