Clear Sky Science · sv
Biomimetisk peptid-självmontering: gränssnitt med biomakromolekyler för att reglera cellulär signalering
Bygga pyttesmå strukturer för att kommunicera med celler
Inuti varje cell stötar, binder och bryts otaliga molekyler upp och skapar de signaler som håller oss vid liv. Denna översikt undersöker hur mycket korta proteinbitar, kallade peptider, kan utformas för att spontant organisera sig till små former som hakar fast vid cellulära komponenter och påverkar dessa signaler i användbara riktningar. Genom att lära sig efterlikna naturens egna strategier hoppas forskare kunna bygga smarta material som selektivt kan döda cancerceller, korrigera felaktig signalering eller leverera genetiska terapier med mycket större precision än dagens läkemedel.
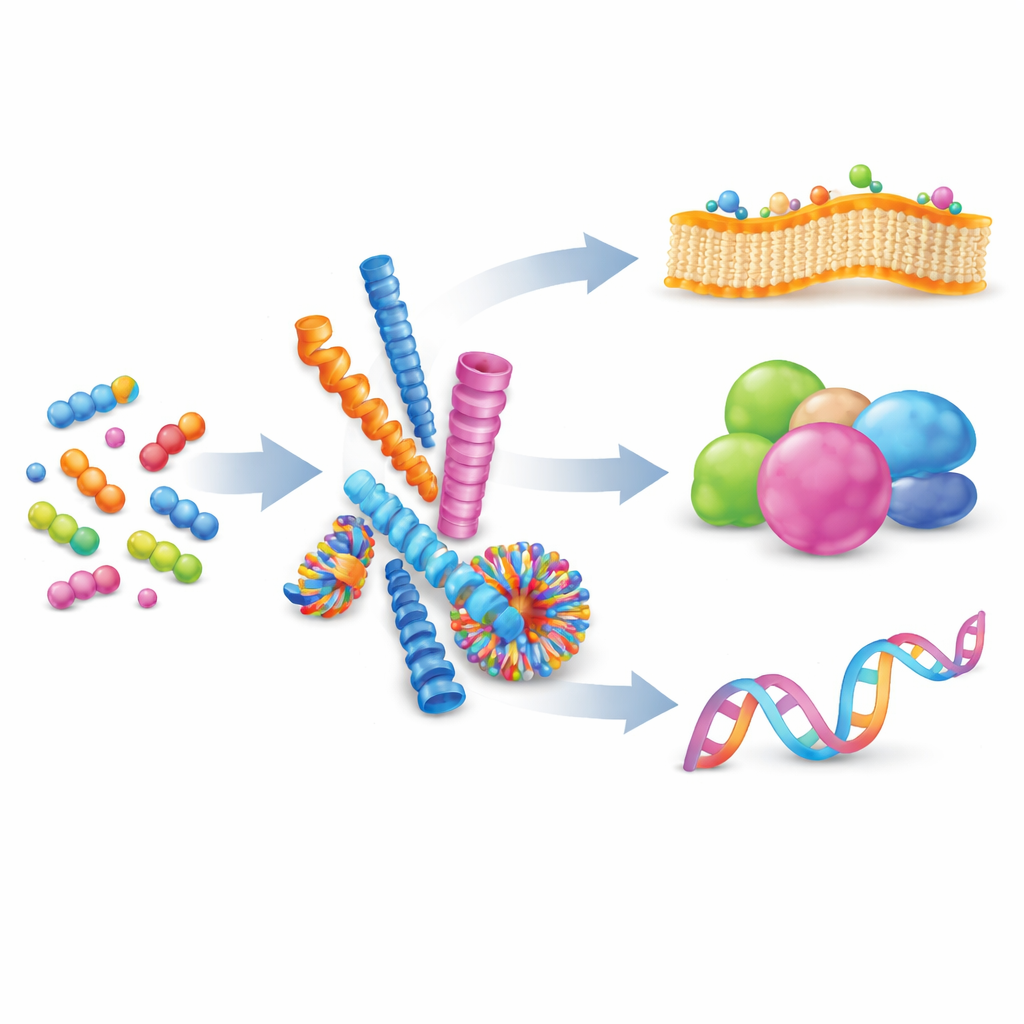
Från lösa molekyler till organiserade nanostrukturer
Författarna inleder med att förklara supramolekylär självmontering: en process där många små molekyler milt attraherar varandra och organiserar sig till större strukturer utan att bilda permanenta kemiska bindningar. Genom att balansera krafter som laddning, vätebindningar och stapling mellan plana ringar kan kemister få peptider att bilda nanofibrer, sfärer, rör eller vesiklar. Dessa former är inte statiska; deras byggstenar kan bytas in och ut, vilket gör konstruktionerna reversibla och anpassningsbara. När många svaga interaktioner uppträder tillsammans på en gemensam yta skapar de »multivalens», ett kraftfullt sätt att förstärka annars svaga bindningsevenemang, ungefär som flera små krokar som griper en yta samtidigt.
Låna naturens spelbok
Naturen använder redan självmontering för att driva komplexa uppgifter. Proteiner viks från enkla kedjor av aminosyror till intrikata tredimensionella former och exponerar stora kontaktytor som binder andra proteiner, DNA eller membraner. Dessa kontakter, ofta spridda över stora ytor, tillåter celler att snabbt och reversibelt slå av och på signalering. Inspirerade av detta designar forskare nu artificiella peptider som imiterar sådana gränssnitt. Jämfört med polymerer, lipider eller DNA-ramverk erbjuder peptidsystem en gynnsam balans: de är biokompatibla, kemiskt mångsidiga och precisa på nivån av enskilda aminosyror, vilket möjliggör noggrann justering av form, laddning och bindningsbeteende. Denna översikt fokuserar på hur dessa människotillverkade peptidaggregationer används för att rikta in sig mot tre huvudmål: cellmembran, proteiner och nukleinsyror.
Omkoppling av cellen från membranet inåt
Ett stort tema i artikeln är att använda peptid-självmontering för att verka direkt på cellulära membran, särskilt hos nyckelorganeller som mitokondrier, lysosomer, det endoplasmatiska retikulumet och Golgiapparaten. Peptider kan förses med målinriktande grupper som leder dem till en specifik organell, där lokala förhållanden — såsom surhetsgrad, elektrisk potential eller enzymaktivitet — utlöser att de monteras till nanofibrer eller partiklar på membranets yta. I mitokondrier, till exempel, förblir vissa konstruktioner ofarliga medan de är dispergerade i cellen men aggregerar till styva fibrer när de koncentreras av organellens negativa spänning. Dessa fibrer kan punktera eller destabilisera dubbla membran, kollapsa energigradienten, frisätta cytokrom c och aktivera programmerade dödsvägar som är värdefulla för att angripa tumörceller.
Göra nedbrytande kompartment till kontrollnav
Lysosomer, ofta betraktade som enkla cellulära återvinningscentraler, omformas här till växelbord för liv‑och‑död‑beslut. Peptider designade för att känna av lysosomens sura pH eller dess enzymer kan montera sig först efter att de blivit intagna av cellen och förflyttade till detta kompartment. När de väl monterats kan deras nanostrukturer försvaga lysosommembranet, vilket tillåter matsmältningsenzymer som katepsiner att läcka ut och utlösa celldöd. Andra peptidsystem är utformade för att fly från lysosomer vid noggrant valda stadier och hjälper till att föra terapeutiska laster som nukleinsyror in i cellens inre. Liknande strategier tillämpade på det endoplasmatiska retikulumet och Golgiapparaten låter forskare öka »stress»-svar eller störa protein-sorteringsflöden, igen med målet att styra celler mot självdestruktion på ett kontrollerat sätt.
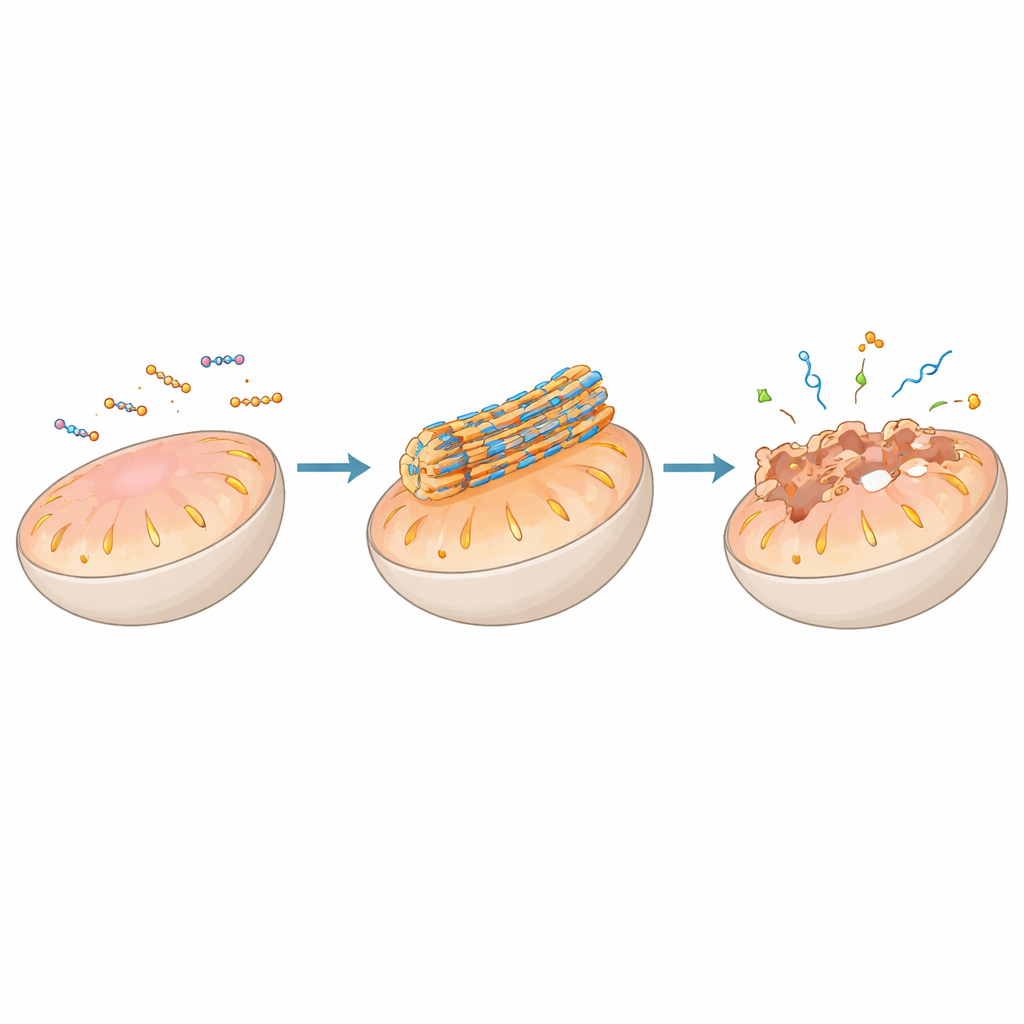
Vägleda proteiner och gener med peptid-stommar
Bortom membran kan peptidaggregationer klämma fast proteiner eller nukleinsyror och omforma hela signalnätverk. Vissa aggregationer imiterar naturliga proteinbindande segment så väl att de tränger in i protein–protein-gränssnitt som tidigare ansågs ogenomträngliga för läkemedel, frigörande pro‑dödsignaler i mitokondrier eller blockering av tillväxtsignaler på cellens yta. Andra sammonterar med antikroppar eller receptorer för att klustra dem, märka dem för nedbrytning i lysosomer eller öka immunsystemets igenkänning av cancerceller. När de kombineras med DNA eller RNA kondenserar positivt laddade peptider genetiskt material till kompakta partiklar eller vätske‑lika droppar som glider in i celler och släpper sitt gods på rätt tid och plats, vilket möjliggör gen‑tystnad eller aktivering. I vissa fall beter sig peptid–RNA‑droppar som artificiella »kondensat», vilket ekar stressgranulor som celler naturligt bildar för att hantera RNA under kriser.
Varför dessa pyttesmå byggare är viktiga
Översikten avslutar med att konstatera att biomimetisk peptid‑självmontering erbjuder en flexibel verktygslåda för att omforma cellulärt beteende med molekylär nivå‑precision. Eftersom dessa system svarar på lokala utlösare och kan omorganisera sig själva kan de i princip skilja sjuka celler från friska och verka endast där det behövs — genom att göra hål i energifabriker, störa återvinningscentraler, tysta skadliga gener eller återuppväcka immunsvar. Författarna menar att i takt med att bildbehandling, modellering och designmetoder förbättras kan dessa små byggare utvecklas från laboratoriekuriositeter till en ny generation adaptiva mediciner som talar samma strukturella språk som cellen själv.
Citering: Kim, D., Park, G., Seu, MS. et al. Biomimetic peptide self-assembly: interfacing with biomacromolecules to regulate cellular signaling. Exp Mol Med 58, 1038–1052 (2026). https://doi.org/10.1038/s12276-026-01691-6
Nyckelord: peptid-självmontering, cellsignalering, nanomedicin, organelle-riktad terapi, supramolekylära biomaterial