Clear Sky Science · ru
Биомиметическое самоорганизующееся пептидное строение: взаимодействие с биомакромолекулами для регулирования клеточной сигнализации
Создание крошечных структур для общения с клетками
Внутри каждой клетки бесчисленные молекулы сталкиваются, связываются и распадаются, формируя сигналы, поддерживающие жизнь. В этом обзоре рассматривается, как очень короткие фрагменты белков — пептиды — можно спроектировать так, чтобы они спонтанно организовывались в крошечные формы, которые прикрепляются к компонентам клетки и направляют сигналы в полезном направлении. Подражая стратегиям природы, учёные стремятся создать «умные» материалы, которые способны выборочно уничтожать раковые клетки, корректировать нарушенную сигнализацию или доставлять генетические терапии с большей точностью, чем современные лекарства.
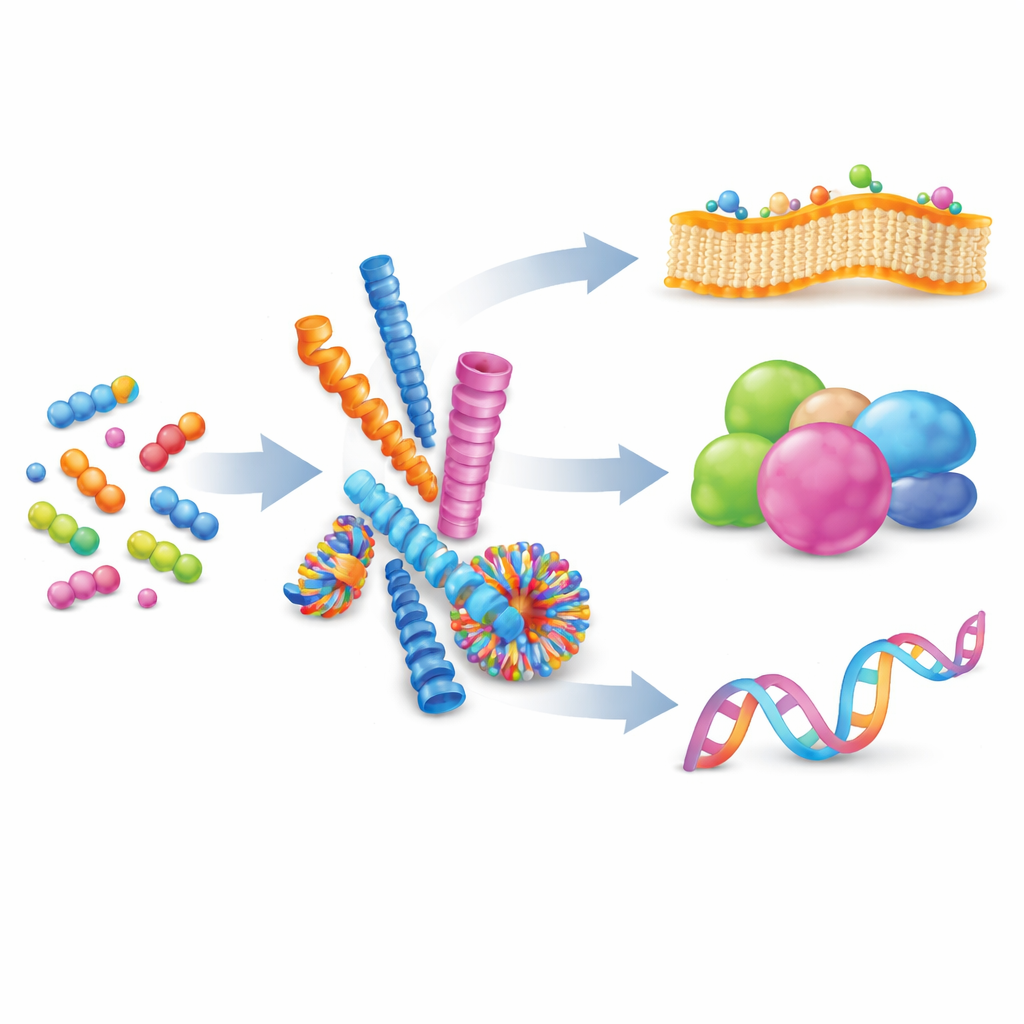
От разрозненных молекул к организованным наноструктурам
Авторы начинают с объяснения супрамолекулярной самосборки: процесса, при котором множество небольших молекул слабо притягиваются друг к другу и организуются в большие структуры без образования постоянных химических связей. Балансируя силы, такие как заряд, водородные связи и стекинг между плоскими кольцами, химики добиваются формирования у пептидов нанофибрилл, сфер, трубок или везикул. Эти формы не являются статичными; их строительные блоки могут обмениваться местами, что делает сборки обратимыми и адаптируемыми. Когда многие слабые взаимодействия сосредоточены на общей поверхности, они создают «мультивалентность» — мощный способ усилить иначе слабые связывания, подобно множеству крошечных крючков, цепляющихся за поверхность одновременно.
Заимствование сценария природы
Природа уже использует самосборку для выполнения сложных задач. Белки сворачиваются из простых цепочек аминокислот в сложные трёхмерные формы, создавая широкие контактные поверхности, которые связывают другие белки, ДНК или мембраны. Эти контакты, часто распределённые по обширным областям, позволяют клеткам быстро и обратимо включать или выключать сигнализацию. Вдохновлённые этим, исследователи разрабатывают искусственные пептиды, имитирующие такие интерфейсы. По сравнению с полимерами, липидами или ДНК‑каркасами пептидные системы занимают удобную «золотую середину»: они биосовместимы, химически разнообразны и точны на уровне отдельных аминокислот, что позволяет тонко настраивать форму, заряд и поведение связывания. Этот обзор фокусируется на том, как синтетические пептидные сборки используются для взаимодействия с тремя основными целями: клеточными мембранами, белками и нуклеиновыми кислотами.
Перепрограммирование клетки из мембраны внутрь
Главная тема статьи — использование самоорганизации пептидов для прямого воздействия на клеточные мембраны, особенно мембраны ключевых органелл, таких как митохондрии, лизосомы, эндоплазматический ретикулум и аппарат Гольджи. Пептиды можно снабдить направляющими группами, которые доставляют их к определённой органелле, где локальные условия — например кислотность, электрический потенциал или активность ферментов — запускают их сборку в нанофибриллы или частицы на поверхности мембраны. В митохондриях, к примеру, некоторые конструкции остаются безвредными в рассеянном состоянии в клетке, но агрегируют в жёсткие волокна при концентрации под воздействием отрицательного потенциала органеллы. Эти волокна могут пробивать или дестабилизировать двойную мембрану, нарушая градиент энергии, высвобождая цитохром c и активируя пути программируемой гибели клеток, что ценно при атаке опухолевых клеток.
Преобразование деградативных компартментов в центры управления
Лизосомы, часто рассматриваемые просто как клеточные центры переработки, здесь показаны как переключательные узлы для решений «жизнь‑или‑смерть». Пептиды, разработанные для обнаружения кислой среды лизосомы или её ферментов, могут собираться только после того, как клетка их поглотит и транспортирует в этот компартмент. После сборки их наноструктуры могут ослаблять лизосомальную мембрану, позволяя пищеварительным ферментам, таким как катепсины, вытекать и запускать клеточную смерть. Другие пептидные системы сконструированы так, чтобы покидать лизосомы на тщательно выбранных стадиях, помогая доставлять терапевтический груз, например нуклеиновые кислоты, в цитоплазму. Подобные стратегии, применённые к эндоплазматическому ретикулуму и аппарату Гольджи, позволяют усиливать «стрессовые» реакции или нарушать сортировку белков, снова направляя клетки к самоуничтожению контролируемым образом.
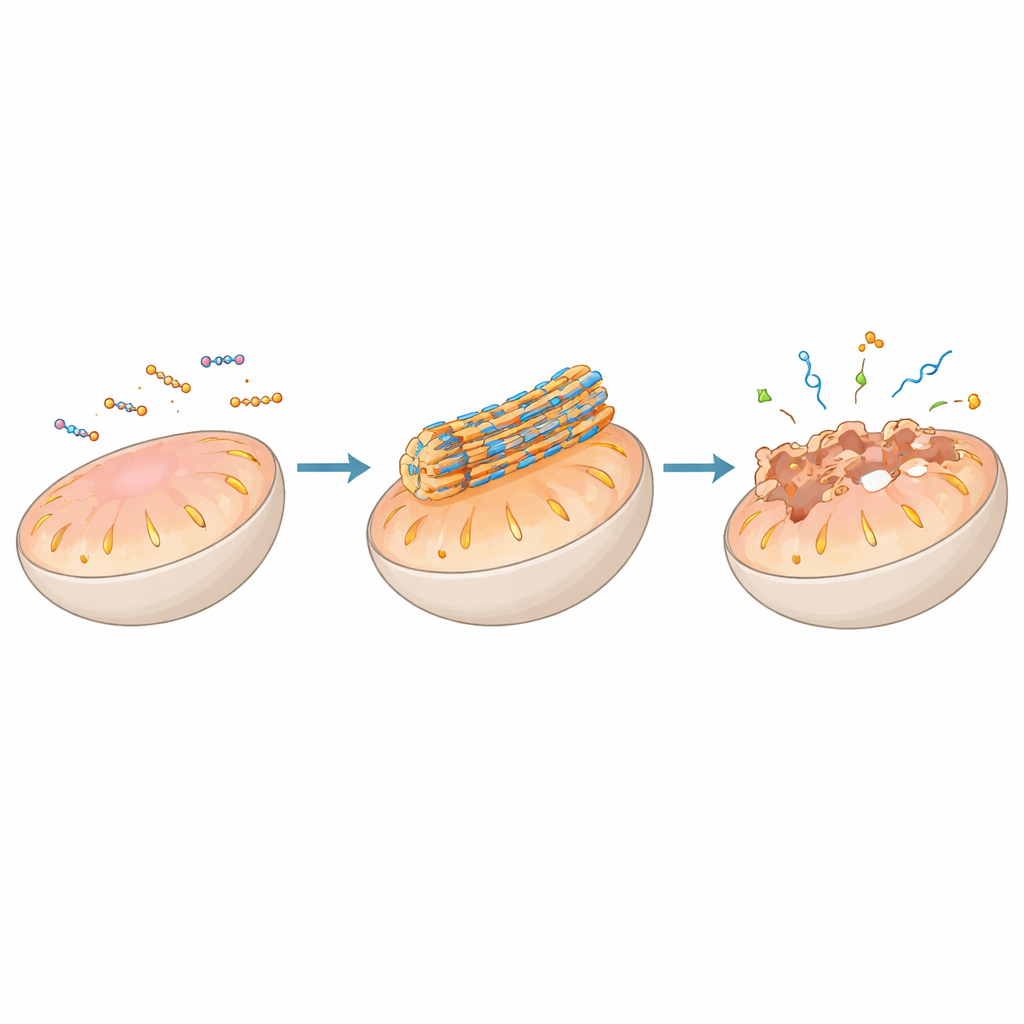
Направление белков и генов с помощью пептидных каркасов
Помимо воздействия на мембраны, пептидные сборки могут захватывать белки или нуклеиновые кислоты и перестраивать целые сигнальные сети. Некоторые сборки так точно имитируют природные участки связывания белков, что встраиваются в интерфейсы белок–белок, считавшиеся ранее недоступными для лекарств, освобождая протективные или про‑смертные сигналы в митохондриях или блокируя сигналы роста на поверхности клеток. Другие со‑сборки с антителами или рецепторами кластеризуют их, помечают для удаления в лизосомах или усиливают иммунное распознавание раковых клеток. В сочетании с ДНК или РНК положительно заряженные пептиды конденсируют генетический материал в компактные частицы или жидкоподобные капли, которые проникают в клетки и высвобождают груз в нужное время и месте, обеспечивая ингибирование или активацию генов. В некоторых случаях пептидно‑РНК капли ведут себя как искусственные «конденсаты», напоминая стресс‑гранулы, которые клетки естественно формируют для управления РНК в критические моменты.
Почему эти крошечные строители важны
В заключение обзор делает вывод, что биомиметическая самосборка пептидов предоставляет гибкий набор инструментов для перестройки клеточного поведения с точностью на молекулярном уровне. Поскольку эти системы реагируют на локальные триггеры и могут реорганизовываться, они, по сути, способны отличать больные клетки от здоровых и действовать только там, где нужно — пробивая «энергетические фабрики», нарушая центры переработки, заглушая вредные гены или вновь разжигая иммунную атаку. Авторы утверждают, что по мере совершенствования методов визуализации, моделирования и дизайна эти крошечные строители могут превратиться из лабораторных курьёзов в новое поколение адаптивных лекарств, говорящих на той же структурной «речи», что и сама клетка.
Цитирование: Kim, D., Park, G., Seu, MS. et al. Biomimetic peptide self-assembly: interfacing with biomacromolecules to regulate cellular signaling. Exp Mol Med 58, 1038–1052 (2026). https://doi.org/10.1038/s12276-026-01691-6
Ключевые слова: самосборка пептидов, клеточная сигнализация, нано-медицина, терапия, нацеленная на органеллы, супрамолекулярные биоматериалы