Clear Sky Science · pt
Auto‑montagem de peptídeos biomiméticos: interação com biomacromoléculas para regular sinalização celular
Construindo Estruturas Minúsculas para Dialogar com as Células
Dentro de cada célula, incontáveis moléculas colidem, se ligam e se separam, gerando os sinais que nos mantêm vivos. Esta revisão explora como trechos muito curtos de proteínas, chamados peptídeos, podem ser projetados para se organizar espontaneamente em formas minúsculas que se prendem a componentes celulares e inclinam esses sinais em direções úteis. Ao aprender a imitar as estratégias da própria natureza, os cientistas esperam construir materiais inteligentes capazes de matar seletivamente células cancerosas, corrigir sinalização defeituosa ou entregar terapias genéticas com muito mais precisão do que os fármacos atuais.
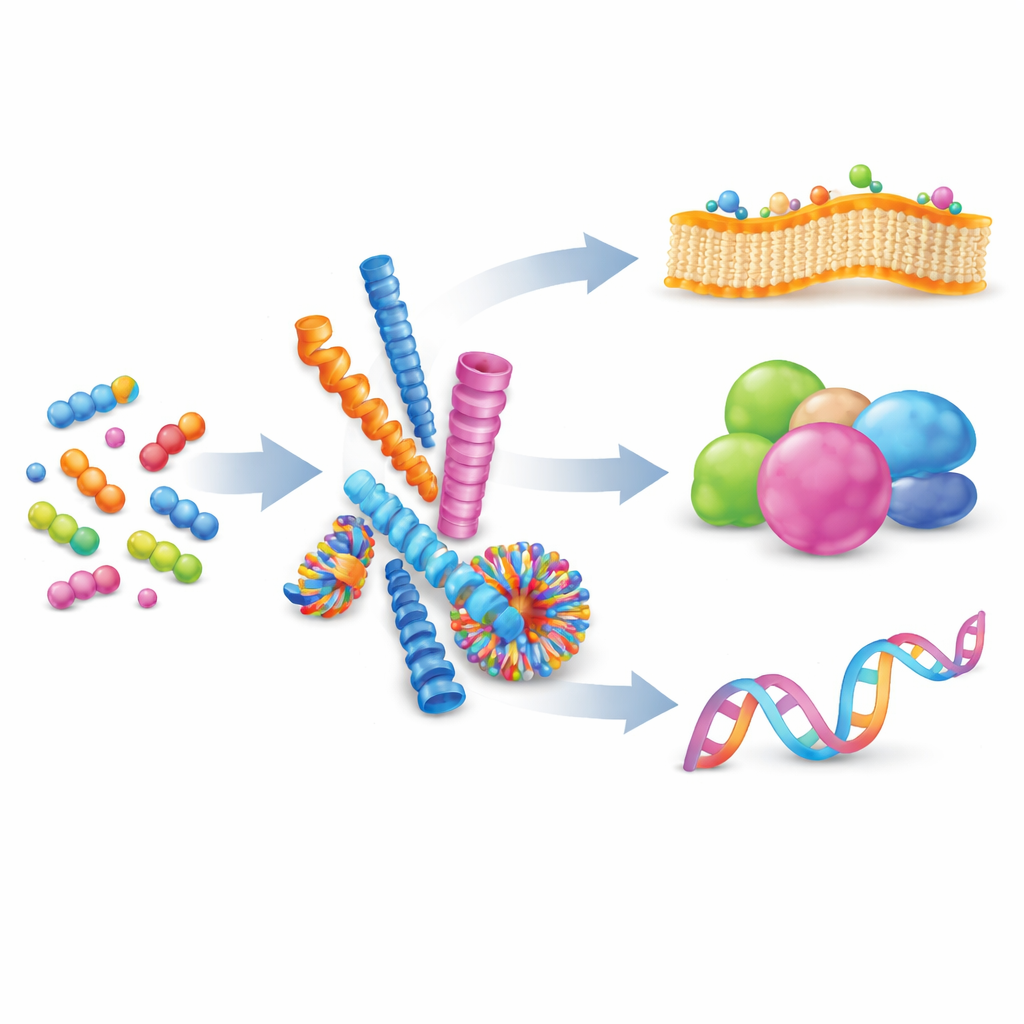
De Moléculas Soltas a Nanoestruturas Organizadas
Os autores começam explicando a auto‑montagem supramolecular: um processo em que muitas moléculas pequenas se atraem suavemente e se organizam em estruturas maiores sem formar ligações químicas permanentes. Ao equilibrar forças como carga, ligações de hidrogênio e empilhamento entre anéis planos, os químicos podem induzir peptídeos a formar nanofibras, esferas, tubos ou vesículas. Essas formas não são estáticas; seus blocos construtores podem trocar de dentro para fora, tornando os conjuntos reversíveis e adaptáveis. Quando muitas interações fracas ocorrem juntas em uma superfície compartilhada, geram “multivalência”, uma forma poderosa de fortalecer interações de ligação que seriam por si fracas, muito semelhante a vários ganchos minúsculos agarrando uma superfície ao mesmo tempo.
Pegando o Manual de Jogadas da Natureza
A natureza já depende da auto‑montagem para executar tarefas complexas. Proteínas se dobram a partir de cadeias simples de aminoácidos em formas tridimensionais intrincadas, expondo amplas áreas de contato que se ligam a outras proteínas, DNA ou membranas. Esses contatos, frequentemente distribuídos por grandes superfícies, permitem que as células liguem e desliguem sinais de forma rápida e reversível. Inspirados por isso, os pesquisadores projetam agora peptídeos artificiais que imitam tais interfaces. Em comparação com polímeros, lipídios ou estruturas de DNA, sistemas peptídicos oferecem um ponto de equilíbrio atraente: são biocompatíveis, quimicamente diversos e precisos ao nível de aminoácidos individuais, permitindo ajuste cuidadoso de forma, carga e comportamento de ligação. Esta revisão foca em como esses conjuntos peptídicos sintéticos são usados para engajar três alvos principais: membranas celulares, proteínas e ácidos nucleicos.
Reconfigurando a Célula de Fora para Dentro, a Partir da Membrana
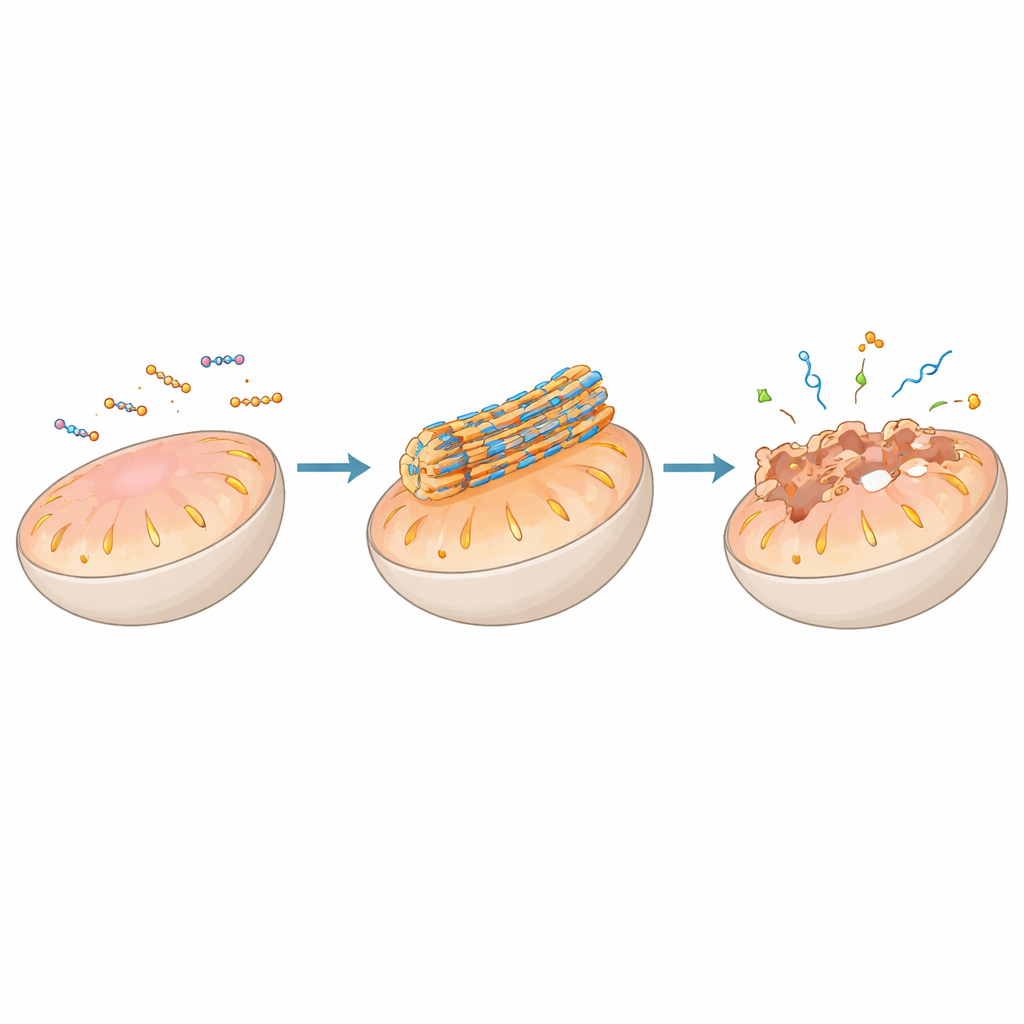
Um tema central do artigo é o uso da auto‑montagem de peptídeos para atuar diretamente nas membranas celulares, especialmente naquelas de organelas-chave como mitocôndrias, lisossomos, retículo endoplasmático e aparelho de Golgi. Peptídeos podem ser decorados com grupos direcionadores que os guiam a uma organela específica, onde condições locais — como acidez, potencial elétrico ou atividade enzimática — desencadeiam sua montagem em nanofibras ou partículas na superfície da membrana. Nas mitocôndrias, por exemplo, certos projetos permanecem inofensivos quando dispersos na célula, mas agregam em fibras rígidas quando concentrados pelo potencial negativo da organela. Essas fibras podem perfurar ou desestabilizar a membrana dupla, colapsando o gradiente de energia, liberando citocromo c e ativando vias de morte celular programada que são valiosas para atacar células tumorais.
Transformando Compartimentos Degradativos em Centros de Controle
Os lisossomos, muitas vezes vistos simplesmente como centros de reciclagem celular, são aqui reinterpretados como painéis de controle para decisões de vida ou morte. Peptídeos projetados para sentir o pH ácido do lisossomo ou enzimas residentes podem se montar somente após serem engolidos pela célula e traficados para esse compartimento. Uma vez montadas, suas nanoestruturas podem enfraquecer a membrana lisossomal, permitindo que enzimas digestivas como catepsinas vazem e desencadeiem a morte celular. Outros sistemas peptídicos são concebidos para escapar dos lisossomos em estágios cuidadosamente escolhidos, ajudando a transportar cargas terapêuticas como ácidos nucleicos para o interior da célula. Estratégias semelhantes aplicadas ao retículo endoplasmático e ao aparelho de Golgi permitem aos pesquisadores aumentar respostas de “estresse” ou perturbar o tráfego de triagem proteica, novamente direcionando células à autodestruição de forma controlada.
Guiando Proteínas e Genes com Andames de Peptídeos
Além das membranas, montagens peptídicas podem se prender a proteínas ou ácidos nucleicos e remodelar redes de sinalização inteiras. Algumas montagens imitam segmentos naturais de ligação a proteínas tão bem que se enfiem em interfaces proteína–proteína antes consideradas impossíveis de drugar, liberando sinais pró‑morte nas mitocôndrias ou bloqueando sinais de crescimento na superfície celular. Outras co‑montam com anticorpos ou receptores para agrupá‑los, marcá‑los para remoção em lisossomos ou aumentar o reconhecimento imune de células cancerosas. Quando combinados com DNA ou RNA, peptídeos carregados positivamente condensam material genético em partículas compactas ou gotículas com comportamento semelhante a líquido que entram nas células e liberam sua carga no momento e local corretos, possibilitando silenciamento ou ativação gênica. Em certos casos, gotículas peptídeo–RNA comportam‑se como “condensados” artificiais, ecoando grânulos de estresse que as células formam naturalmente para gerenciar RNA durante crises.
Por que Esses Pequenos Construtores São Importantes
A revisão conclui que a auto‑montagem de peptídeos biomiméticos oferece um kit de ferramentas flexível para remodelar o comportamento celular com precisão ao nível molecular. Porque esses sistemas respondem a gatilhos locais e podem se reorganizar, eles podem, em princípio, distinguir células doentes das saudáveis e agir somente onde necessário — perfurando fábricas de energia, perturbando centros de reciclagem, silenciando genes nocivos ou reacendendo o ataque imune. Os autores argumentam que, à medida que métodos de imagem, modelagem e design melhoram, esses pequenos construtores podem evoluir de curiosidades de laboratório para uma nova geração de medicamentos adaptativos que falem a mesma linguagem estrutural da própria célula.
Citação: Kim, D., Park, G., Seu, MS. et al. Biomimetic peptide self-assembly: interfacing with biomacromolecules to regulate cellular signaling. Exp Mol Med 58, 1038–1052 (2026). https://doi.org/10.1038/s12276-026-01691-6
Palavras-chave: auto‑montagem de peptídeos, sinalização celular, nanomedicina, terapia direcionada a organelas, biomateriais supramoleculares