Clear Sky Science · tr
Biyomimetik peptit kendi-kendine toplanması: hücresel sinyallemeyi düzenlemek için biomakromoleküllerle arayüz oluşturmak
Hücrelerle Konuşmak İçin Minik Yapılar İnşa Etmek
Her hücrenin içinde sayısız molekül çarpışır, bağlanır ve parçalanır; bunlar yaşamı sürdüren sinyalleri oluşturur. Bu derleme, peptit adı verilen çok kısa protein parçalarının, hücresel bileşenlere tutunup bu sinyalleri yararlı yönlere doğru itebilecek biçimde kendiliğinden minik şekillere organize olacak şekilde nasıl tasarlanabileceğini inceliyor. Doğanın kendi stratejilerini taklit etmeyi öğrenerek, bilim insanları kanser hücrelerini seçici olarak öldürebilen, bozuk sinyallemeyi düzeltebilen veya gen terapilerini günümüz ilaçlarından çok daha yüksek bir hassasiyetle taşıyabilen akıllı malzemeler inşa etmeyi umuyorlar.
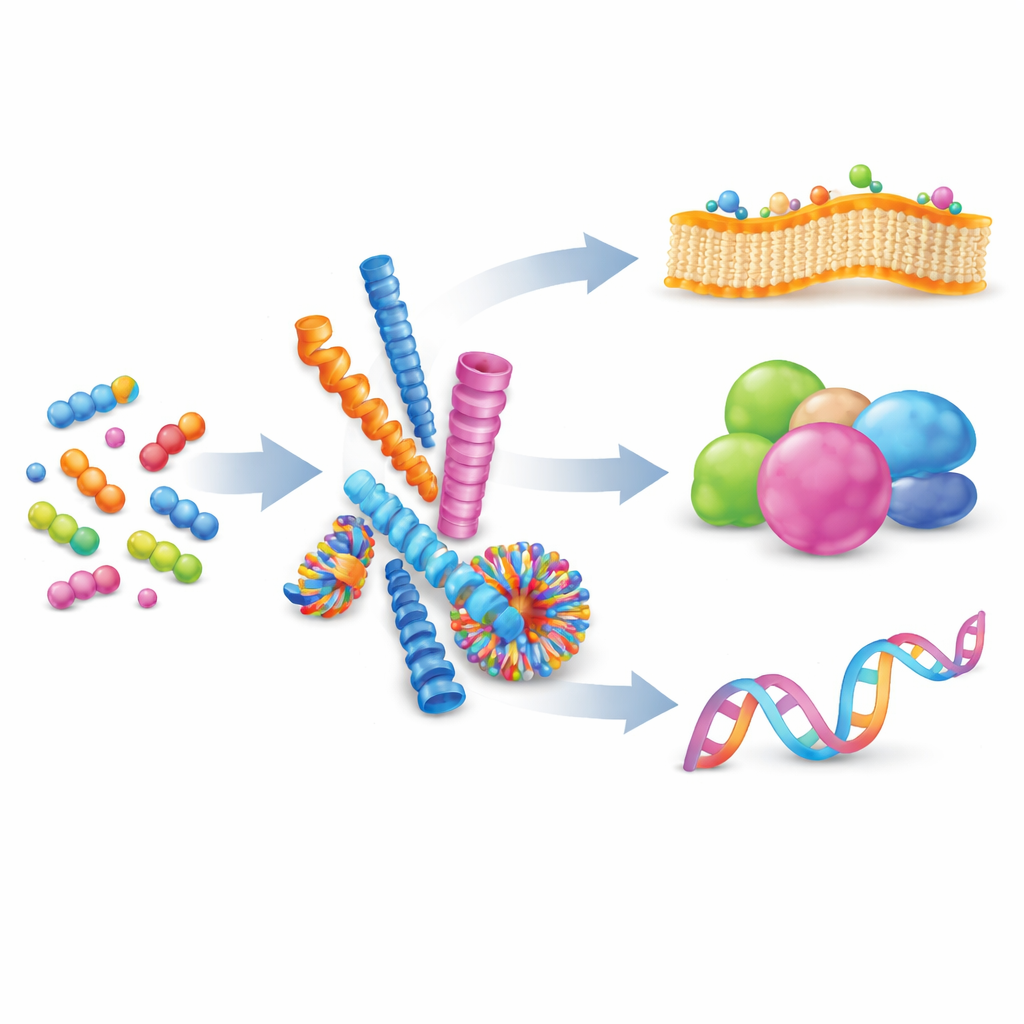
Gevşek Moleküllerden Düzenli Nanoyapılara
Yazarlar, birçok küçük molekülün birbirine nazikçe çekilerek kalıcı kimyasal bağlar oluşturmadan daha büyük yapılara organize olduğu supramoleküler kendi-kendine toplanmayı açıklamakla başlıyor. Yük, hidrojen bağları ve düz halkalar arasındaki istiflenme gibi kuvvetlerin dengelenmesiyle kimyagerler peptitleri nanolifler, küreler, tüpler veya veziküller oluşturacak şekilde yönlendirebiliyor. Bu şekiller statik değildir; yapıtaşları içeri girip çıkabilir, bu da montajların geri döndürülebilir ve uyarlanabilir olmasını sağlar. Birçok zayıf etkileşim ortak bir yüzeyde bir araya geldiğinde “multivalans” oluşur; bu, aksi takdirde zayıf olan bağlanma olaylarını güçlendiren, aynı anda bir yüzeyi kavrayan çok sayıda küçük kanca gibi etkili bir yoldur.
Doğanın Oyun Kitabını Ödünç Almak
Doğa karmaşık görevleri yürütmek için zaten kendi-kendine toplanmaya güvenir. Proteinler, amino asitlerin basit zincirlerinden katlanarak karmaşık üç boyutlu formlar alır ve diğer proteinlere, DNA'ya veya zarlarına bağlanan geniş temas alanları açığa çıkarır. Bu temaslar genellikle geniş yüzeylere yayılır ve hücrelerin sinyallemeyi hızlı ve geri döndürülebilir şekilde açıp kapatmasına olanak verir. Buna ilhamla, araştırmacılar artık bu tür arayüzleri taklit eden yapay peptitler tasarlıyor. Polimerler, lipidler veya DNA çerçeveleriyle karşılaştırıldığında peptit sistemleri uygun bir denge sunar: biyouyumlu, kimyasal olarak çeşitli ve tek tek amino asit düzeyinde hassasiyet sağlayarak şekil, yük ve bağlanma davranışının dikkatle ayarlanmasına imkan verir. Bu derleme, bu insan yapımı peptit montajlarının üç ana hedefle nasıl etkileşime girdiğine odaklanıyor: hücre zarları, proteinler ve nükleik asitler.
Zardan İçeriye Hücreyi Yeniden Kabuklandırmak
Makalenin ana temalarından biri, peptit kendi-kendine toplanmasının özellikle mitokondri, lizozom, endoplazmik retikulum ve Golgi aygıtı gibi önemli organellerin zarlarında doğrudan hareket etmesi için kullanılmasıdır. Peptitler, onları belirli bir organele yönlendiren hedefleme gruplarıyla donatılabilir; burada asidite, elektriksel potansiyel veya enzim aktivitesi gibi yerel koşullar, onların zar yüzeyinde nanolifler veya partiküller oluşturmak üzere toplanmasını tetikler. Örneğin mitokondride, belirli tasarımlar hücre içinde dağınık haldeyken zararsız kalır ama organelin negatif voltajı tarafından yoğunlaştırıldıklarında sert lifler halinde toplanır. Bu lifler çift zarı delip istikrarsızlaştırarak enerji gradyanını çökertir, sitokrom c'nin serbest kalmasına neden olur ve tümör hücrelerine karşı faydalı olabilecek programlı hücre ölüm yollarını aktive eder.
Yıkıcı Bölmeleri Kontrol Merkezlerine Dönüştürmek
Sıklıkla sadece hücresel geri dönüşüm merkezleri olarak düşünülen lizozomlar burada yaşam ve ölüm kararları için birer anahtar panosu olarak yeniden kurgulanıyor. Lizozomun asidik pH'ını veya yerel enzimlerini algılayacak şekilde tasarlanmış peptitler, yalnızca hücre tarafından yutulup bu bölmeye taşındıklarında toplanabilir. Bir kez toplandıklarında, nanoyapıları lizozomal zarı zayıflatabilir, böylece kathepsinler gibi sindirici enzimlerin sızmasına ve hücre ölümünü tetiklemesine izin verir. Diğer peptit sistemleri, nükleik asitler gibi terapötik yükleri hücrenin içine taşımaya yardımcı olmak için dikkatle seçilmiş aşamalarda lizozomdan kaçmak üzere tasarlanmıştır. Endoplazmik retikulum ve Golgi üzerinde uygulanan benzer stratejiler, araştırmacıların “stres” yanıtlarını artırmasına veya protein ayırma trafiğini bozmasına izin vererek hücreleri yine kontrollü bir şekilde kendi kendilerini yok etmeye yönlendirir.
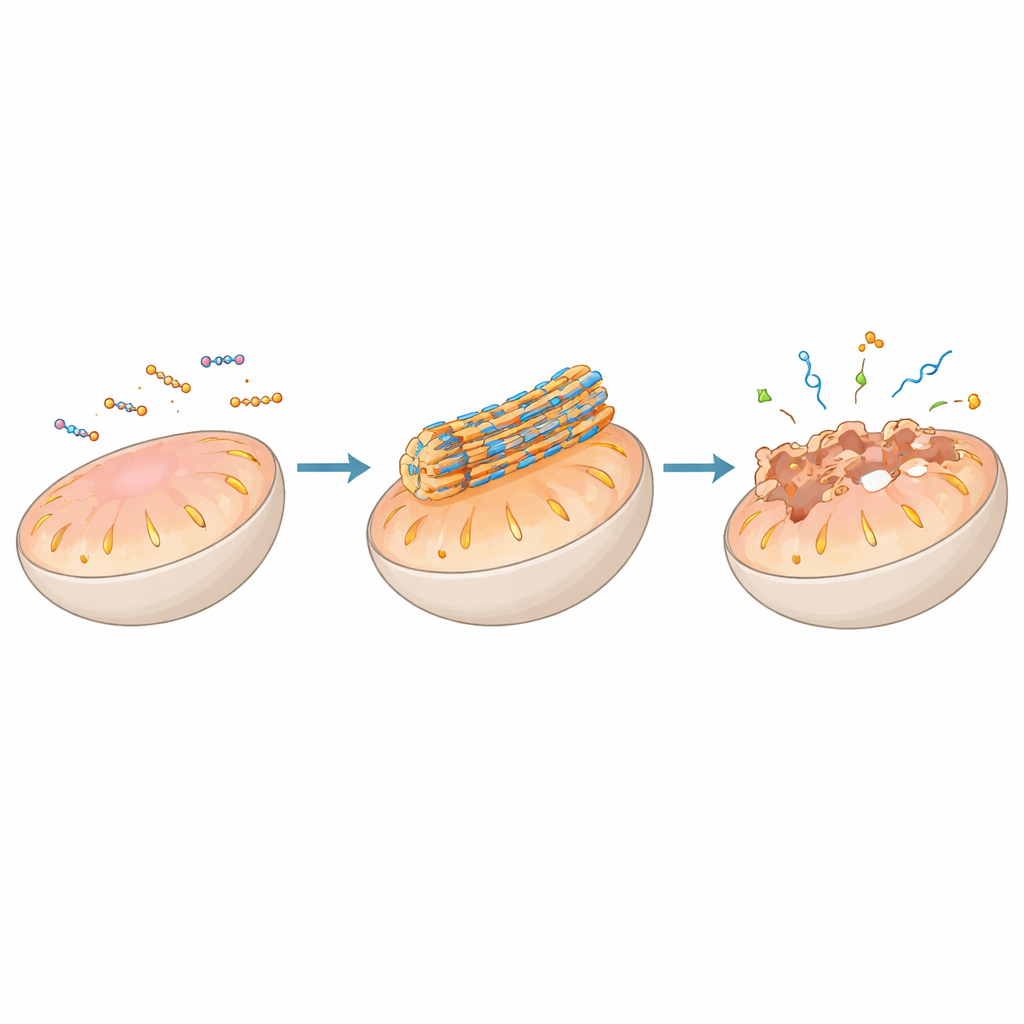
Peptit İskeleleriyle Proteinleri ve Genleri Yönlendirmek
Zarların ötesinde, peptit montajları proteinlere veya nükleik asitlere tutunarak tüm sinyal ağlarını yeniden şekillendirebilir. Bazı montajlar doğal protein-binder segmentlerini o kadar iyi taklit eder ki, bir zamanlar ilaçla hedeflenmesi imkansız kabul edilen protein–protein arayüzlerine girerek mitokondride ölüm sinyallerini serbest bırakır veya hücre yüzeyindeki büyüme işaretlerini engeller. Diğerleri antikorlar veya reseptörlerle birlikte toplanarak bunları kümeler, lizozomlarda yok edilmek üzere işaretler veya kanser hücrelerinin bağışıklık tanınmasını güçlendirir. DNA veya RNA ile birleştirildiğinde, pozitif yüklü peptitler genetik materyali hücrelere girip yükü doğru zaman ve yerde serbest bırakacak sıkıştırılmış partiküllere veya sıvı-benzeri damlacıklara yoğunlaştırır; bu da gen susturma veya aktivasyonunu mümkün kılar. Bazı durumlarda peptit–RNA damlacıkları, hücrelerin kriz sırasında RNA'yı yönetmek için doğal olarak oluşturduğu stres granüllerini andıran yapay “kondensatlar” gibi davranır.
Neden Bu Minik İnşaatçılar Önemli?
Derleme, biyomimetik peptit kendi-kendine toplanmasının hücresel davranışı moleküler düzeyde hassasiyetle yeniden şekillendirmek için esnek bir araç takımı sunduğunu özetleyerek sona eriyor. Bu sistemler yerel tetiklere yanıt verdikleri ve kendilerini yeniden düzenleyebildikleri için, teoride, hasta hücreleri sağlıklı olanlardan ayırt edebilir ve yalnızca gerektiği yerde hareket edebilir—enerji fabrikalarında delikler açarak, geri dönüşüm merkezlerini bozarak, zararlı genleri susturarak veya bağışıklık saldırısını yeniden alevlendirerek. Yazarlar, görüntüleme, modelleme ve tasarım yöntemleri geliştikçe bu minik inşaatçıların laboratuvar merakından hücrenin kendi yapısal dilinde konuşan yeni nesil uyarlanabilir ilaçlara evrilebileceğini savunuyorlar.
Atıf: Kim, D., Park, G., Seu, MS. et al. Biomimetic peptide self-assembly: interfacing with biomacromolecules to regulate cellular signaling. Exp Mol Med 58, 1038–1052 (2026). https://doi.org/10.1038/s12276-026-01691-6
Anahtar kelimeler: peptit kendi-kendine toplanması, hücre sinyallemesi, nanotıp, organel hedefli tedavi, supramoleküler biyomalzemeler