Clear Sky Science · nl
Biomimetische peptide‑zelfassemblage: interfacing met biomacromoleculen om cellulaire signalering te reguleren
Kleine structuren bouwen om met cellen te communiceren
In elke cel botsen, binden en breken talloze moleculen voortdurend, waardoor de signalen ontstaan die ons in leven houden. Deze overzichtsartikel onderzoekt hoe zeer korte stukjes eiwitten, peptides genoemd, zo kunnen worden ontworpen dat ze spontaan organiseren tot kleine vormen die zich aan celcomponenten hechten en die signalen in nuttige richtingen sturen. Door de strategieën van de natuur na te bootsen, hopen onderzoekers slimme materialen te bouwen die selectief kankercellen kunnen doden, foutieve signalering kunnen corrigeren of genetische therapieën met veel grotere precisie kunnen afleveren dan de huidige geneesmiddelen.
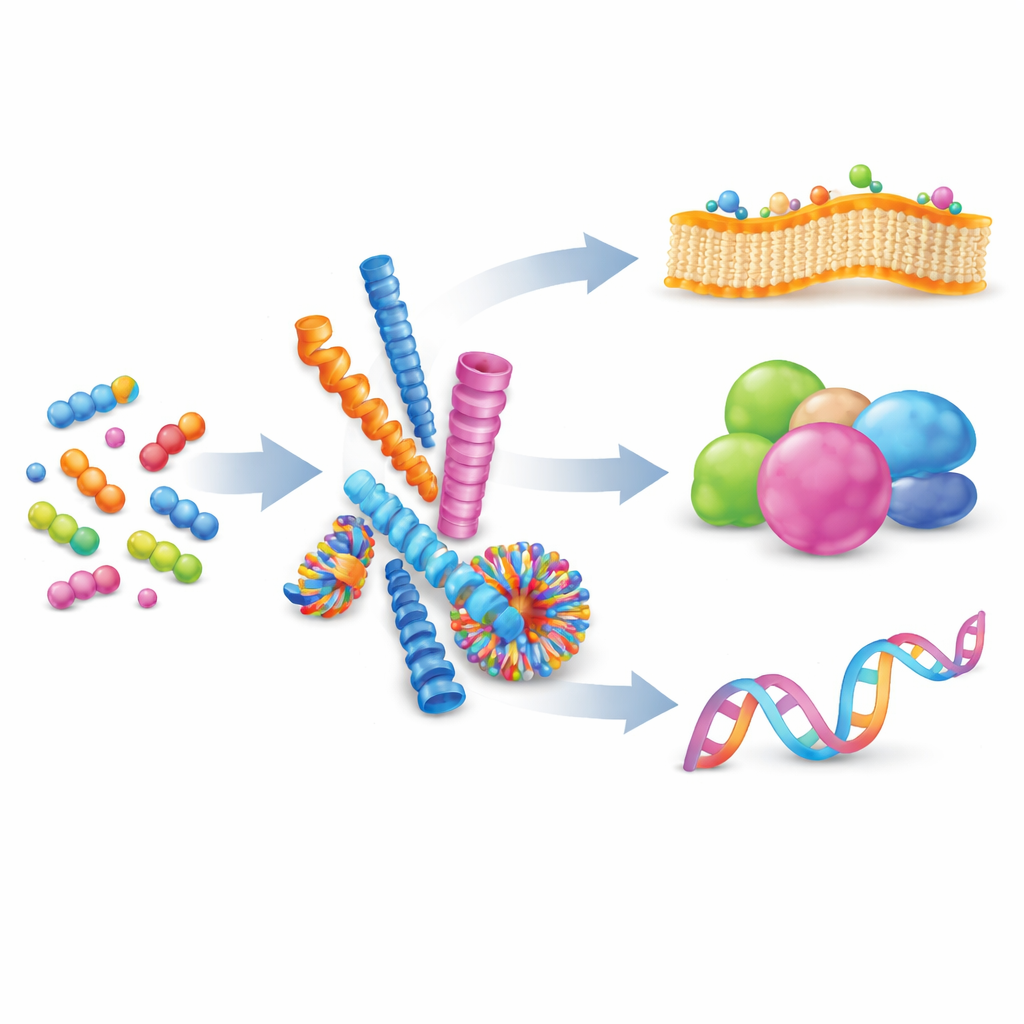
Van losse moleculen naar georganiseerde nanostructuren
De auteurs beginnen met het uitleggen van supramoleculaire zelfassemblage: een proces waarbij veel kleine moleculen elkaar zacht aantrekken en zich organiseren tot grotere structuren zonder permanente covalente bindingen te vormen. Door krachten zoals lading, waterstofbruggen en stapeling tussen vlakke ringen in balans te brengen, kunnen chemici peptides verleiden om nanovezels, sferen, buizen of vesikels te vormen. Deze vormen zijn niet statisch; hun bouwstenen kunnen in- en uitwisselen, waardoor de assemblages omkeerbaar en aanpasbaar zijn. Wanneer veel zwakke interacties samen op een gedeeld oppervlak plaatsvinden, creëren ze ‘multivalentie’, een krachtige manier om anders zwakke bindingsgebeurtenissen te versterken, vergelijkbaar met meerdere kleine haakjes die tegelijk een oppervlak grijpen.
Inspiratie uit het spelboek van de natuur
De natuur vertrouwt al op zelfassemblage om complexe taken uit te voeren. Eiwitten vouwen zich van eenvoudige ketens aminozuren tot ingewikkelde driedimensionale vormen, waarbij brede contactgebieden worden blootgelegd die andere eiwitten, DNA of membranen binden. Deze contacten, vaak verspreid over grote oppervlakken, stellen cellen in staat signalering snel en omkeerbaar aan of uit te zetten. Geïnspireerd door dit principe ontwerpen onderzoekers nu kunstmatige peptides die dergelijke interfaces imiteren. In vergelijking met polymeren, lipiden of DNA‑raamwerken bieden peptides een aantrekkelijk midden: ze zijn biocompatibel, chemisch divers en nauwkeurig op het niveau van individuele aminozuren, waardoor vorm, lading en bindgedrag zorgvuldig kunnen worden afgestemd. Dit overzicht richt zich op hoe deze kunstmatig gemaakte peptideassemblages worden ingezet om drie hoofddoelen te raken: celmembranen, eiwitten en nucleïnezuren.
De cel herbedraden vanaf het membraan naar binnen
Een belangrijk thema van het artikel is het gebruik van peptide‑zelfassemblage om direct op cellulaire membranen in te werken, met name die van belangrijke organellen zoals mitochondriën, lysosomen, het endoplasmatisch reticulum en het Golgi‑apparaat. Peptides kunnen worden voorzien van richtgroepen die ze naar een specifiek organel leiden, waar lokale omstandigheden—zoals zuurgraad, elektrische potentiaal of enzymactiviteit—hen doen assembleren tot nanovezels of deeltjes op het membraanoppervlak. In mitochondriën blijven bepaalde ontwerpen bijvoorbeeld onschadelijk wanneer ze verspreid in de cel circuleren, maar aggregeren ze tot stijve vezels zodra ze door de negatieve spanning van het organel worden geconcentreerd. Deze vezels kunnen de dubbele membraan doorboren of destabiliseren, de energiegradiënt laten instorten, cytochroom c vrijlaten en geprogrammeerde celdoodroutes activeren die waardevol zijn voor het aanvallen van tumorcellen.
Degraderende compartimenten omvormen tot controlepunten
Lysosomen, vaak gezien als louter cellulaire recyclingcentra, worden hier opgevat als schakelborden voor levens‑of‑doodsbeslissingen. Peptides die zijn ontworpen om de zure pH of residentiële enzymen van de lysosoom te detecteren, kunnen pas assembleren nadat ze door de cel zijn opgenomen en naar dit compartiment zijn getransporteerd. Eenmaal geassembleerd, kunnen hun nanostructuren het lysosomale membraan verzwakken, waardoor spijsverteringsenzymen zoals cathepsines kunnen lekken en celdood kunnen oproepen. Andere peptidesystemen zijn ontworpen om op zorgvuldig gekozen momenten uit lysosomen te ontsnappen, zodat therapeutische ladingen zoals nucleïnezuren het celinterieur kunnen bereiken. Vergelijkbare strategieën toegepast op het endoplasmatisch reticulum en het Golgi‑apparaat stellen onderzoekers in staat stressreacties op te voeren of het eiwit‑sorteringsverkeer te verstoren, opnieuw cellen op gecontroleerde wijze richting zelfvernietiging te sturen.
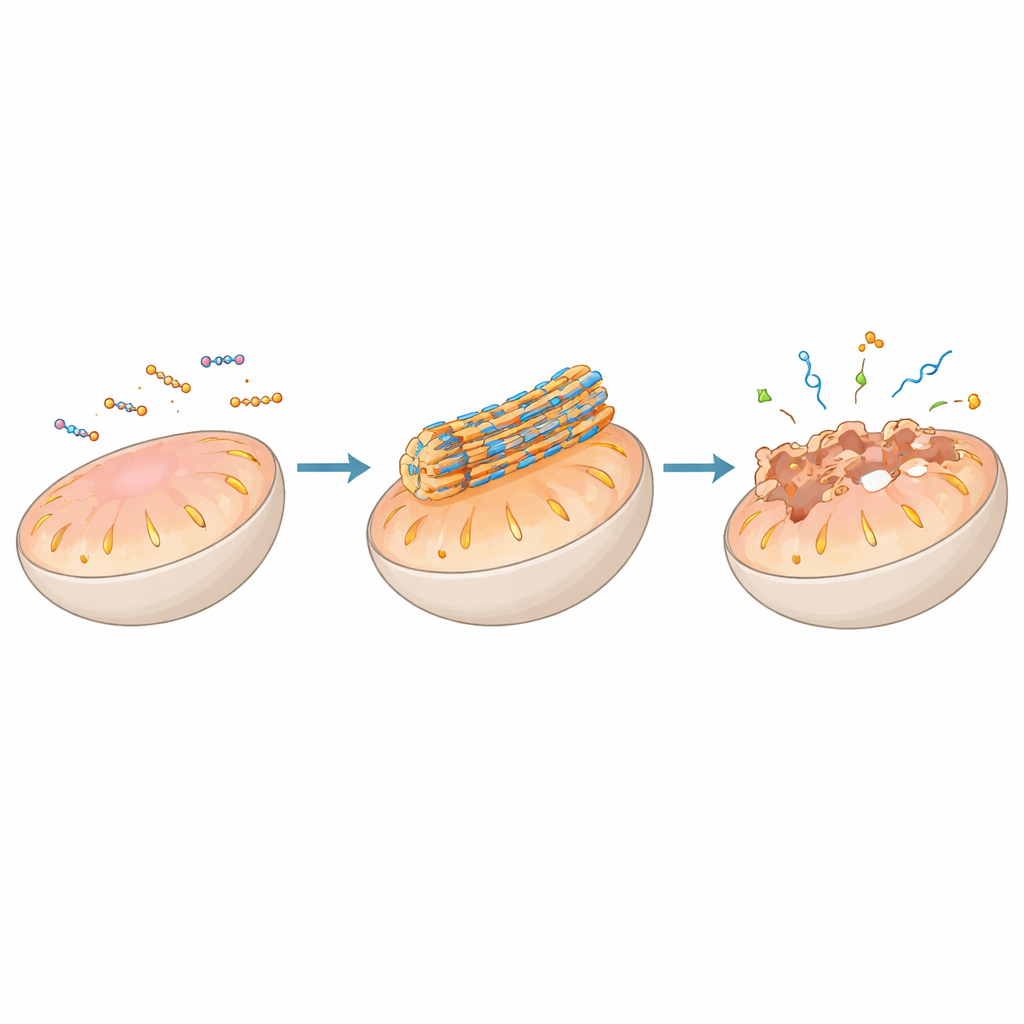
Eiwitten en genen sturen met peptide‑scaffolds
Buiten membranen kunnen peptideassemblages zich vastklemmen aan eiwitten of nucleïnezuren en complete signaalnetwerken hervormen. Sommige assemblages imiteren natuurlijke eiwitbindingssegmenten zo goed dat ze in eiwit‑eiwitinterfaces glijden die eerder als onbereikbaar voor geneesmiddelen werden beschouwd, waardoor pro‑doodsignalen in mitochondriën vrijkomen of groeisignalen aan het celoppervlak worden geblokkeerd. Andere co‑assembleren met antilichamen of receptoren om deze te clusteren, te markeren voor verwijdering in lysosomen, of de immuunherkenning van kankercellen te versterken. In combinatie met DNA of RNA condensen positief geladen peptides genetisch materiaal tot compacte deeltjes of vloeibare‑achtige druppels die in cellen glippen en hun lading op het juiste moment en de juiste plaats vrijgeven, waarmee gen‑stillegging of activering mogelijk wordt. In bepaalde gevallen gedragen peptide–RNA‑druppels zich als kunstmatige ‘condensaten’, die doen denken aan stressgranules die cellen van nature vormen om RNA tijdens crisissen te beheren.
Waarom deze kleine bouwers ertoe doen
Het review besluit dat biomimetische peptide‑zelfassemblage een flexibel gereedschapskist biedt om cellulair gedrag op moleculair niveau opnieuw vorm te geven. Omdat deze systemen reageren op lokale triggers en zichzelf kunnen reorganiseren, kunnen ze in principe zieke cellen van gezonde onderscheiden en alleen daar werken waar het nodig is—door gaten te slaan in energiecentrales, recyclingcentra te verstoren, schadelijke genen stil te leggen of de immuunaanval te heractiveren. De auteurs betogen dat naarmate beeldvorming, modellering en ontwerpmethoden verbeteren, deze kleine bouwers kunnen evolueren van laboratoriumcuriosa tot een nieuwe generatie adaptieve geneesmiddelen die dezelfde structurele taal spreken als de cel zelf.
Bronvermelding: Kim, D., Park, G., Seu, MS. et al. Biomimetic peptide self-assembly: interfacing with biomacromolecules to regulate cellular signaling. Exp Mol Med 58, 1038–1052 (2026). https://doi.org/10.1038/s12276-026-01691-6
Trefwoorden: peptide zelfassemblage, celsignalering, nanomedicine, organel‑gericht therapie, supramoleculaire biomaterialen