Clear Sky Science · fr
Auto-assemblage de peptides biomimétiques : interfacer avec des biomacromolécules pour réguler la signalisation cellulaire
Construire de minuscules structures pour dialoguer avec les cellules
À l’intérieur de chaque cellule, d’innombrables molécules se heurtent, se lient et se séparent, générant les signaux qui nous maintiennent en vie. Cette revue examine comment de très courts fragments de protéines, appelés peptides, peuvent être conçus pour s’organiser spontanément en formes microscopiques qui s’accrochent aux composants cellulaires et orientent ces signaux de manière utile. En apprenant à imiter les stratégies naturelles, les scientifiques espèrent construire des matériaux intelligents capables d’éliminer sélectivement des cellules cancéreuses, de corriger des signalements défaillants ou de délivrer des thérapies géniques avec une précision bien supérieure à celle des médicaments actuels.
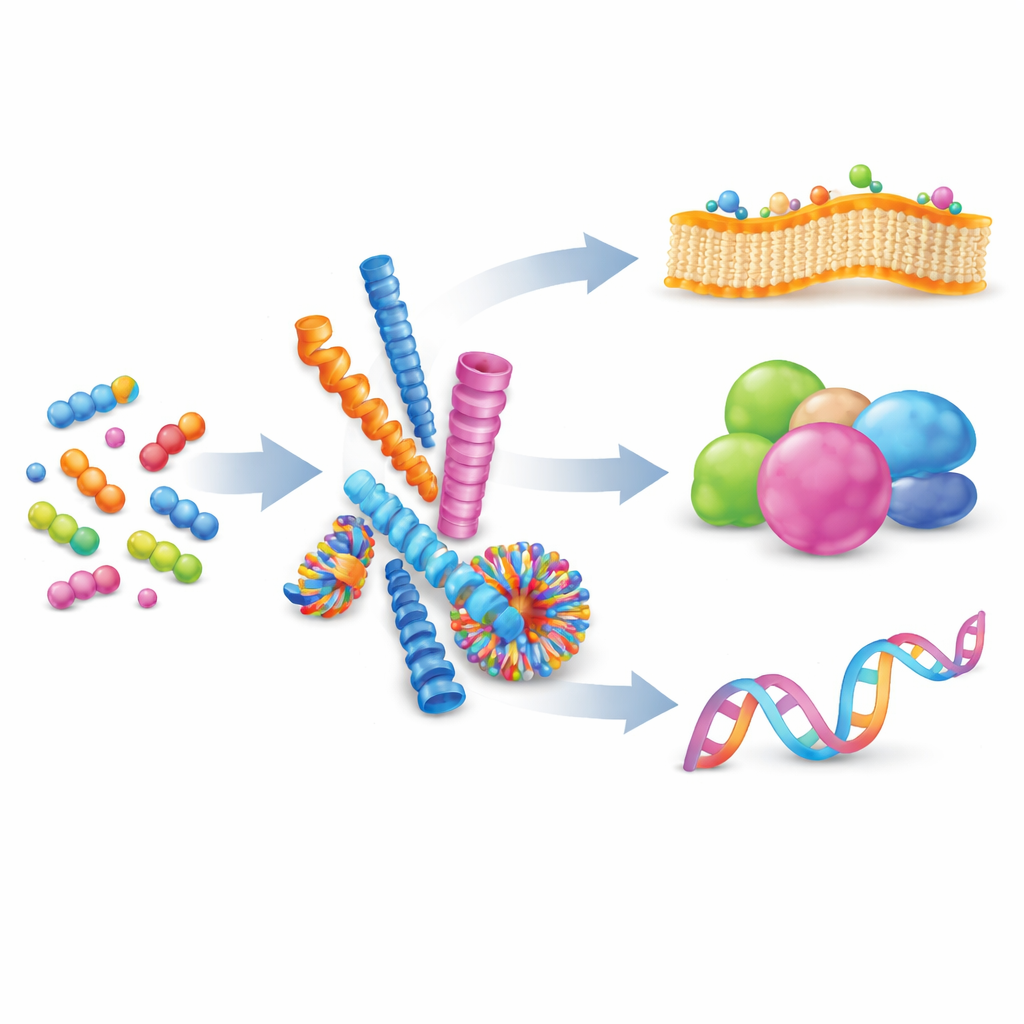
De molécules lâches à des nanostructures organisées
Les auteurs commencent par expliquer l’auto-assemblage supramoléculaire : un processus où de nombreuses petites molécules s’attirent doucement et s’organisent en structures plus grandes sans former de liaisons chimiques permanentes. En équilibrant des forces telles que la charge, les liaisons hydrogène et l’empilement entre anneaux plats, les chimistes peuvent inciter les peptides à former des nanofibres, des sphères, des tubes ou des vésicules. Ces formes ne sont pas statiques ; leurs éléments constitutifs peuvent s’échanger, rendant les assemblages réversibles et adaptables. Quand de nombreuses interactions faibles se produisent simultanément sur une surface partagée, elles créent une « multivalence », un moyen puissant de renforcer des événements de liaison autrement faibles, à l’instar de nombreux petits crochets agrippant une surface à la fois.
Emprunter le manuel de la nature
La nature s’appuie déjà sur l’auto-assemblage pour exécuter des tâches complexes. Les protéines se replient à partir de chaînes simples d’acides aminés en formes tridimensionnelles complexes, exposant de larges surfaces de contact qui lient d’autres protéines, l’ADN ou des membranes. Ces contacts, souvent répartis sur de grandes surfaces, permettent aux cellules d’activer et de désactiver la signalisation rapidement et de façon réversible. Inspirés par cela, les chercheurs conçoivent aujourd’hui des peptides artificiels qui imitent de telles interfaces. Comparés aux polymères, lipides ou architectures à base d’ADN, les systèmes peptidiques offrent un compromis intéressant : biocompatibles, chimiquement divers et précis au niveau des acides aminés individuels, ils permettent d’ajuster finement la forme, la charge et le comportement de liaison. Cette revue se concentre sur la manière dont ces assemblages peptidiques artificiels sont utilisés pour cibler trois principaux éléments : les membranes cellulaires, les protéines et les acides nucléiques.
Reconfigurer la cellule depuis la membrane vers l’intérieur
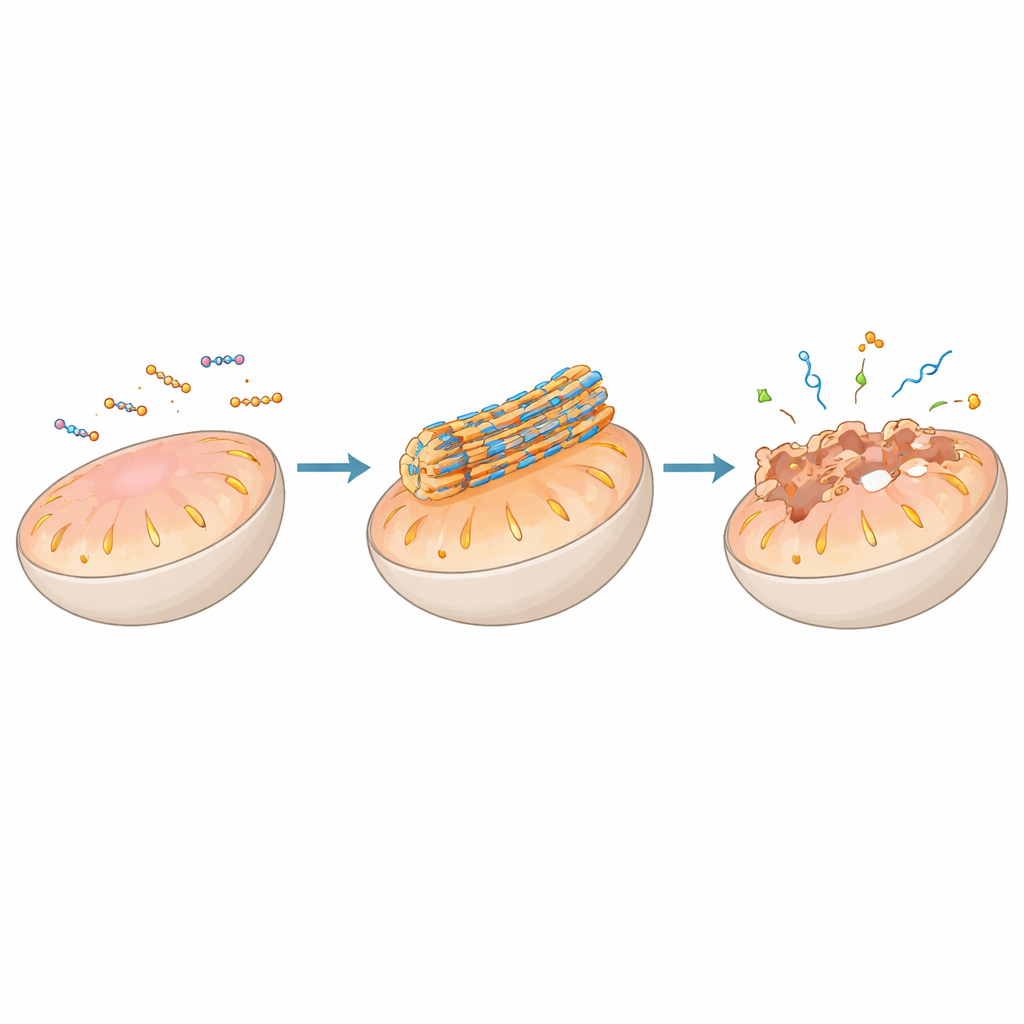
Un thème majeur de l’article est l’utilisation de l’auto-assemblage de peptides pour agir directement sur les membranes cellulaires, en particulier celles d’organelles clés telles que les mitochondries, les lysosomes, le réticulum endoplasmique et l’appareil de Golgi. Les peptides peuvent être décorés de groupes de ciblage qui les guident vers un organelle spécifique, où des conditions locales — telles que l’acidité, le potentiel électrique ou l’activité enzymatique — déclenchent leur assemblage en nanofibres ou particules à la surface de la membrane. Dans les mitochondries, par exemple, certains designs restent inoffensifs lorsqu’ils sont dispersés dans la cellule mais s’agrègent en fibres rigides une fois concentrés par la polarité négative de l’organite. Ces fibres peuvent perforer ou déstabiliser la membrane double, effondrer le gradient d’énergie, libérer le cytochrome c et activer des voies de mort cellulaire programmée utiles pour attaquer les cellules tumorales.
Transformer les compartiments dégradatifs en centres de contrôle
Les lysosomes, souvent vus simplement comme des centres de recyclage cellulaires, sont ici reconsidérés comme des tableaux de commande des décisions de vie ou de mort. Des peptides conçus pour détecter le pH acide du lysosome ou ses enzymes résidentes peuvent s’assembler uniquement après avoir été absorbés par la cellule et dirigés vers ce compartiment. Une fois assemblées, leurs nanostructures peuvent affaiblir la membrane lysosomale, permettant aux enzymes digestives telles que les cathepsines de fuir et de déclencher la mort cellulaire. D’autres systèmes peptidiques sont conçus pour s’échapper des lysosomes à des stades soigneusement choisis, aidant à acheminer des charges thérapeutiques comme des acides nucléiques vers l’intérieur de la cellule. Des stratégies similaires appliquées au réticulum endoplasmique et à l’appareil de Golgi permettent d’augmenter les réponses de « stress » ou de perturber le tri des protéines, orientant de nouveau les cellules vers l’autodestruction de façon contrôlée.
Guidage des protéines et des gènes par des échafaudages peptidiques
Au-delà des membranes, les assemblages peptidiques peuvent se fixer sur des protéines ou des acides nucléiques et remodeler des réseaux de signalisation entiers. Certains assemblages imitent si bien des segments de liaison protéique naturels qu’ils se glissent dans des interfaces protéine–protéine autrefois considérées comme inaccessibles aux médicaments, libérant des signaux pro‑mort dans les mitochondries ou bloquant des signaux de croissance à la surface cellulaire. D’autres co‑assemblent avec des anticorps ou des récepteurs pour les regrouper, les marquer pour élimination dans les lysosomes ou renforcer la reconnaissance immunitaire des cellules cancéreuses. Lorsqu’ils sont combinés avec de l’ADN ou de l’ARN, des peptides chargés positivement condensent le matériel génétique en particules compactes ou en gouttelettes de type liquide qui pénètrent dans les cellules et libèrent leur cargaison au moment et à l’endroit appropriés, permettant l’extinction ou l’activation génique. Dans certains cas, des gouttelettes peptide–ARN se comportent comme des « condensats » artificiels, rappelant les granules de stress que les cellules forment naturellement pour gérer l’ARN en période de crise.
Pourquoi ces petits bâtisseurs comptent
La revue conclut que l’auto-assemblage peptidique biomimétique offre une boîte à outils flexible pour remodeler le comportement cellulaire avec une précision au niveau moléculaire. Parce que ces systèmes répondent à des déclencheurs locaux et peuvent se réorganiser, ils peuvent en principe distinguer les cellules malades des cellules saines et n’agir que là où c’est nécessaire — en perforant les centrales énergétiques, en perturbant les centres de recyclage, en faisant taire des gènes nocifs ou en relançant l’attaque immunitaire. Les auteurs soutiennent qu’à mesure que les méthodes d’imagerie, de modélisation et de conception s’améliorent, ces petits bâtisseurs pourraient évoluer de curiosités de laboratoire vers une nouvelle génération de médicaments adaptatifs qui parlent le même langage structural que la cellule elle‑même.
Citation: Kim, D., Park, G., Seu, MS. et al. Biomimetic peptide self-assembly: interfacing with biomacromolecules to regulate cellular signaling. Exp Mol Med 58, 1038–1052 (2026). https://doi.org/10.1038/s12276-026-01691-6
Mots-clés: auto-assemblage de peptides, signalisation cellulaire, nanomédecine, thérapie ciblée sur les organelles, biomatériaux supramoléculaires