Clear Sky Science · he
הרכבה עצמית של פפטידים בביומימטיקה: ממשק עם ביומקרומולקולות לוויסות איתות תאי
בניית מבנים זעירים כדי לתקשר עם תאים
בתוך כל תא, מולקולות רבות מתנגשות, נקשרות ומתפרקות, ויוצרות את האותות ששומרים על חיינו. סקירה זו בוחנת כיצד חתיכות חלבון קצרות מאוד, הנקראות פפטידים, יכולות להיות מתוכננות להתארגן ספונטנית לצורות זעירות הנצמדות לרכיבים תאיים ומכוונות את אותות התא בכיוונים מועילים. על‑ידי חיקוי האסטרטגיות של הטבע, מדענים שואפים לבנות חומרים חכמים שיכולים להרוג תאים סרטניים בררנית, לתקן איתותים פגומים או למסור טיפולים גנטיים בדיוק רב יותר מאשר תרופות קיימות.
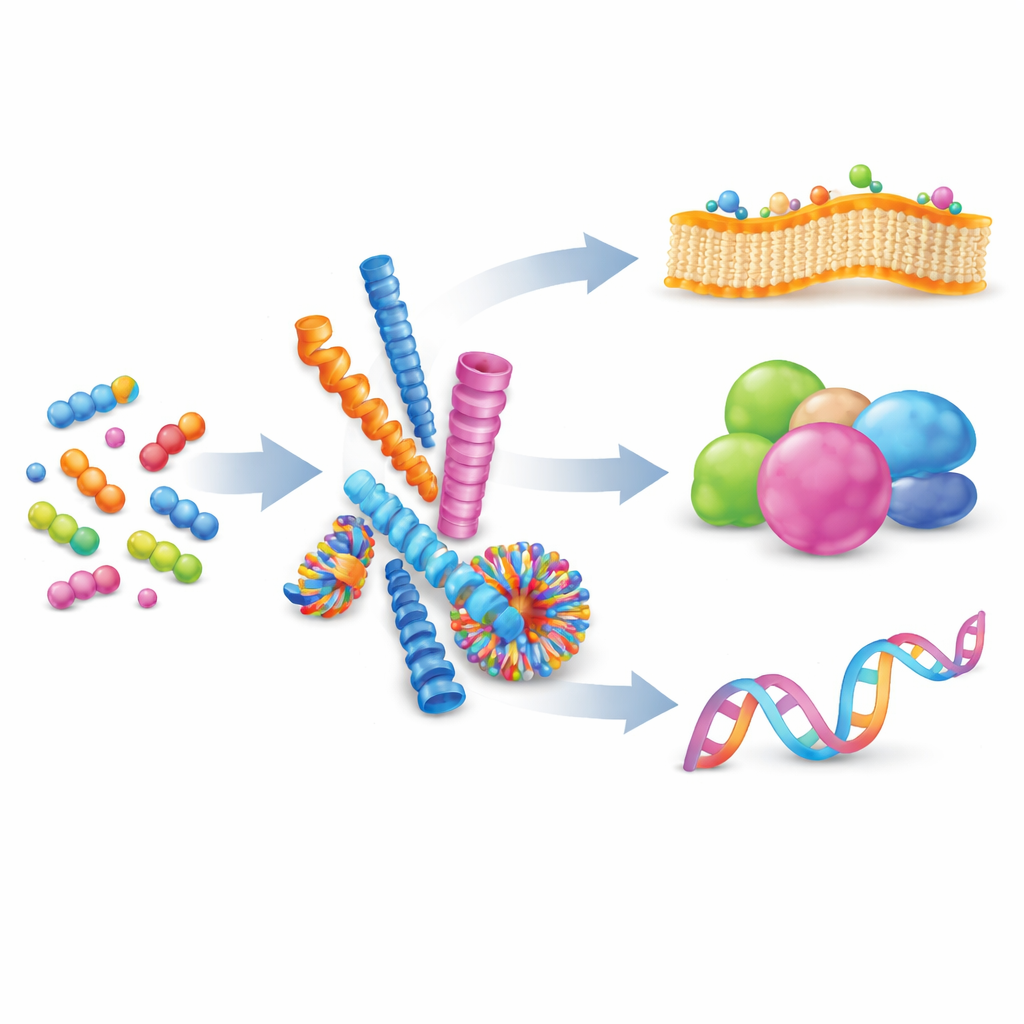
ממולקולות פזורות לננוסטרוקטורות מאורגנות
המחברים מתחילים בהסבר על הרכבה עצמית על‑מולקולרית: תהליך שבו מולקולות קטנות רבות נמשכות זו לזו ומתארגנות למבנים גדולים יותר מבלי ליצור קשרים כימיים קבועים. באמצעות איזון כוחות כמו מטען, קשרי מימן ו־stacking בין טבעות שטוחות, כימאים יכולים לגרום לפפטידים ליצור ננ inclusionים כמו סיביות, כדורים, צינורות או וזיקולות. הצורות הללו אינן סטטיות; יחידות הבנייה יכולות להחליף במבנה, מה שהופך את האסמבלאז’ים להפיכים ומתאימים. כאשר אינטראקציות חלשות רבות מתרחשות יחד על משטח משותף, הן יוצרות "רב‑ערכיות" (multivalency), דרך חזקה להגביר קישור שאינו חזק בפני עצמו, בדומה למספר ווים קטנים האוחזים במשטח במקביל.
שימוש בספר המשחקים של הטבע
הטבע כבר מסתמך על הרכבה עצמית כדי להפעיל משימות מורכבות. חלבונים מקפלים משרשראות חומצות אמיניות פשוטות לצורות תלת־ממדיות מורכבות, החושפות שטחים רחבים של מגע הקושרים חלבונים אחרים, DNA או ממברנות. מגעים אלו, שלעיתים מתפרסים על פני משטחים גדולים, מאפשרים לתאים להדליק ולכבות איתותים במהירות ובאופן הפיך. בהשראת זאת, חוקרים מעצבים כיום פפטידים מלאכותיים שמחקים ממשקים כאלה. בהשוואה לפולימרים, ליפידים או שלדות DNA, מערכות פפטידיות מציעות נקודת איזון נוחה: הן תואמות ביולוגית, מגוונות מבחינה כימית ומדויקות ברמת חומצת אמינו בודדת, מה שמאפשר כוונון מדויק של צורה, מטען והתנהגות קישור. סקירה זו מתמקדת כיצד ההרכבות הפפטידיות המלאכותיות משמשות למעורבות בשלושה יעדים עיקריים: ממברנות תאים, חלבונים וחומר תורשתי.
תכנות התא מהממברנה פנימה
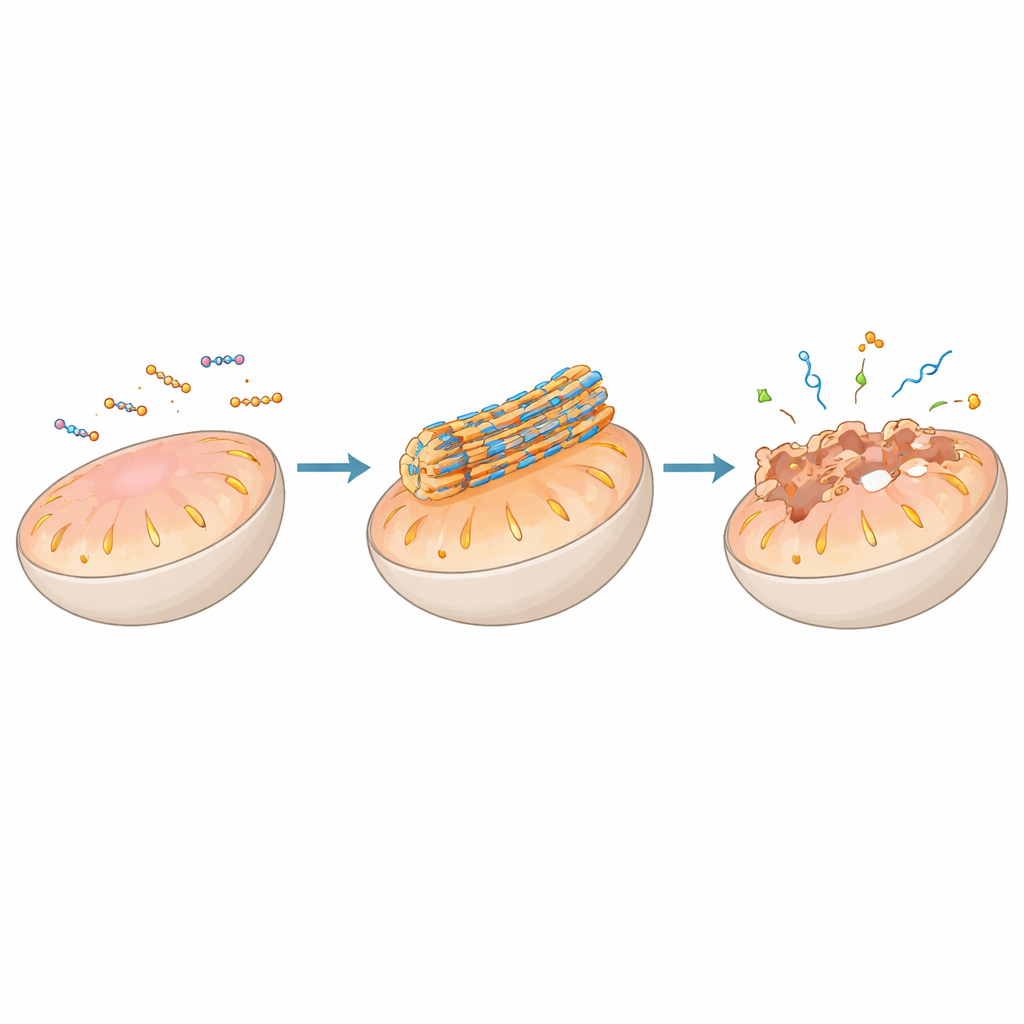
נושא מרכזי במאמר הוא שימוש בהרכבה עצמית של פפטידים כדי לפעול ישירות על ממברנות תאיות, במיוחד אלה של אברונים מרכזיים כגון מיטוכונדריה, ליזוזומים, רטיקולום אנדופלזמטי וגולג'י. פפטידים יכולים להיות מקושטים בקבוצות מטרה שמנחות אותם אל אברון מסוים, שם תנאים מקומיים — כגון חומציות, פוטנציאל חשמלי או פעילות אנזימטית — מעוררים אותם להתאסף לסיבי ננו או חלקיקים על פני הממברנה. במיטוכונדריה, לדוגמה, עיצובים מסוימים נשארים בלתי מזיקים כשהם מפוזרים בתא אך מצטברים לסיבים נוקשים ברגע שהם מרוכזים על ידי פוטנציאל שלילי של האברון. סיבים אלה יכולים לנקב או לייצב את ממברנת הכפולה, לקרוס את גרדיאנט האנרגיה, לשחרר ציטוכרום c ולהפעיל מסלולים של מוות מתוכנת שחשובים להתקפה על תאי גידול.
הפיכת תאיות פירוק לצירי שליטה
ליזוזומים, שלעיתים נתפסים כתאי מיחזור בלבד, מוצגים כאן כמפסקי החלטה בין חיים ומוות. פפטידים מהונדסים שמרגישים את ה־pH החמוצי של הליזוזום או אנזימים תושבים יכולים להתאסף רק לאחר שנבלעו על‑ידי התא ונסלו לתוך המחלקה הזו. לאחר ההרכבה, הננוסטרוקטורות שלהן יכולות להחליש את ממברנת הליזוזום, לאפשר לאנזימי פירוק כמו קטפסינים לדלוף ולהפעיל מוות תאי. מערכות פפטידיות אחרות מתוכננות לברוח מהליזוזום בשלבים נבחרים בקפידה, ולסייע בהעברת מטען תרפי כמו חומרים גנטיים לפנים התא. אסטרטגיות דומות המיושמות על הרטיקולום האנדופלזמטי וגולג'י מאפשרות לחוקרים להגביר תגובות "סטרס" או להפריע לתנועה של מיון חלבונים, שוב לכוון תאים לעבר השמדה עצמית באופן מבוקר.
הכוונת חלבונים וגנים בעזרת תבניות פפטידיות
מעבר לממברנות, הרכבות פפטידיות יכולות להצמיד לעצמן חלבונים או חומצות גרעין ולעצב מחדש רשתות איתות שלמות. חלק מההרכבות מחקות מקטעי קישור חלבוניים טבעיים כהדוק עד שהן נחדרות לממשקי חלבון‑חלבון שנחשבו בעבר לבלתי ניתנים לתרופה, משחררות אותות פרו‑מוות במיטוכונדריה או חוסמות אותות גדילה על פני תאי השטח. אחרות משתתפות בהרכבה משותפת עם נוגדנים או קולטים כדי לצבורם, לסמן אותם להסרה בליזוזומים או להגביר את ההכרה החיסונית בתאי סרטן. בשילוב עם DNA או RNA, פפטידים טעונים בחיוב מדחסים חומר גנטי לחלקיקים קומפקטיים או לטיפות שנראות נוזליות החודרות לתאים ומשחררות את המטען בזמן ובמקום המתאימים, מה שמאפשר השתקת גנים או הפעלתם. במקרים מסוימים, טיפות פפטיד–RNA מתנהגות כמו "עיבודים" מלאכותיים, מהדהדות גרגירי סטרס שתאים יוצרים באופן טבעי לניהול RNA בעת משבר.
למה בוני הזעירים האלה חשובים
הסקירה מסכמת כי הרכבה עצמית ביומימטית של פפטידים מציעה ערכת כלים גמישה לעיצוב מחדש של התנהגות תאית ברזולוציה מולקולרית. מאחר שמערכות אלו מגיבות למעוררים מקומיים ויכולות לארגן את עצמן מחדש, הן מסוגלות, בעקרון, להבחין בין תאים חולים לבריאים ולפעול רק במקום שבו נדרש — על ידי יצירת חורים במפעלי האנרגיה, הפרעת מרכזי המיחזור, השתקה של גנים מזיקים או הצתה מחודשת של ההתקפה החיסונית. המחברים טוענים שככל ששיטות הדמיה, מודלים ועיצוב ישתפרו, בוני‑הזעירים הללו עשויים להתפתח מסקרנות מעבדתית לדור חדש של תרופות אדפטיביות המדברות את שפת המבנה של התא עצמו.
ציטוט: Kim, D., Park, G., Seu, MS. et al. Biomimetic peptide self-assembly: interfacing with biomacromolecules to regulate cellular signaling. Exp Mol Med 58, 1038–1052 (2026). https://doi.org/10.1038/s12276-026-01691-6
מילות מפתח: ההרכבה העצמית של פפטידים, איתות תאי, ננודרגות, טיפול ממוקד אברון, ביומחומרים על‑מולקולריים