Clear Sky Science · tr
Rhodostomin ve Trimucrin tarafından integrin αvβ3’ün farklı tanınmasının yapısal temeli
Zehrin Proteinleri Hassas Tıp Araçlarına Dönüştü
Yılan zehri tamamen zehir gibi gelebilir, ama içindeki bazı moleküller vücudumuzdaki hastalıkla ilişkili proteinleri şaşırtıcı derecede iyi engeller. Bu çalışma, bu zehir kaynaklı moleküllerden ikisinin kansere ve kan damarı oluşumuna bağlı önemli bir hücre yüzeyi reseptörüne nasıl tutunduğunu atom düzeyinde ortaya koyuyor; bu bilgiler daha güvenli ve daha hedefe yönelik ilaçlar tasarlamaya rehberlik edebilir.
Kanserin Sömürdüğü Bir Hücre Tutamağı
Hücrelerimiz, çevrelerine tutunmak ve mekanik ile kimyasal ipuçlarını algılamak için integrin adı verilen protein “tutamaçları” kullanır. αvβ3 adındaki belirli bir integrin, hücrelerin çevrelerine yanıt vermesine yardımcı olur ve yeni kan damarlarının büyümesi, tümör genişlemesi, kanser hücrelerinin yayılımı ve ilaç direnci gibi süreçlerde önemli rol oynar. Bu nedenle αvβ3, yıllardır anti-kanser ve anti-anjiyojenik ilaç hedefi olmuştur. Ancak onlarca yıllık çalışmalar insan kullanımı için onaylanmış bir αvβ3 inhibitörü üretememiştir; bunun nedenlerinden biri de farklı moleküllerin bu reseptöre nasıl bağlanıp onu nasıl kontrol ettiğini tam olarak anlamanın zor olmasıdır.
Yılan Zehri Molekülleri Neden Bu Kadar Güçlü?
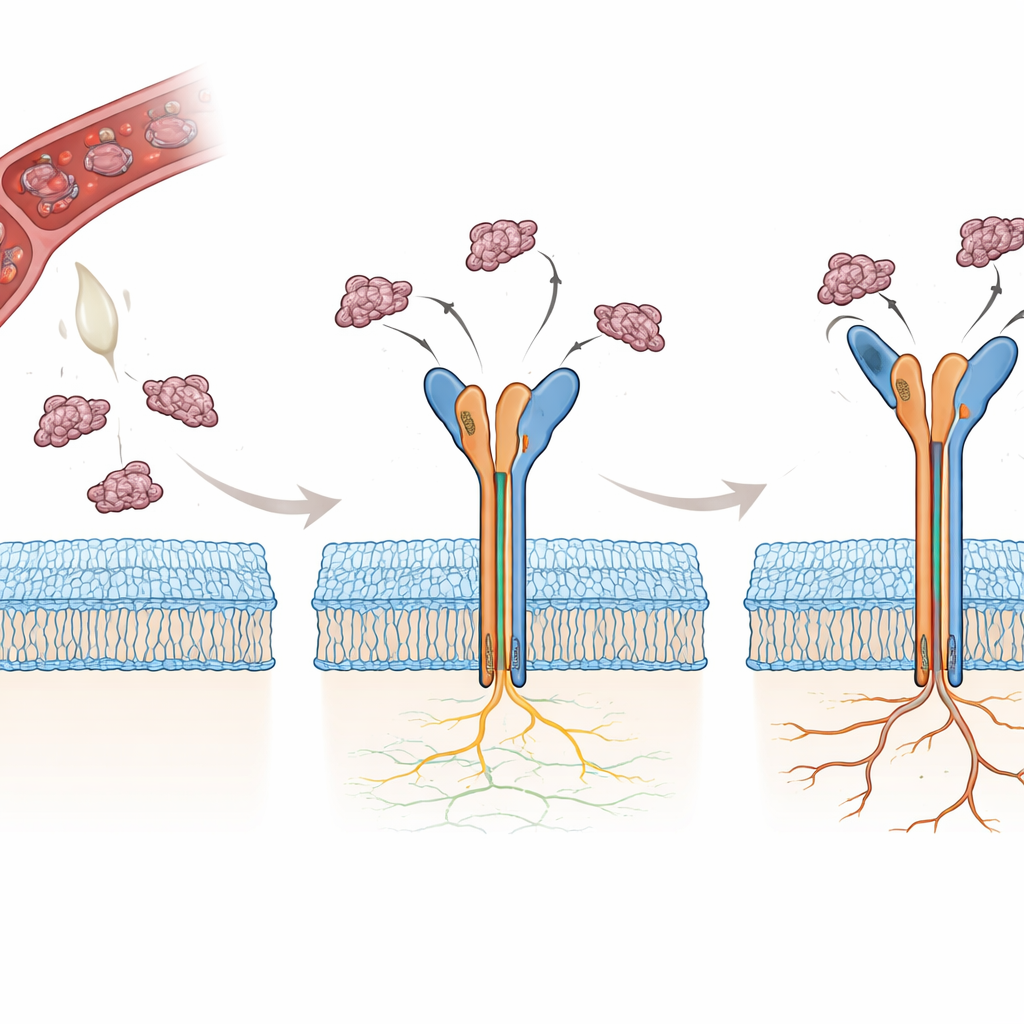
Birçok yılan, integrinleri doğal olarak bloke eden ve kanın pıhtılaşmasını engelleyen ile hücre adezyonunu bozan küçük proteinler olan disintegrinleri üretir. Bu disintegrinlerden ikisi, rhodostomin (Rho) ve trimucrin (Tmu), αvβ3 tarafından tanınan üç amino asitlik kısa bir diziyi—arginin-glisin-aspartat yani RGD—içerir. İlginç bir şekilde, Tmu Rho’ya kıyasla bu integrini kapatmada yaklaşık üç ila dört kat daha etkilidir. İki molekül dizilerinin çoğunu paylaşır ancak kısa bir bağlayıcı, esnek RGD içeren halka ve proteinin kuyruk ucu olmak üzere üç önemli bölgede farklılık gösterirler. Yazarlar, bu küçük farklılıkların her bir zehir proteininin αvβ3’e nasıl tutunduğunu ve neden Tmu’yu daha güçlü bir inhibitör yaptığını atom atom belirlemeyi amaçladılar.
Yapıları Yüksek Ayrıntıda Yakalamak
Bu soruları yanıtlamak için araştırmacılar önce Tmu’nun yalnız halinin kristal yapısını çok yüksek çözünürlükte çözdüler ve altı disülfid bağı ile stabilize edilmiş kompakt, rijit bir çerçeve oluşturduğunu doğruladılar. Ardından kriyo-elektron mikroskopisi kullanarak αvβ3’ün ya Rho ya da Tmu’ya bağlı üç boyutlu yapısını belirlediler ve bağlanmanın gerçekleştiği reseptör başı için üç angstremden daha iyi çözünürlüklere ulaştılar. Her iki durumda da disintegrin, integrin başının iki domaini arasındaki bir yarığa oturuyor ve RGD halkasını metal içeren bir siteye sokuyordu. Bu bölgede Rho ile Tmu’nun iskelet şekli neredeyse özdeşti; bu, her iki proteinin de reseptöre bağlanırken büyük yeniden düzenlemeler geçirmek yerine bağlanmaya hazır ön-oluşumlu bir şekle sahip olduğunu gösteriyor.
Üç Temas Bölgesi ve Daha Güçlü Bir Mengeney
Daha yakından incelendiğinde bağlanmanın yalnızca RGD üçlüsüyle yönetilmediği görüldü. Her iki disintegrin üç işbirlikçi temas bölgesi kullanır: RGD halkası; yakınlardaki bir bağlayıcı bölge; ve C-terminal kuyruk. Tmu’da bağlayıcıdaki pozitif yüklü amino asit kümesi, β3 alt biriminin negatif yüklü yüzeyiyle ek elektrostatik temaslar kurarak αvβ3’e daha sıkı bir şekilde klemplemesine yardımcı olur. Buna karşılık Rho, ekstra temaslar için daha çok kuyruk bölgesine dayanır. Araştırmacılar iki zehir proteini arasında belirli dizi segmentlerini değiştirdiklerinde, engelleme gücünü artırıp azaltabildiler. Özellikle Tmu’nun yüklü bağlayıcısını Rho’ya aktarmak, Rho’nun αvβ3’ü inhibe etme yeteneğini yaklaşık on kat artırdı; bu da bu ekstra bağlanma yamasının etkinliğin önemli bir katkısı olduğunu doğruluyor.
Bağlanma Reseptörü Nasıl Açığa Çıkarır — ve Tek Bir Atomun Önemi
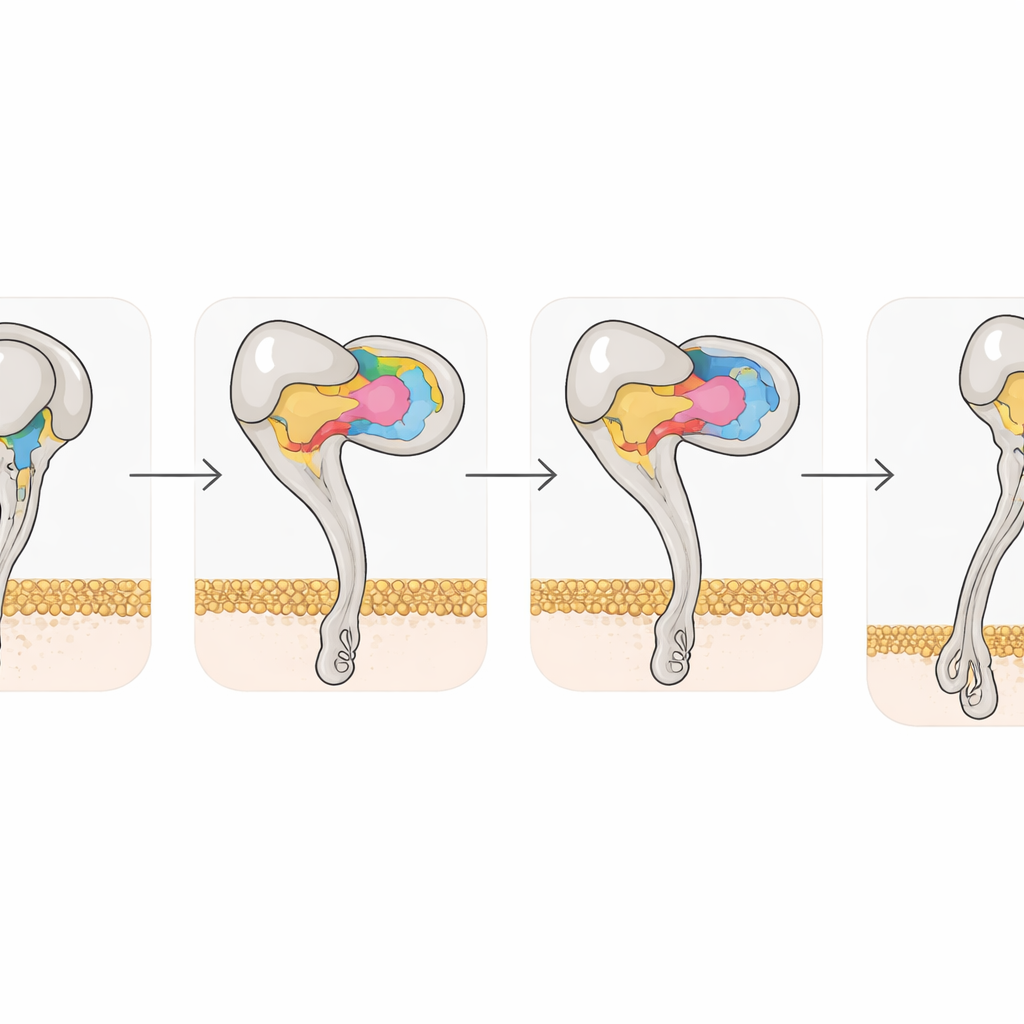
Yapısal anlık görüntüler ayrıca disintegrin bağlanmasının integrini nasıl yeniden şekillendirdiğini yakaladı. Serbest αvβ3, bükülmüş, kapalı bir duruşu tercih eder; Rho ya da Tmu bağlandığında, reseptörün β3 yarısı iki heliks ve metal bağlayan bölgelerde koordineli kaymalar geçirerek reseptörü yüksek aktiviteyle ilişkilendirilen tamamen uzanmış, açık bir duruma iter. Yine de β3’teki tirozin 110 adlı tek bir amino asit, iki domaini köprüleyerek bükülmüş formu bir arada tutmaya yardımcı olur. Araştırmacılar bu kalıntıyı alanin ile değiştirdiklerinde, reseptör kendiliğinden uzanmış durumu daha çok tercih etti ve doğal bağdaşığı vitronektine daha sıkı bağlandı. Bu, ince atomik değişikliklerin integrin aktivasyonunu nasıl ayarlayabileceğini vurgular ve mühendislik varyantlarının yeni ilaçların taranmasında yararlı araçlar olabileceğini öne sürer.
Zehir İpuçlarından Geleceğin Kanser İlaçlarına
Toplanan bulgular, orta büyüklükteki zehir disintegrinlerinin αvβ3’ü hedeflemek için üç koordineli temas bölgesi ve rijit bir bağlanma halkası kullanarak basit RGD-tabanlı moleküllerden daha iyi performans gösteren çok verimli bir iskelet sağladığını gösteriyor. Tmu ve Rho’nun reseptörü tam olarak nasıl yakaladığını ve küçük dizi değişikliklerinin bu etkileşimi nasıl değiştirdiğini haritalayarak, çalışma αvβ3’e daha seçici ve kanama ya da diğer yan etkiler yapma olasılığı daha düşük olan yeni nesil integrin engelleyiciler tasarlamak için yapısal bir plan sunuyor. Özetle, yılanların hücre adezyon mekanizmamızı son derece hassas bir şekilde nasıl devre dışı bıraktığını öğrenerek, bilim insanları bu doğal silahları kansere ve iltihabi hastalıklara karşı hedefe yönelik tedavilere dönüştürme konusunda yeni fikirler kazanıyor.
Atıf: Wang, YT., Chang, YT., Huang, CH. et al. Structural basis for the differential recognition of integrin αvβ3 by rhodostomin and trimucrin. Commun Biol 9, 583 (2026). https://doi.org/10.1038/s42003-026-10139-6
Anahtar kelimeler: integrin alfa v beta 3, yılan zehri disintegrinleri, rhodostomin trimucrin, kanser ve anjiyogenez, kriyoolgun elektron mikroskopisi