Clear Sky Science · sv
Strukturell grund för den differentierade igenkänningen av integrin αvβ3 av rhodostomin och trimucrin
Giftproteiner förvandlade till precisionsmedicinska verktyg
Ormgift låter kanske som ren förgiftning, men några av dess molekyler är anmärkningsvärt bra på att blockera sjukdomsrelaterade proteiner i våra kroppar. Denna studie undersöker hur två sådana molekyler, härledda från gift, hakar fast vid en nyckelreceptor på cellytan kopplad till cancer och blodkärlstillväxt och avslöjar atomdetaljer som kan vägleda utformningen av säkrare, mer precisa läkemedel.
Ett cellgrepp som cancer lärt sig utnyttja
Våra celler använder protein"grepp" kallade integriner för att fästa vid omgivningen och för att känna mekaniska och kemiska signaler. Ett särskilt integrin, kallat αvβ3, hjälper celler att reagera på sin miljö och spelar en huvudroll i nybildning av blodkärl, tumörtillväxt, spridning av cancerceller och läkemedelsresistens. Därför har αvβ3 länge varit ett mål för anticancer- och anti-angiogena läkemedel. Men årtionden av arbete har inte resulterat i godkända αvβ3-hämmare för mänskligt bruk, delvis eftersom det varit svårt att förstå exakt hur olika molekyler binder till och kontrollerar denna receptor.
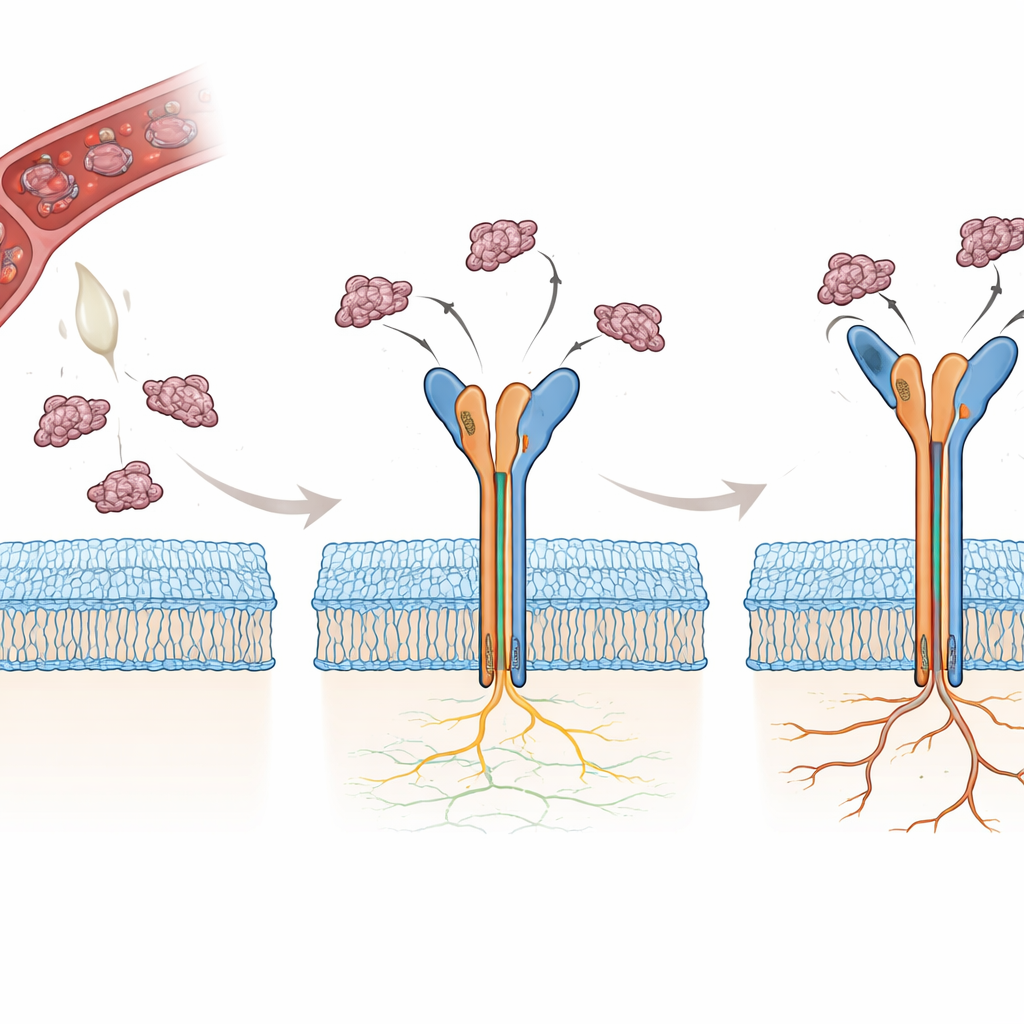
Varför ormgiftmolekyler är så potenta
Många ormar producerar små proteiner kallade disintegriner som naturligt blockerar integriner, hindrar blodet från att koagulera och stör celladhesion. Två sådana disintegriner, rhodostomin (Rho) och trimucrin (Tmu), innehåller båda en kort sekvens av tre aminosyror—arginin-glycin-asparaginsyra, eller RGD—som känns igen av αvβ3. Överraskande nog är Tmu ungefär tre till fyra gånger bättre än Rho på att stänga av detta integrin. De två molekylerna delar större delen av sin sekvens men skiljer sig i tre nyckelregioner: en kort länksekvens, den flexibla RGD-innehållande loopen och proteinets C-terminala ände. Författarna satte ut för att fastställa, atom för atom, hur dessa små skillnader ändrar sättet varje giftprotein greppar αvβ3 och varför det gör Tmu till en mer kraftfull hämmare.
Fånga strukturerna i hög detalj
För att besvara dessa frågor bestämde forskarna först kristallstrukturen för Tmu ensam med mycket hög upplösning, vilket bekräftade att det bildar ett kompakt, styvt ramverk stabiliserat av sex disulfidbindningar. De använde sedan kryogen elektronmikroskopi för att bestämma tredimensionella strukturer av αvβ3 bundet till antingen Rho eller Tmu, och nådde upplösningar under tre ångström för receptorhuvudet där bindningen sker. I båda fallen sitter disintegrinen i en fåra mellan två domäner i integrinhuvudet och för in sin RGD-loop i en metallinnehållande plats. Ryggradsformen hos Rho och Tmu i detta område är nästan identisk, vilket visar att båda proteinerna anländer förformade i en bindningsklar konformation snarare än att behöva genomgå stora omarrangemang vid engagerandet av receptorn.
Tre kontaktzoner och ett starkare klämgrepp
Närmare granskning avslöjade att bindningen inte styrs av RGD-triplet ensam. Båda disintegrinerna använder tre samverkande kontaktzoner: själva RGD-loopen; en närliggande länkregion; och C-terminala svansen. I Tmu gör en klunga positivt laddade aminosyror i länken ytterligare elektrostatisk kontakt med den negativt laddade ytan på β3-subenheten, vilket hjälper den att klämma sig tätare runt αvβ3. Rho, däremot, förlitar sig mer på sin svansregion för extra kontakter. När teamet bytte specifika sekvenssegment mellan de två giftproteinerna kunde de reglera blockeringsstyrkan upp eller ner. Särskilt, genom att föra över Tmus laddade länk till Rho ökades Rhos förmåga att hämma αvβ3 med ungefär tiofaldigt, vilket bekräftar att detta extra bindningsområde är en stor bidragsgivare till potensen.
Hur bindning slår på receptorn—och hur en enda atom betyder
De strukturella ögonblicksbilderna fångade också hur disintegrinbindning omformar själva integrinet. Fritt αvβ3 föredrar en böjd, sluten hållning; när Rho eller Tmu binder genomgår β3-halvan av receptorn koordinerade skift i två helixar och metallbindande platser, vilket driver receptorn till ett fullständigt utsträckt, öppet tillstånd som associeras med hög aktivitet. Ändå hjälper en enda aminosyra, tyrosin 110 i β3, till att hålla ihop den böjda formen genom att bilda en brygga mellan två domäner. När forskarna muterade denna rest till alanin föredrog receptorn spontant det utsträckta tillståndet och band starkare till sin naturliga partner, vitronektin. Detta belyser hur subtila atomära förändringar kan finjustera integrinaktivering och antyder att konstruerade varianter kan vara användbara verktyg för att screena nya läkemedel.
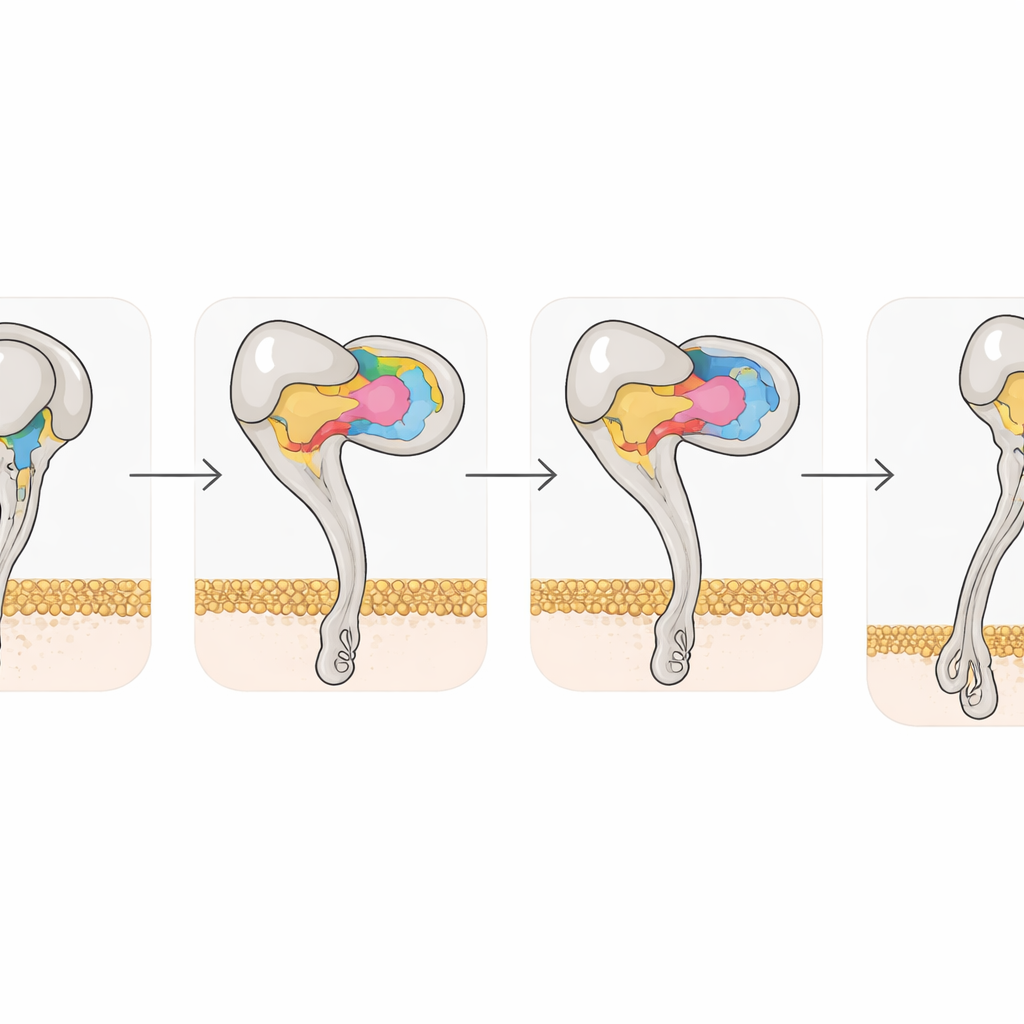
Från giftledtrådar till framtida cancerläkemedel
Tillsammans visar arbetet att medelstora giftdisintegriner erbjuder ett mycket effektivt ramverk för att rikta in sig på αvβ3, genom att använda tre samordnade kontaktregioner och en styv bindningsloop för att överträffa enkla RGD-baserade molekyler. Genom att kartlägga exakt hur Tmu och Rho engagerar receptorn—och hur små sekvensförändringar ändrar detta engagemang—erbjuder studien en strukturell ritning för att designa nästa generations integrinhämmare som är mer selektiva för αvβ3 och mindre benägna att orsaka blödning eller andra biverkningar. I huvudsak, genom att lära sig hur ormar inaktiverar vår celladhesionsapparat med utsökt precision, får forskare nya idéer för att förvandla dessa naturliga vapen till riktade terapier mot cancer och inflammatoriska sjukdomar.
Citering: Wang, YT., Chang, YT., Huang, CH. et al. Structural basis for the differential recognition of integrin αvβ3 by rhodostomin and trimucrin. Commun Biol 9, 583 (2026). https://doi.org/10.1038/s42003-026-10139-6
Nyckelord: integrin alpha v beta 3, ormgiftets disintegriner, rhodostomin trimucrin, cancer och angiogenes, kryo-elektronmikroskopi