Clear Sky Science · ru
Структурные основы дифференциального распознавания интегрина αvβ3 родостомином и тримукрином
Белки яда, превращённые в инструменты точной медицины
Змеиный яд звучит как чистый яд, но некоторые его молекулы удивительно хорошо блокируют белки, вовлечённые в болезни в нашем организме. В этом исследовании изучают, как две такие производные яда молекулы прикрепляются к ключевому рецептору на поверхности клеток, связанному с раком и ростом кровеносных сосудов, раскрывая атомные детали, которые могут направлять разработку более безопасных и точных препаратов.
Клеточная «хваталка», которой пользуется рак
Наши клетки используют белковые «хватки», называемые интегринами, чтобы прикрепляться к окружению и воспринимать механические и химические сигналы. Один из интегринов, обозначаемый αvβ3, помогает клеткам реагировать на среду и играет ключевую роль в росте новых сосудов, увеличении опухолей, распространении раковых клеток и устойчивости к лекарствам. Именно поэтому αvβ3 долгое время был мишенью для антираковых и антиангиогенных препаратов. Однако десятилетия работы пока не привели к одобренным блокаторам αvβ3 для человека — отчасти потому, что было трудно точно понять, как разные молекулы связываются с этим рецептором и управляют его функцией.
Почему молекулы змеиного яда так эффективны
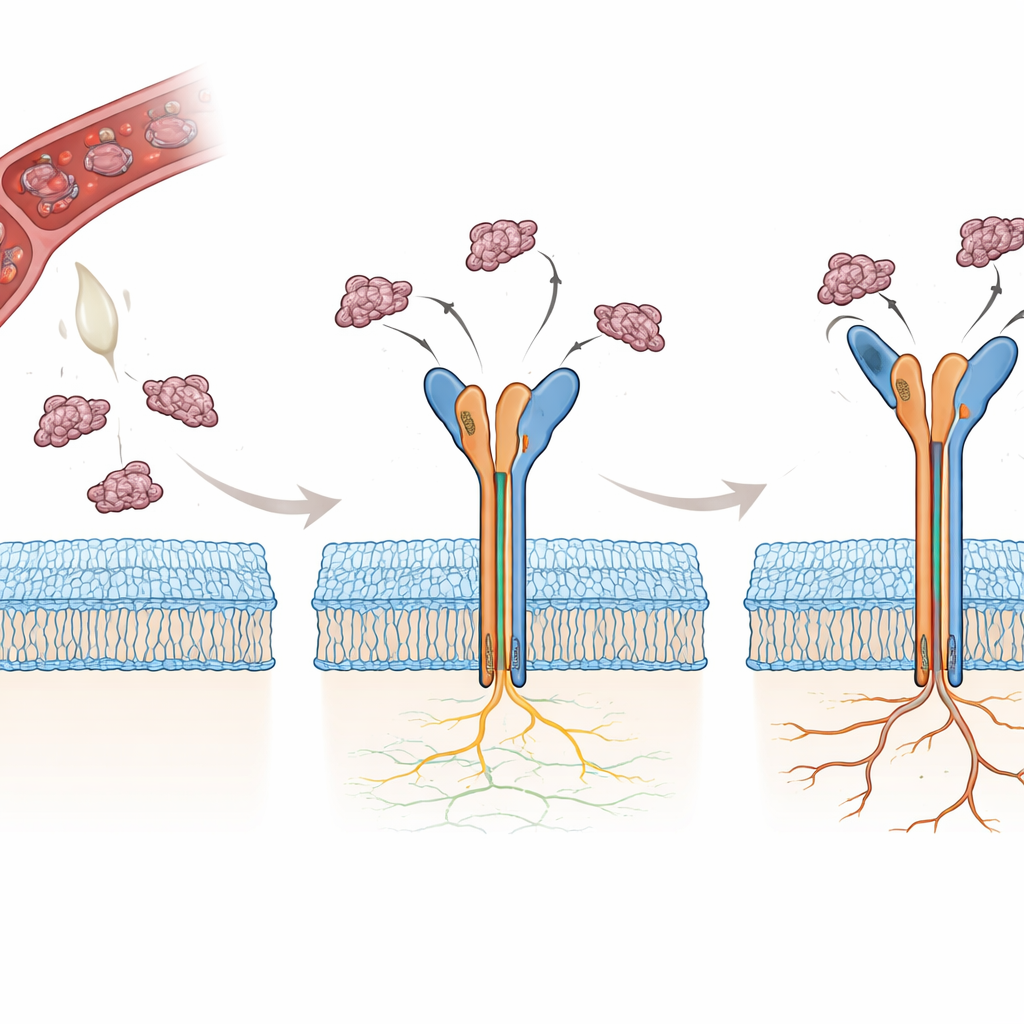
Многие змеи производят небольшие белки, называемые дизинтринами, которые естественно блокируют интегрины, препятствуя свертыванию крови и нарушая клеточную адгезию. Два таких дизинтрина, родостомин (Rho) и тримукрин (Tmu), содержат короткую последовательность из трёх аминокислот — аргинин-глицин-аспартат, или RGD — которую распознаёт αvβ3. Удивительно, но Tmu примерно в три–четыре раза эффективнее, чем Rho, в подавлении этого интегрина. Эти две молекулы имеют общую большую часть последовательности, но отличаются в трёх ключевых участках: коротком линкере, гибкой петле, содержащей RGD, и хвостовом конце белка. Авторы стремились определить, атом за атомом, как эти небольшие различия меняют способ захвата αvβ3 каждой молекулой и почему Tmu оказывается более мощным ингибитором.
Запечатление структур в высоком разрешении
Чтобы ответить на эти вопросы, исследователи сначала определили кристаллическую структуру Tmu в высоком разрешении, подтвердив, что она формирует компактную жёсткую рамку, стабилизированную шестью дисульфидными связями. Затем они использовали криогенную электронную микроскопию, чтобы получить трёхмерные структуры αvβ3 в комплексе либо с Rho, либо с Tmu, достигнув разрешения ниже трёх ангстрем в области «головы» рецептора, где происходит связывание. В обоих случаях дизинтрин располагается в углублении между двумя доменами головки интегрина, вводя свою RGD-петлю в участки, содержащие металл. Конформция основной цепи Rho и Tmu в этой области почти идентична, что показывает: обе молекулы приходят в связующую форму уже заранее, а не подвергаются крупным перестройкам при взаимодействии с рецептором.
Три зоны контакта и более плотный зажим
Более пристальное рассмотрение показало, что связывание определяется не только триплетом RGD. Оба дизинтрина используют три кооперативные зоны контакта: сама RGD-петля; соседний линкер; и С-концевой хвост. В Tmu кластер положительно заряженных аминокислот в линкере устанавливает дополнительные электростатические контакты с отрицательно заряженной поверхностью субъединицы β3, помогая плотнее «зажать» αvβ3. В отличие от этого, Rho больше полагается на свою хвостовую область для дополнительных контактов. Когда команда меняла определённые фрагменты последовательности между двумя белками яда, они могли ослаблять или усиливать блокирующую способность. В частности, перенос заряженного линкера Tmu в Rho повысил способность Rho ингибировать αvβ3 примерно в десять раз, подтвердив, что эта дополнительная зона связывания является основным фактором мощности.
Как связывание переключает рецептор — и как важна одна атомная деталь
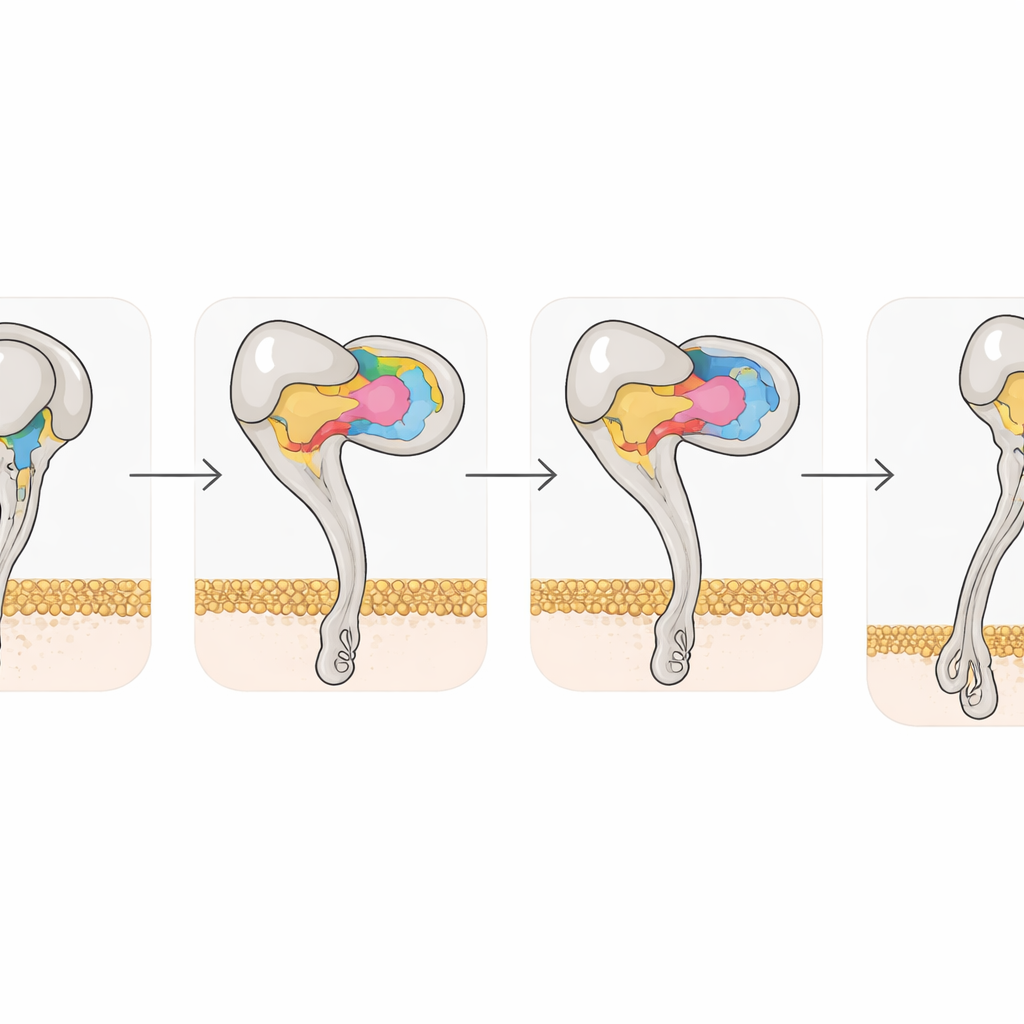
Структурные снимки также запечатлели, как связывание дизинтрина изменяет сам интегрин. Свободный αvβ3 предпочитает согнутую, закрытую конформацию; после связывания Rho или Tmu половинка рецептора β3 претерпевает скоординированные сдвиги в двух спиралях и участках связывания металлов, переводя рецептор в полностью вытянутое, открытое состояние, связанное с высокой активностью. В то же время одна аминокислота — тирозин 110 в β3 — помогает удерживать согнутую форму, связывая два домена. Когда исследователи мутировали этот остаток в аланин, рецептор спонтанно смещался в сторону вытянутого состояния и сильнее связывался со своим естественным партнёром, витронектином. Это подчёркивает, как тонкие атомные изменения могут настраивать активацию интегринов и предполагает, что инженерные варианты могут служить полезными инструментами для скрининга новых препаратов.
От подсказок в яде к будущим противораковым препаратам
В целом работа показывает, что средних размеров дизинтрины яда являются высокоэффективным каркасом для нацеливания на αvβ3, используя три скоординированные зоны контакта и жёсткую связывающую петлю, чтобы превосходить простые RGD-основанные молекулы. Точная карта того, как Tmu и Rho взаимодействуют с рецептором — и как небольшие изменения последовательности меняют это взаимодействие — предлагает структурный план для разработки следующего поколения блокаторов интегринов, более селективных к αvβ3 и менее склонных вызывать кровотечения или другие побочные эффекты. По сути, изучая, как змеи с поразительной точностью отключают нашу систему клеточной адгезии, учёные получают новые идеи о том, как превратить эти природные «оружия» в целевые терапии против рака и воспалительных заболеваний.
Цитирование: Wang, YT., Chang, YT., Huang, CH. et al. Structural basis for the differential recognition of integrin αvβ3 by rhodostomin and trimucrin. Commun Biol 9, 583 (2026). https://doi.org/10.1038/s42003-026-10139-6
Ключевые слова: интегрин альфа v бета 3, дизинтрины змеиного яда, родостомин тримукрин, рак и ангиогенез, криоэлектронная микроскопия