Clear Sky Science · pl
Podstawa strukturalna różnicowego rozpoznawania integryny αvβ3 przez rhodostominę i trimukrynę
Białka jadowe przekształcone w narzędzia precyzyjnej medycyny
Jad węża brzmi jak czysta trucizna, ale niektóre jego molekuły doskonale blokują białka związane z chorobami w naszych organizmach. W tym badaniu zbadano, jak dwa takie związki pochodzące z jadu wiążą się z kluczowym receptorem powierzchniowym związanym z rakiem i wzrostem naczyń krwionośnych, ujawniając szczegóły na poziomie atomowym, które mogą poprowadzić projektowanie bezpieczniejszych, bardziej precyzyjnych leków.
Uchwyt komórkowy, którego uczy się wykorzystywać rak
Nasze komórki korzystają z białkowych „uchwytów” zwanych integrynami, by przyłączać się do otoczenia i wyczuwać sygnały mechaniczne oraz chemiczne. Jedna integryna, oznaczana jako αvβ3, pomaga komórkom reagować na środowisko i odgrywa istotną rolę w tworzeniu nowych naczyń, rozwoju guza, rozsiewie komórek nowotworowych oraz oporności na leki. Z tego powodu αvβ3 od dawna stanowi cel terapii przeciwnowotworowych i antyangiogennych. Mimo dekad badań nie powstał however zatwierdzony inhibitor αvβ3 do stosowania u ludzi, częściowo dlatego, że trudno było dokładnie zrozumieć, jak różne molekuły wiążą i regulują ten receptor.
Dlaczego molekuły jadu węży są tak silne
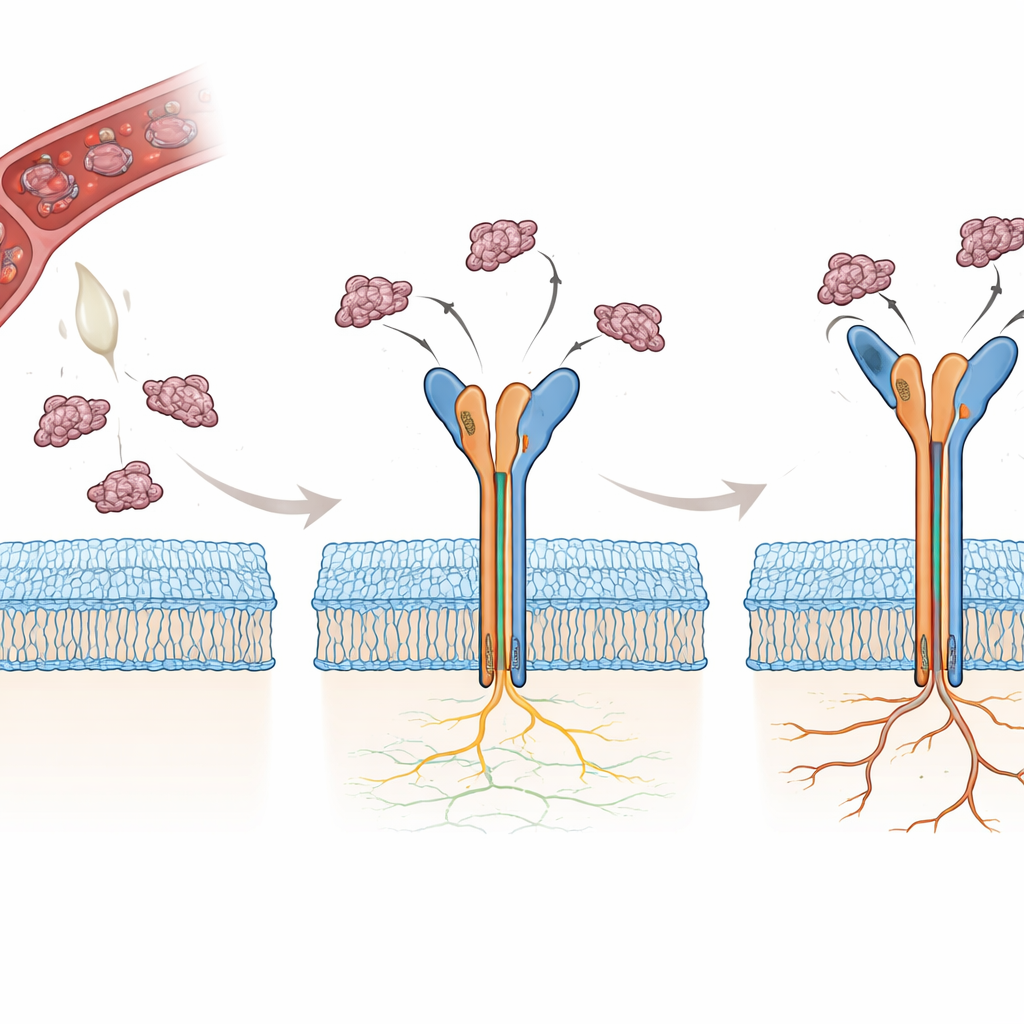
Wiele węży wytwarza niewielkie białka zwane disintegrynami, które naturalnie blokują integryny, zapobiegając krzepnięciu krwi i zakłócając adhezję komórek. Dwie takie disintegryny, rhodostomina (Rho) i trimukryna (Tmu), zawierają krótką sekwencję trzech aminokwasów — arginina-glicyna-kwas asparaginowy, czyli RGD — rozpoznawaną przez αvβ3. Co zaskakujące, Tmu jest około trzy- -czterokrotnie skuteczniejsza od Rho w hamowaniu tej integryny. Obie molekuły mają podobną sekwencję, ale różnią się w trzech kluczowych obszarach: krótkim łączniku, elastycznej pętli zawierającej RGD oraz końcówce C- -terminalnej białka. Autorzy postanowili ustalić, atom po atomie, jak te niewielkie różnice zmieniają sposób, w jaki każde z białek jadowych chwyta αvβ3 i dlaczego Tmu jest silniejszym inhibitorem.
Uchwycenie struktur w wysokiej rozdzielczości
Aby odpowiedzieć na te pytania, badacze najpierw wyznaczyli strukturę krystaliczną Tmu w bardzo wysokiej rozdzielczości, potwierdzając, że tworzy zwarte, sztywne rusztowanie stabilizowane przez sześć mostków disiarczkowych. Następnie użyli kriogenicznej mikroskopii elektronowej, by określić trójwymiarowe struktury αvβ3 związanej albo z Rho, albo z Tmu, osiągając rozdzielczości poniżej trzech angstremów dla części głowowej receptora, gdzie zachodzi wiązanie. W obu przypadkach disintegryna siedzi w szczelinie między dwoma domenami głowy integryny, wkładając swoją pętlę RGD w miejsce zawierające metal. Szkieletowy kształt Rho i Tmu w tym obszarze jest niemal identyczny, co pokazuje, że oba białka są z góry ukształtowane w formę gotową do wiązania, zamiast przechodzić duże przearanżowania podczas angażowania receptora.
Trzy strefy kontaktu i silniejszy zacisk
Bliższa analiza ujawniła, że wiązanie nie jest rządzone wyłącznie przez triplet RGD. Obie disintegryny wykorzystują trzy współdziałające strefy kontaktu: samą pętlę RGD; pobliski region łącznika; oraz ogon C-terminalny. W Tmu skupisko dodatnio naładowanych aminokwasów w łączniku tworzy dodatkowe kontakty elektrostatyczne z ujemnie naładowaną powierzchnią podjednostki β3, co pomaga zacisnąć się mocniej na αvβ3. Rho, przeciwnie, polega bardziej na swojej końcówce dla dodatkowych kontaktów. Gdy zespół podmienił konkretne fragmenty sekwencji między obiema disintegrynami, mogli stopniować siłę blokowania. W szczególności przeniesienie naładowanego łącznika Tmu do Rho zwiększyło zdolność Rho do hamowania αvβ3 około dziesięciokrotnie, potwierdzając, że ta dodatkowa płaszczyzna wiązania jest głównym czynnikiem mocy działania.
Jak wiązanie przełącza receptor — i jak jednemu atomowi przypada znaczenie
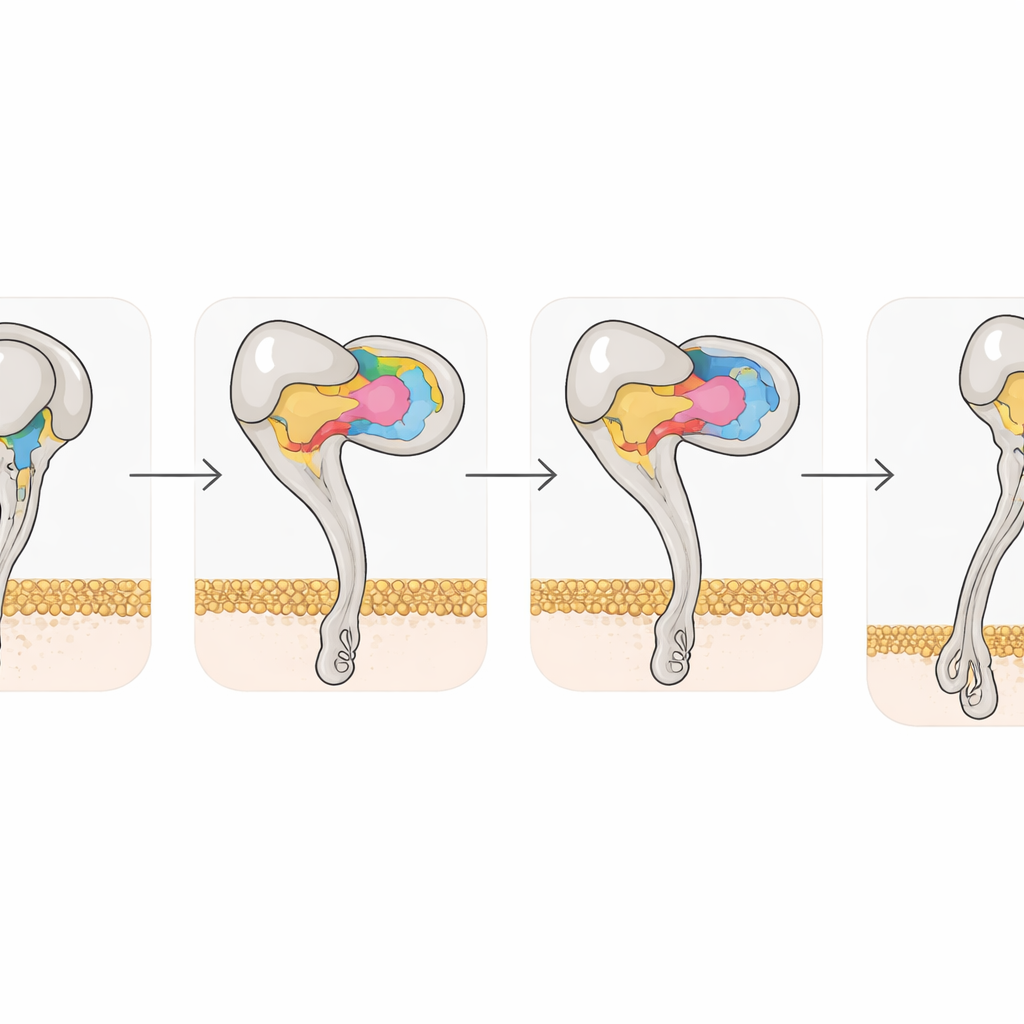
Ujęcia strukturalne uchwyciły także, jak wiązanie disintegryn przeobraża samą integrynę. Wolna αvβ3 preferuje zgiętą, zamkniętą konfigurację; kiedy Rho lub Tmu się wiążą, połowa receptora z β3 przechodzi skoordynowane przesunięcia w dwóch helisach i miejscach wiążących metale, przekształcając receptor w całkowicie wydłużony, otwarty stan związany z wysoką aktywnością. Jednak pojedynczy aminokwas, tyrozyna 110 w β3, pomaga utrzymać formę zgiętą, łącząc dwie domeny. Gdy badacze zmienili ten rezyduum na alaninę, receptor spontanicznie preferował stan wydłużony i silniej wiązał swojego naturalnego partnera, witronektynę. To podkreśla, jak subtelne zmiany atomowe mogą dostroić aktywację integryny i sugeruje, że zmodyfikowane warianty mogłyby posłużyć jako przydatne narzędzia do przesiewania nowych leków.
Od wskazówek z jadu do przyszłych leków przeciwnowotworowych
Podsumowując, praca pokazuje, że średniej wielkości disintegryny jadowe stanowią wysoce wydajne rusztowanie do celowania w αvβ3, wykorzystując trzy skoordynowane regiony kontaktowe i sztywną pętlę wiążącą, by przewyższać proste molekuły oparte na RGD. Mapując dokładnie, jak Tmu i Rho angażują receptor — i jak małe zmiany sekwencji modyfikują to angażowanie — badanie dostarcza strukturalnego planu do projektowania następnej generacji blokerów integryn, które będą bardziej selektywne wobec αvβ3 i mniej skłonne wywoływać krwawienia lub inne skutki uboczne. W istocie, ucząc się, jak węże precyzyjnie unieruchamiają nasz mechanizm adhezji komórek, naukowcy zyskują nowe pomysły na przekształcanie tych naturalnych „broni” w celowane terapie przeciw rakowi i chorobom zapalnym.
Cytowanie: Wang, YT., Chang, YT., Huang, CH. et al. Structural basis for the differential recognition of integrin αvβ3 by rhodostomin and trimucrin. Commun Biol 9, 583 (2026). https://doi.org/10.1038/s42003-026-10139-6
Słowa kluczowe: integryna alfa v beta 3, disintegryny jadu węży, rhodostomina trimukryna, rak i angiogeneza, kriomikroskopia elektronowa