Clear Sky Science · pt
Base estrutural para o reconhecimento diferencial da integrina αvβ3 por rhodostomina e trimucrina
Proteínas do veneno transformadas em ferramentas de medicina de precisão
Veneno de serpente pode soar como puro veneno, mas algumas de suas moléculas são excepcionalmente eficazes em bloquear proteínas associadas a doenças em nosso corpo. Este estudo explora como duas dessas moléculas derivadas do veneno se ligam a um receptor de superfície celular chave, relacionado ao câncer e ao crescimento de vasos sanguíneos, revelando detalhes em nível atômico que podem orientar o desenho de medicamentos mais seguros e precisos.
Uma aderência celular que o câncer aprende a explorar
Nossas células usam “garras” proteicas chamadas integrinas para se prender ao entorno e perceber sinais mecânicos e químicos. Uma integrina em particular, chamada αvβ3, ajuda as células a responder ao ambiente e desempenha papel importante no crescimento de novos vasos sanguíneos, expansão tumoral, disseminação de células cancerígenas e resistência a drogas. Por isso, a αvβ3 tem sido um alvo de longa data para fármacos anticâncer e antiangiogênicos. Ainda assim, décadas de trabalho não produziram bloqueadores de αvβ3 aprovados para uso humano, em parte porque tem sido difícil compreender exatamente como diferentes moléculas se ligam e modulam esse receptor.
Por que as moléculas do veneno são tão potentes
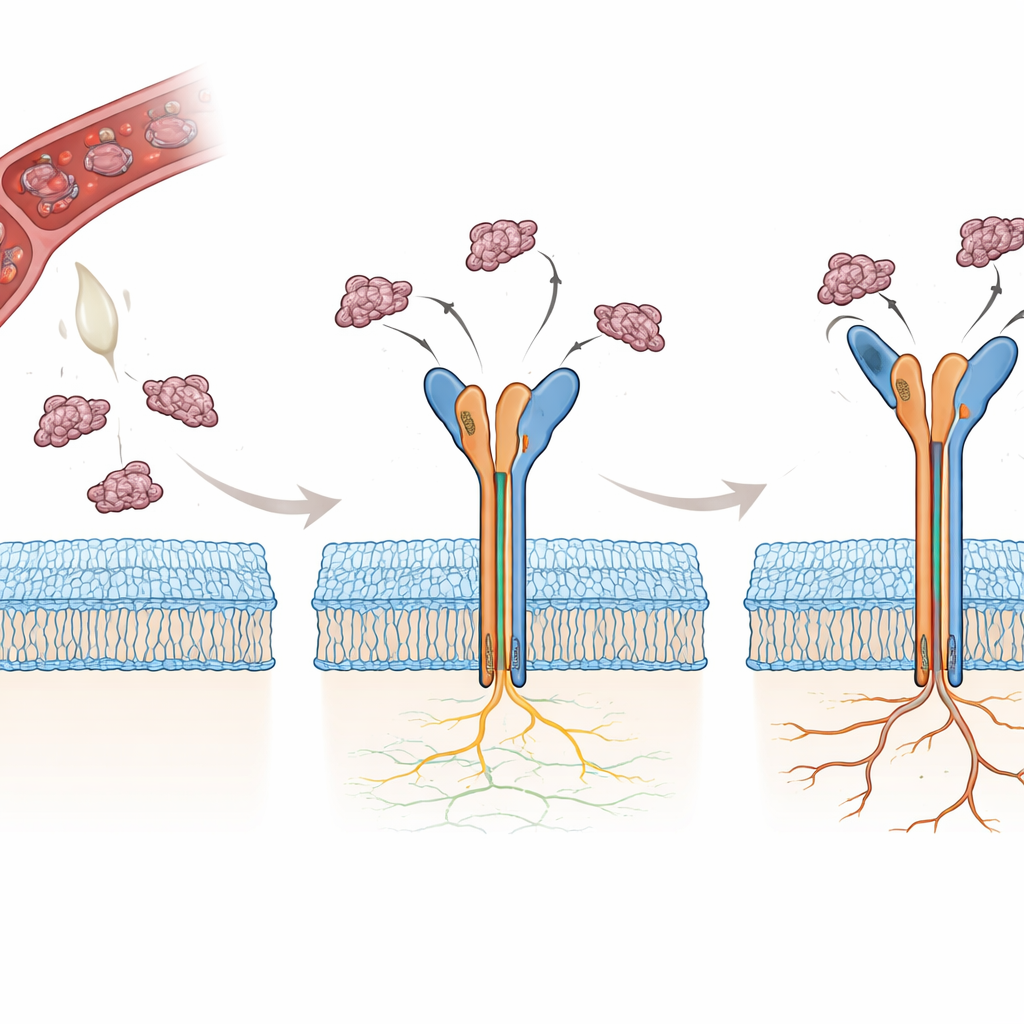
Muitas serpentes produzem pequenas proteínas chamadas disintegrinas que bloqueiam integrinas de forma natural, impedindo a coagulação do sangue e interferindo na adesão celular. Duas dessas disintegrinas, rhodostomina (Rho) e trimucrina (Tmu), contêm ambas uma curta sequência de três aminoácidos — arginina-glicina-ácido aspártico, ou RGD — que é reconhecida por αvβ3. Surpreendentemente, Tmu é cerca de três a quatro vezes mais eficaz que Rho em desativar essa integrina. As duas moléculas compartilham a maior parte de sua sequência, mas diferem em três regiões-chave: um pequeno conector (linker), o laço flexível que contém o RGD e a extremidade C-terminal da proteína. Os autores buscaram determinar, átomo por átomo, como essas pequenas diferenças alteram a forma como cada proteína do veneno agarra αvβ3 e por que isso torna Tmu um inibidor mais potente.
Capturando as estruturas em alta resolução
Para responder a essas perguntas, os pesquisadores primeiro resolveram a estrutura cristalina de Tmu isolada em altíssima resolução, confirmando que ela forma uma estrutura compacta e rígida estabilizada por seis pontes dissulfeto. Em seguida, usaram microscopia eletrônica crio para determinar estruturas tridimensionais de αvβ3 ligado a Rho ou a Tmu, alcançando resoluções abaixo de três angstroms para a cabeça do receptor onde ocorre a ligação. Em ambos os casos, a disintegrina se aloja em uma fenda entre dois domínios da cabeça da integrina, inserindo seu laço RGD em um sítio que contém metal. A conformação da espinha dorsal de Rho e Tmu nessa região é quase idêntica, mostrando que ambas as proteínas chegam pré-formadas em uma forma pronta para se ligar, em vez de sofrer grandes rearranjos ao envolver o receptor.
Três zonas de contato e uma trava mais forte
Inspeção mais detalhada revelou que a ligação não é governada apenas pelo trímero RGD. Ambas as disintegrinas utilizam três zonas de contato cooperativas: o próprio laço RGD; uma região de conector próxima; e a cauda C-terminal. Em Tmu, um aglomerado de aminoácidos carregados positivamente no conector estabelece contatos eletrostáticos adicionais com a superfície negativamente carregada da subunidade β3, ajudando-a a se fechar com mais firmeza sobre αvβ3. Rho, em contraste, depende mais de sua região terminal para contatos extras. Quando a equipe trocou segmentos de sequência específicos entre as duas proteínas do veneno, eles conseguiram ajustar a potência de bloqueio para mais ou para menos. Em particular, transferir o conector carregado de Tmu para Rho aumentou a capacidade de Rho de inibir αvβ3 em aproximadamente dez vezes, confirmando que esse patch adicional de ligação é um contribuinte principal para a potência.
Como a ligação ativa o receptor — e como um único átomo importa
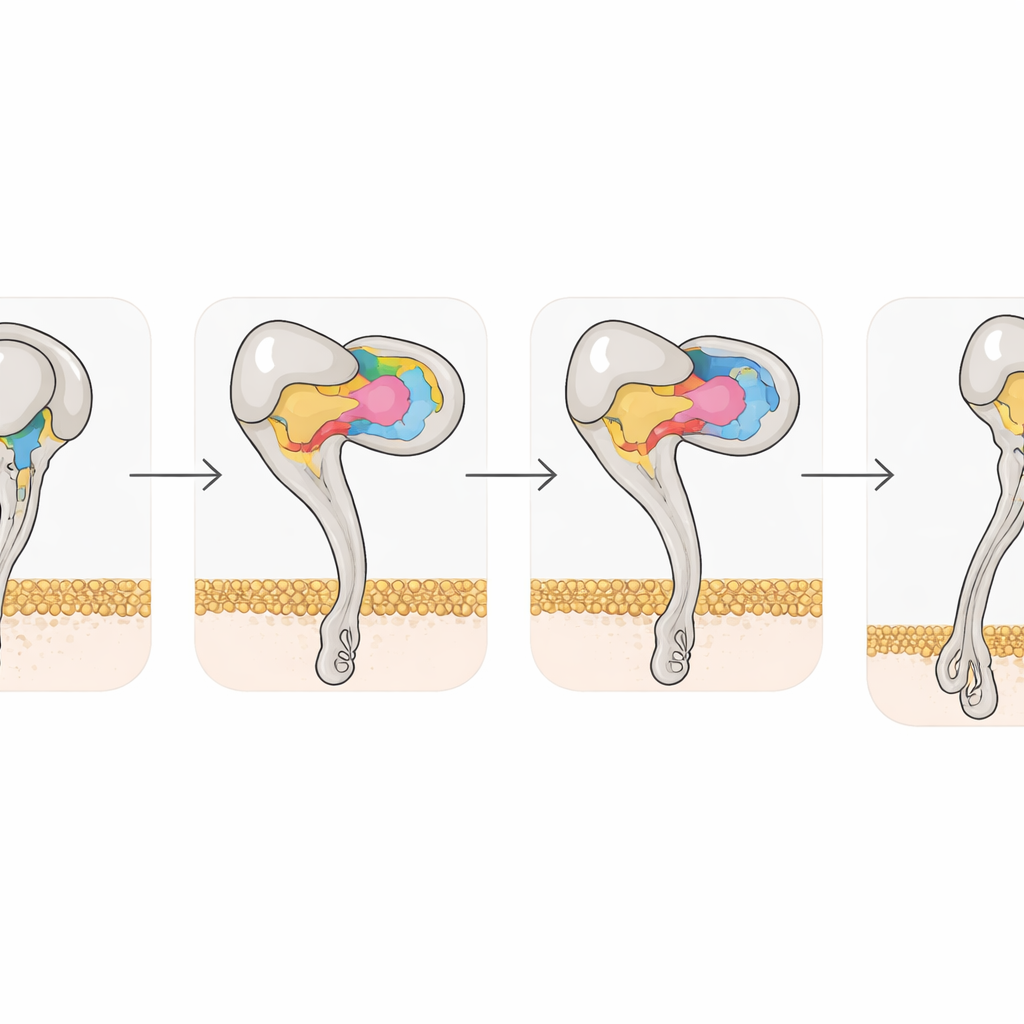
As imagens estruturais também capturaram como a ligação das disintegrinas remodela a própria integrina. A αvβ3 livre prefere uma postura dobrada e fechada; uma vez que Rho ou Tmu se ligam, a metade β3 do receptor sofre deslocamentos coordenados em duas hélices e em sítios de ligação de metal, impulsionando o receptor para um estado totalmente estendido e aberto associado a alta atividade. Ainda assim, um único aminoácido, tirosina 110 em β3, ajuda a manter a forma dobrada unindo dois domínios. Quando os pesquisadores mutaram esse resíduo para alanina, o receptor espontaneamente passou a favorecer o estado estendido e ligou-se mais fortemente ao seu parceiro natural, a vitronectina. Isso destaca como mudanças atômicas sutis podem ajustar a ativação da integrina e sugere que variantes projetadas poderiam ser ferramentas úteis para triagem de novos fármacos.
De pistas do veneno a futuros medicamentos contra o câncer
No conjunto, o trabalho mostra que disintegrinas de tamanho médio do veneno fornecem um andaime altamente eficiente para direcionar αvβ3, usando três regiões de contato coordenadas e um laço de ligação rígido para superar moléculas simples baseadas em RGD. Ao mapear exatamente como Tmu e Rho envolvem o receptor — e como pequenas mudanças de sequência alteram esse envolvimento — o estudo oferece um roteiro estrutural para projetar bloqueadores de integrina de próxima geração que sejam mais seletivos para αvβ3 e menos propensos a causar sangramentos ou outros efeitos colaterais. Em essência, ao aprender como as serpentes desativam nossa máquina de adesão celular com precisão refinada, os cientistas obtêm novas ideias para transformar essas armas naturais em terapias direcionadas contra o câncer e doenças inflamatórias.
Citação: Wang, YT., Chang, YT., Huang, CH. et al. Structural basis for the differential recognition of integrin αvβ3 by rhodostomin and trimucrin. Commun Biol 9, 583 (2026). https://doi.org/10.1038/s42003-026-10139-6
Palavras-chave: integrina alfa v beta 3, disintegrinas de veneno de serpente, rhodostomin trimucrin, câncer e angiogênese, crio-microscopia eletrônica