Clear Sky Science · de
Strukturelle Grundlage für die differentielle Erkennung von Integrin αvβ3 durch Rhodostomin und Trimucrin
Gifte als präzise medizinische Werkzeuge
Schlangengift klingt nach purer Toxizität, doch einige seiner Moleküle blockieren erstaunlich effizient krankheitsrelevante Proteine in unserem Körper. Diese Studie untersucht, wie zwei solche, aus Gift stammende Moleküle an einen wichtigen zellulären Oberflächenrezeptor binden, der mit Krebs und dem Wachstum von Blutgefäßen verknüpft ist, und zeigt atomare Details, die die Entwicklung sichererer, präziserer Wirkstoffe leiten könnten.
Ein Zellgriff, den Krebs auszunutzen lernt
Unsere Zellen verwenden Protein‑„Griffe“, sogenannte Integrine, um sich an ihre Umgebung anzuheften und mechanische sowie chemische Signale wahrzunehmen. Ein spezielles Integrin, αvβ3, hilft Zellen, auf ihre Umwelt zu reagieren, und spielt eine zentrale Rolle beim Neubildung von Blutgefäßen, beim Tumorwachstum, bei der Ausbreitung von Krebszellen und bei Arzneimittelresistenz. Deshalb ist αvβ3 ein langjähriges Ziel für Anti‑Krebs‑ und Anti‑Angiogenese‑Medikamente. Trotzdem hat die jahrzehntelange Forschung bislang keine zugelassenen αvβ3‑Blocker für den Menschen hervorgebracht, was unter anderem daran liegt, dass es schwierig war, genau zu verstehen, wie unterschiedliche Moleküle an diesen Rezeptor binden und ihn steuern.
Warum Moleküle aus Schlangengift so wirksam sind
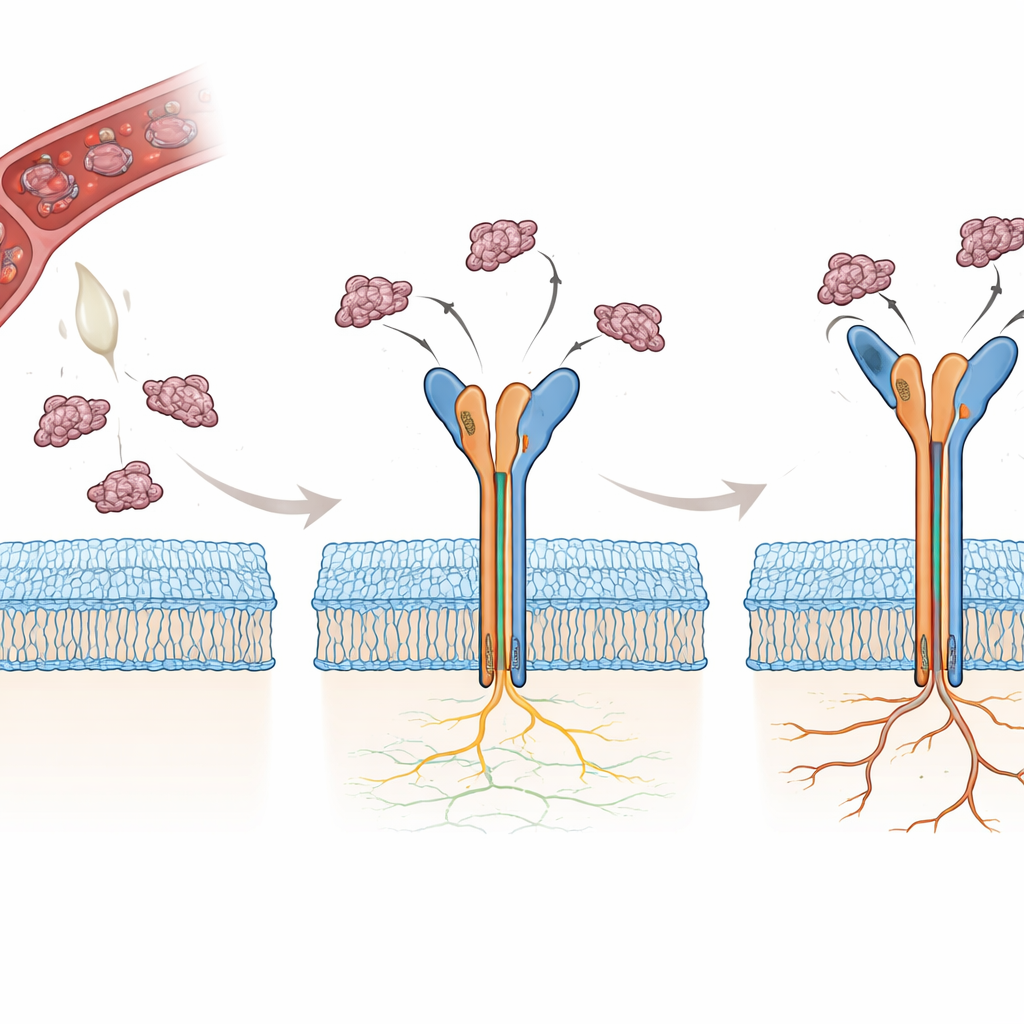
Viele Schlangen produzieren kleine Proteine, sogenannte Disintegrine, die Integrine natürlich blockieren, die Blutgerinnung hemmen und Zelladhäsion stören. Zwei dieser Disintegrine, Rhodostomin (Rho) und Trimucrin (Tmu), enthalten beide eine kurze Sequenz aus drei Aminosäuren – Arginin‑Glycin‑Asparaginsäure, oder RGD – die von αvβ3 erkannt wird. Überraschenderweise ist Tmu etwa drei- bis viermal effektiver als Rho bei der Hemmung dieses Integrins. Die beiden Moleküle teilen den Großteil ihrer Sequenz, unterscheiden sich jedoch in drei Schlüsselregionen: einem kurzen Linker, der flexiblen RGD‑enthaltenden Schleife und dem C‑terminalen Proteinende. Die Autorinnen und Autoren wollten atomgenau aufklären, wie diese kleinen Unterschiede die Art und Weise verändern, wie jedes Giftprotein αvβ3 greift, und warum Tmu ein stärkerer Inhibitor ist.
Die Strukturen in hoher Detailtreue einfangen
Um diese Fragen zu beantworten, lösten die Forschenden zunächst die Kristallstruktur von Tmu allein mit sehr hoher Auflösung und bestätigten, dass es ein kompaktes, steifes Gerüst bildet, das durch sechs Disulfidbrücken stabilisiert wird. Anschließend nutzten sie kryogene Elektronenmikroskopie, um dreidimensionale Strukturen von αvβ3 in Komplex mit entweder Rho oder Tmu zu bestimmen und erreichten dabei Auflösungen unter drei Ångström für den Kopfbereich des Rezeptors, in dem die Bindung stattfindet. In beiden Fällen sitzt das Disintegrin in einer Vertiefung zwischen zwei Domänen des Integrinkopfes und schiebt seine RGD‑Schleife in eine metallhaltige Bindungsstelle. Die Rückgrat‑Konformation von Rho und Tmu in diesem Bereich ist nahezu identisch, was zeigt, dass beide Proteine bereits vorgeformt in einer bindungsbereiten Gestalt vorliegen, statt sich beim Andocken groß umzustrukturieren.
Drei Kontaktzonen und eine stärkere Klammer
Genauere Untersuchungen zeigten, dass die Bindung nicht nur durch das RGD‑Triplett bestimmt wird. Beide Disintegrine nutzen drei kooperative Kontaktzonen: die RGD‑Schleife selbst; eine benachbarte Linker‑Region; und das C‑terminale Ende. Bei Tmu bildet ein Cluster positiv geladener Aminosäuren im Linker zusätzliche elektro-statische Kontakte zur negativ geladenen Oberfläche der β3‑Untereinheit, was ein festeres Zupacken an αvβ3 unterstützt. Rho dagegen stützt sich stärker auf seine Schwanzregion für zusätzliche Kontakte. Als das Team spezifische Sequenzsegmente zwischen den beiden Giftproteinen austauschte, konnten sie die Blockierwirkung steigern oder abschwächen. Insbesondere erhöhte das Einfügen von Tmus geladenem Linker in Rho die Fähigkeit von Rho, αvβ3 zu hemmen, um etwa das Zehnfache, was bestätigt, dass dieser zusätzliche Bindungspatch ein wesentlicher Beitrag zur Wirksamkeit ist.
Wie Bindung den Rezeptor umschaltet — und wie ein einzelnes Atom zählt
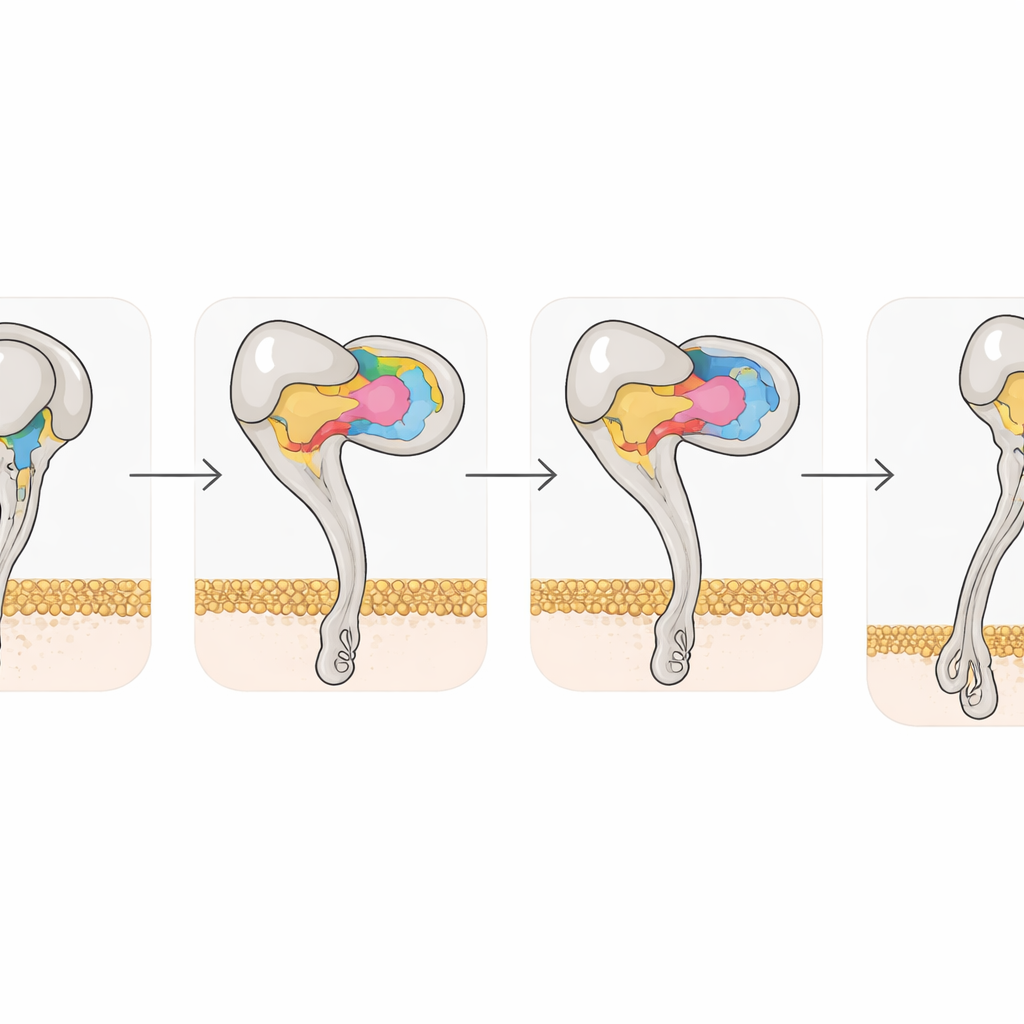
Die strukturellen Momentaufnahmen zeigten auch, wie die Disintegrin‑Bindung das Integrin selbst umformt. Freies αvβ3 bevorzugt eine gekrümmte, geschlossene Konformation; sobald Rho oder Tmu binden, erfährt die β3‑Hälfte des Rezeptors koordinierte Verschiebungen in zwei Helices und in metallbindenden Stellen, die den Rezeptor in einen vollständig gestreckten, offenen Zustand treiben, der mit hoher Aktivität assoziiert ist. Doch eine einzelne Aminosäure, Tyrosin 110 in β3, hilft, die gekrümmte Form durch eine Brücke zwischen zwei Domänen zusammenzuhalten. Wenn die Forschenden diese Position zu Alanin mutierten, bevorzugte der Rezeptor spontan den gestreckten Zustand und band stärker an seinen natürlichen Partner Vitronectin. Das unterstreicht, wie subtile atomare Veränderungen die Integrinaktivierung steuern können, und legt nahe, dass gentechnisch veränderte Varianten nützliche Werkzeuge für das Screening neuer Wirkstoffe sein könnten.
Von Hinweisen aus dem Gift zur zukünftigen Krebstherapie
Insgesamt zeigen die Ergebnisse, dass mittelgroße Disintegrine aus Schlangengift ein hocheffizientes Gerüst zum Anvisieren von αvβ3 bereitstellen, indem sie drei koordinierte Kontaktregionen und eine starre Bindungsschleife nutzen und so einfachen RGD‑basierten Molekülen überlegen sind. Indem die Studie genau kartiert, wie Tmu und Rho den Rezeptor ansprechen — und wie kleine Sequenzänderungen diese Interaktion verändern — liefert sie einen strukturellen Bauplan für die Entwicklung der nächsten Generation von Integrinblockern, die selektiver gegenüber αvβ3 sind und weniger wahrscheinlich Blutungen oder andere Nebenwirkungen verursachen. Kurz: Indem Wissenschaftlerinnen und Wissenschaftler lernen, wie Schlangen unsere Zelladhäsionsmechanik mit größter Präzision lahmlegen, gewinnen sie neue Ideen, diese natürlichen Waffen in gezielte Therapien gegen Krebs und entzündliche Erkrankungen zu verwandeln.
Zitation: Wang, YT., Chang, YT., Huang, CH. et al. Structural basis for the differential recognition of integrin αvβ3 by rhodostomin and trimucrin. Commun Biol 9, 583 (2026). https://doi.org/10.1038/s42003-026-10139-6
Schlüsselwörter: integrin alpha v beta 3, Schlangengift-Disintegrine, rhodostomin trimucrin, Krebs und Angiogenese, Kryo-Elektronenmikroskopie