Clear Sky Science · ar
الأساس البنيوي للاعتراف التفاضلي للإنتيجرين αvβ3 بواسطة رودوستومين وتريموكرين
تحويل بروتينات السم إلى أدوات طبية دقيقة
قد يبدو سم الأفاعي سمًا خالصًا، لكن بعض جزيئاته فعّالة بشكل ملحوظ في حجب بروتينات مرتبطة بالأمراض داخل أجسامنا. تستكشف هذه الدراسة كيف يلتصق جزيئان مشتقان من السم بمستقبل مهم على سطح الخلية مرتبط بالسرطان ونمو الأوعية الدموية، كاشفةً تفاصيل على المستوى الذري قد توجه تصميم أدوية أكثر أمانًا ودقة.
قابضة خلوية تتعلمها السرطان للاستفادة منها
تستخدم خلايانا "قوابض" بروتينية تُدعى إنتيجرينات للالتحام ببيئتها ولإحساس الإشارات الميكانيكية والكيميائية. أحد هذه الإنتيجرينات، المسمى αvβ3، يساعد الخلايا على الاستجابة لبيئتها وله دور رئيسي في نمو أوعية دموية جديدة، توسع الأورام، انتشار الخلايا السرطانية، ومقاومة الأدوية. لهذا السبب، لطالما كان αvβ3 هدفًا للأدوية المضادة للسرطان ومضادة لتكوّن الأوعية. ومع ذلك، فإن عقودًا من العمل لم تسفر عن أي مثبطات αvβ3 معتمدة للاستخدام البشري، جزئيًا لأن فهم كيفية ارتباط جزيئات مختلفة بهذا المستقبل والتحكم فيه كان صعبًا.
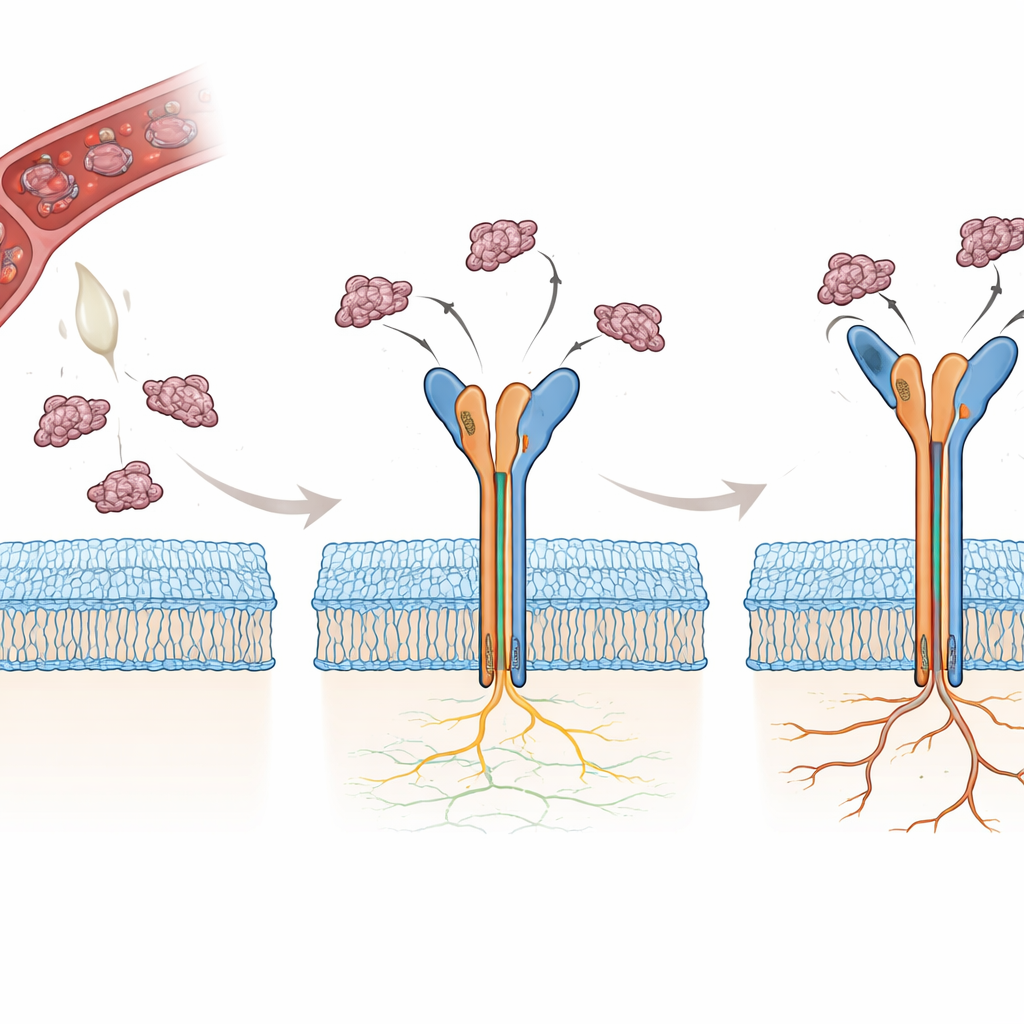
لماذا جزيئات سم الأفاعي قوية جدًا
تنتج العديد من الأفاعي بروتينات صغيرة تُدعى ديسانتجرينات (disintegrins) تحجب الإنتيجرينات طبيعيًا، مما يمنع تجلط الدم ويتداخل مع التصاق الخلايا. اثنان من هذه الديسانتجرينات، رودوستومين (Rho) وتريموكرين (Tmu)، يحتويان على تسلسل قصير من ثلاثة أحماض أمينية—أرجينين-جليسين-أسبارتات، أو RGD—الذي يتعرف عليه αvβ3. من المدهش أن Tmu أقوى بحوالي ثلاثة إلى أربعة أضعاف من Rho في تعطيل هذا الإنتيجرين. يتشارك الجزيئان معظم تسلسلهما لكنهما يختلفان في ثلاثة مناطق رئيسية: وصلة قصيرة، والحلقة المرنة التي تحتوي RGD، ونهاية الذيل للبروتين. سعى المؤلفون إلى تحديد، ذرة بذرة، كيف تغيّر هذه الاختلافات الصغيرة طريقة كل بروتين سمّي في قبضة αvβ3 ولماذا يجعل ذلك Tmu مثبطًا أقوى.
التقاط البنى بتفصيل عالٍ
للإجابة عن هذه الأسئلة، حلل الباحثون أولاً البنية البلورية لـTmu وحده بدقة عالية جدًا، مؤكدين أنها تشكل إطارًا مدمجًا وصلبًا مثبتًا بست روابط ثنائية الكبريتيد. ثم استخدموا المجهري الإلكتروني بالتبريد لتحديد البنى ثلاثية الأبعاد لـαvβ3 المرتبط إما بـRho أو Tmu، محققين دقة أقل من ثلاثة أنغسترومات لرأس المستقبل حيث يحدث الارتباط. في الحالتين، يجلس الديسانتجرين في شق بين نطاقين من رأس الإنتيجرين، مدخلًا حلقة RGD في موقع يحتوي على معدن. شكل العمود الفقري لـRho وTmu في هذه المنطقة متطابق تقريبًا، ما يبيّن أن كلا البروتينين يأتِيان مُشكَّلين مسبقًا في حالة جاهزة للارتباط، بدلاً من الاضطرار لخضوعهما لإعادة ترتيب كبيرة عند الالتصاق بالمستقبل.
ثلاث مناطق اتصال ومشبك أقوى
كشف الفحص الدقيق أن الارتباط لا يحكمه مجرد ثلاثي RGD وحده. يستخدم كلا الديسانتجرينين ثلاث مناطق تلامس تعاونية: حلقة RGD نفسها؛ منطقة الوصلة القريبة؛ وذيل C-الطرف. في Tmu، تُكوِّن مجموعة من الأحماض الأمينية الموجبة الشحنة في الوصلة اتصالات كهربائية إضافية مع السطح السالب الشحنة للوحدة β3، مما يساعده على التشبث بقوة أكبر بـαvβ3. بالمقابل، يعتمد Rho أكثر على منطقة ذيله للحصول على اتصالات إضافية. عند تبادل مقاطع تسلسلية محددة بين بروتيني السم، تمكن الفريق من زيادة أو خفض قوة الحجب. وعلى وجه الخصوص، أدى نقل وصلة Tmu المشحونة إلى Rho إلى تعزيز قدرة Rho على تثبيط αvβ3 بنحو عشرة أضعاف، مؤكّدًا أن رقعة الارتباط الإضافية هذه تُعد مساهمًا رئيسيًا في الفعالية.
كيف يقلب الارتباط حالة المستقبل—وكيف تهم ذرة واحدة
التقاطات البُنى وثقت أيضًا كيف يعيد ارتباط الديسانتجرين شكل الإنتيجرين نفسه. يفضّل αvβ3 الحر وضعية منحنية ومغلقة؛ لكن بمجرد ارتباط Rho أو Tmu، يخضع نصف β3 من المستقبل لتحولات منسقة في لولبيتين ومواقع ارتباط المعادن، ما يدفع المستقبل إلى حالة ممتدة ومفتوحة مرتبطة بفعالية عالية. ومع ذلك، تساعد حمضة أمينية واحدة، التيروزين عند الموقع 110 في β3، على تثبيت الشكل المنحني عبر جسر بين نطاقين. عندما بدّل الباحثون هذا البقايا إلى ألانين، فضّل المستقبل تلقائيًا الحالة الممتدة وربط شريكه الطبيعي، الفيتروكتين، بقوة أكبر. يسلّط ذلك الضوء على كيف يمكن لتغيرات ذرية طفيفة أن تضبط تنشيط الإنتيجرين ويقترح أن المتغيرات المصممة قد تكون أدوات مفيدة لفحص أدوية جديدة.
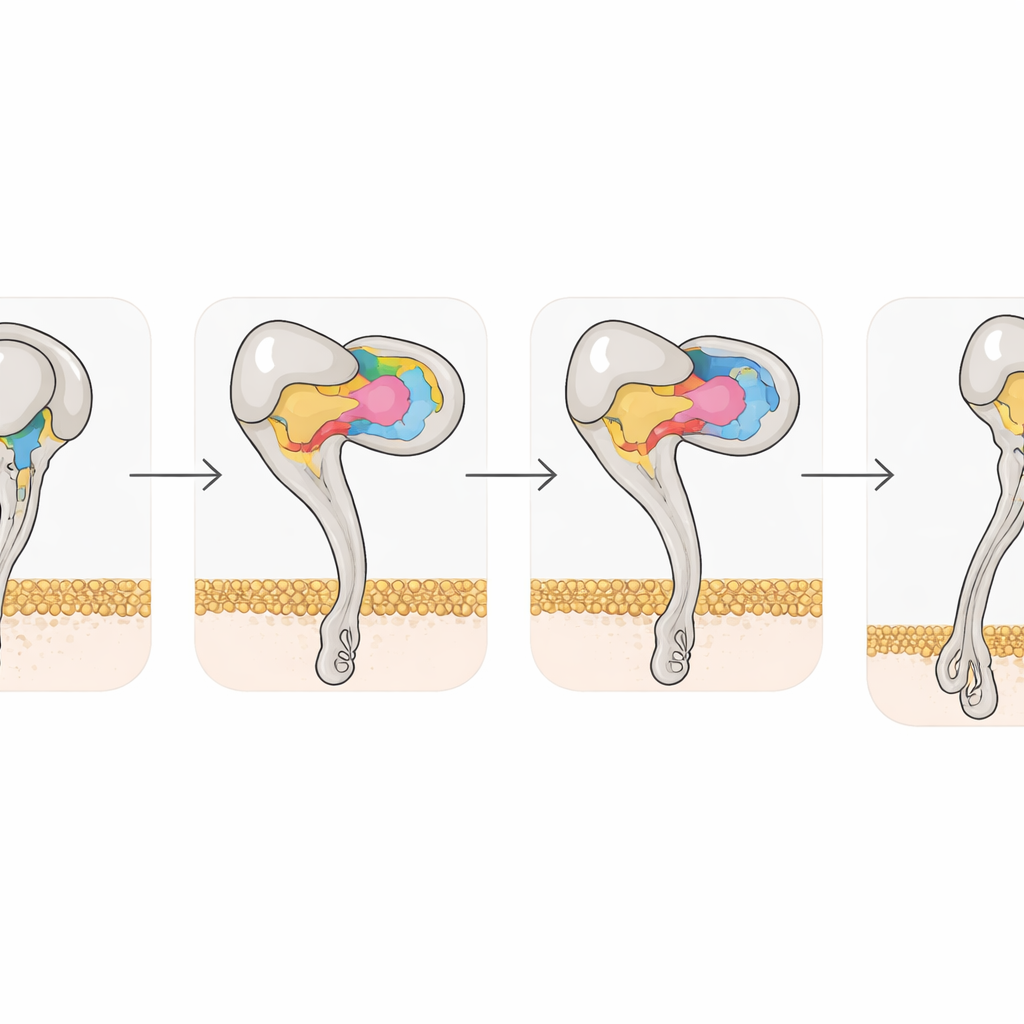
من دلائل السم إلى أدوية مستقبلية للسرطان
تظهر الأعمال مجتمعة أن الديسانتجرينات المتوسطة الحجم المشتقة من السم توفر سقالة فعّالة للغاية لاستهداف αvβ3، مستخدمة ثلاث مناطق تلامس منسقة وحلقة رابطة صلبة لتتفوق على الجزيئات البسيطة المبنية على RGD. من خلال رسم خريطة دقيقة لكيفية تفاعل Tmu وRho مع المستقبل—وكيف تغيّر التغييرات التسلسلية الصغيرة هذا التفاعل—تقدّم الدراسة مخططًا بنيويًا لتصميم مثبطات إنتيجرين من الجيل التالي تكون أكثر انتقائية لـαvβ3 وأقل احتمالًا للتسبب في نزف أو آثار جانبية أخرى. جوهريًا، من خلال تعلّم كيف تعطل الأفاعي آليات التصاق خلايانا بدقة رائعة، يكتسب العلماء أفكارًا جديدة لتحويل هذه الأسلحة الطبيعية إلى علاجات مستهدفة ضد السرطان والأمراض الالتهابية.
الاستشهاد: Wang, YT., Chang, YT., Huang, CH. et al. Structural basis for the differential recognition of integrin αvβ3 by rhodostomin and trimucrin. Commun Biol 9, 583 (2026). https://doi.org/10.1038/s42003-026-10139-6
الكلمات المفتاحية: الإنتيجرين ألفا فاء بيتا 3, مشتقات سموم الأفاعي المانعة للتماسك, رودوستومين تريموكرين, السرطان وتكوّن الأوعية الدموية, مجهري إلكتروني بالتبريد