Clear Sky Science · it
Base strutturale per il riconoscimento differenziale dell’integrina αvβ3 da parte di rhodostomin e trimucrin
Proteine del veleno trasformate in strumenti di medicina di precisione
Il veleno di serpente può suonare come puro veleno, ma alcune sue molecole sono straordinariamente efficaci nel bloccare proteine correlate alle malattie nel nostro organismo. Questo studio esplora come due molecole derivate dal veleno si agganciano a un recettore chiave sulla superficie cellulare, collegato al cancro e alla crescita dei vasi sanguigni, rivelando dettagli a livello atomico che potrebbero guidare la progettazione di farmaci più sicuri e più precisi.
Una presa cellulare che il cancro impara a sfruttare
Le nostre cellule usano “prese” proteiche chiamate integrine per attaccarsi all’ambiente circostante e per percepire segnali meccanici e chimici. Un’integrina in particolare, chiamata αvβ3, aiuta le cellule a rispondere all’ambiente e gioca un ruolo importante nella formazione di nuovi vasi sanguigni, nell’espansione dei tumori, nella diffusione delle cellule tumorali e nella resistenza ai farmaci. Per questo motivo, αvβ3 è stata a lungo un bersaglio per farmaci anticancro e anti-angiogenici. Eppure decenni di lavoro non hanno portato a inibitori di αvβ3 approvati per uso umano, in parte perché è stato difficile comprendere esattamente come molecole diverse si legano e modulano questo recettore.
Perché le molecole del veleno sono così potenti
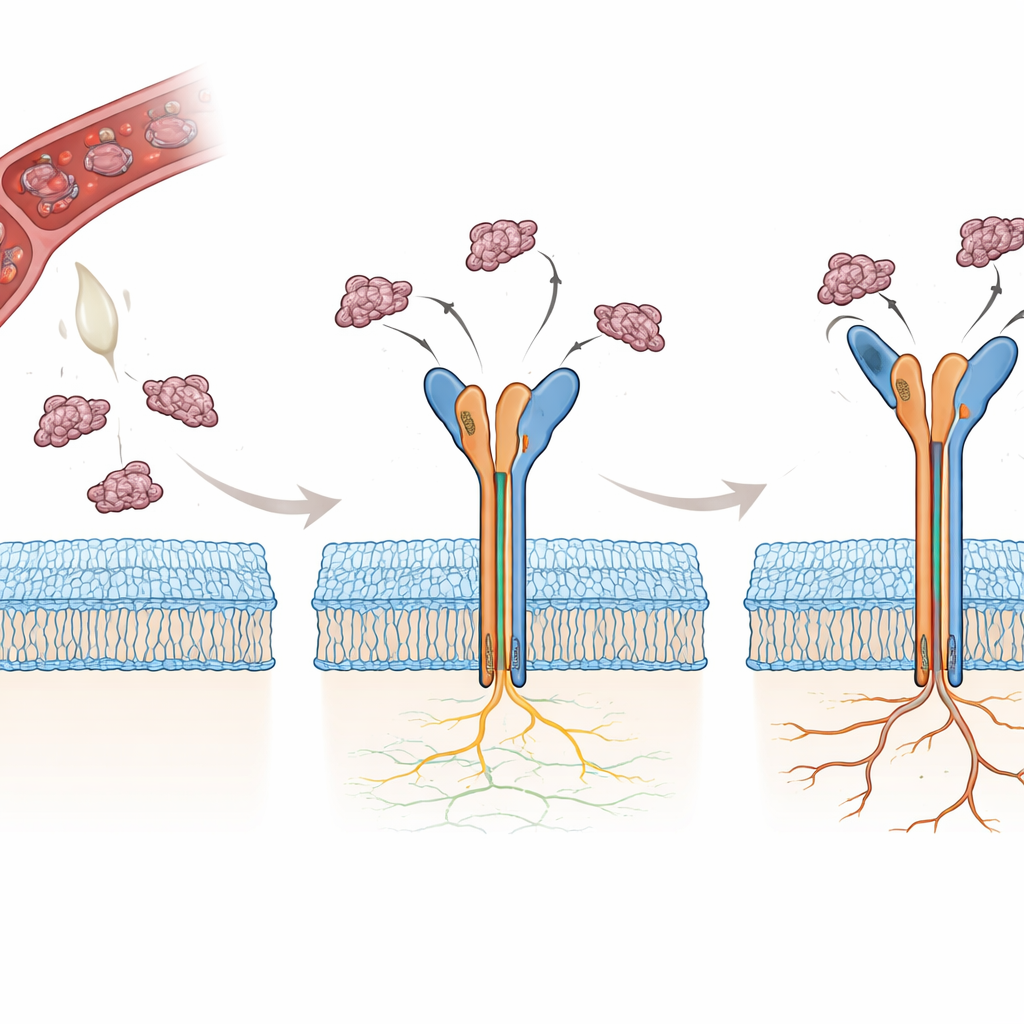
Molti serpenti producono piccole proteine chiamate disintegrine che bloccano naturalmente le integrine, impedendo la coagulazione del sangue e interferendo con l’adesione cellulare. Due di queste disintegrine, rhodostomin (Rho) e trimucrin (Tmu), contengono entrambe una breve sequenza di tre amminoacidi — arginina-glicina-aspartato, o RGD — riconosciuta da αvβ3. Sorprendentemente, Tmu è circa tre-quattro volte più efficace di Rho nello spegnere questa integrina. Le due molecole condividono la maggior parte della sequenza ma differiscono in tre regioni chiave: un breve linker, il loop flessibile contenente l’RGD e l’estremità C-terminale della proteina. Gli autori hanno voluto determinare, atomo per atomo, come queste piccole differenze cambino il modo in cui ciascuna proteina del veleno si ancora a αvβ3 e perché ciò rende Tmu un inibitore più potente.
Catturare le strutture con alto dettaglio
Per rispondere a queste domande, i ricercatori hanno prima risolto la struttura cristallina di Tmu da sola ad altissima risoluzione, confermando che forma un’impalcatura compatta e rigida stabilizzata da sei legami disolfuro. Hanno poi usato la microscopia elettronica criogenica per determinare le strutture tridimensionali di αvβ3 legata a Rho o a Tmu, raggiungendo risoluzioni inferiori a tre angstrom per la testa del recettore dove avviene il legame. In entrambi i casi, la disintegrina si adagia in una fessura tra due domini della testa dell’integrina, inserendo il suo loop RGD in un sito contenente metalli. L’andamento della spina dorsale di Rho e Tmu in questa regione è quasi identico, mostrando che entrambe le proteine arrivano preformate in una conformazione pronta al legame, anziché dover subire grandi riorganizzazioni per interagire con il recettore.
Tre zone di contatto e una presa più forte
L’analisi più approfondita ha rivelato che il legame non è governato solo dal tripletto RGD. Entrambe le disintegrine utilizzano tre zone di contatto cooperative: il loop RGD stesso; una regione linker vicina; e la coda C-terminale. In Tmu, un cluster di amminoacidi carichi positivamente nel linker stabilisce contatti elettrostatici aggiuntivi con la superficie negativamente carica della subunità β3, contribuendo a serrarsi più saldamente su αvβ3. Rho, al contrario, si affida maggiormente alla sua regione terminale per contatti supplementari. Quando il team ha scambiato segmenti di sequenza specifici tra le due proteine del veleno, ha potuto modulare la potenza inibitoria. In particolare, trasferire il linker carico di Tmu in Rho ha aumentato la capacità di Rho di inibire αvβ3 di circa dieci volte, confermando che questa patch di legame aggiuntiva è un contributo principale alla potenza.
Come il legame attiva il recettore — e come un singolo atomo conta
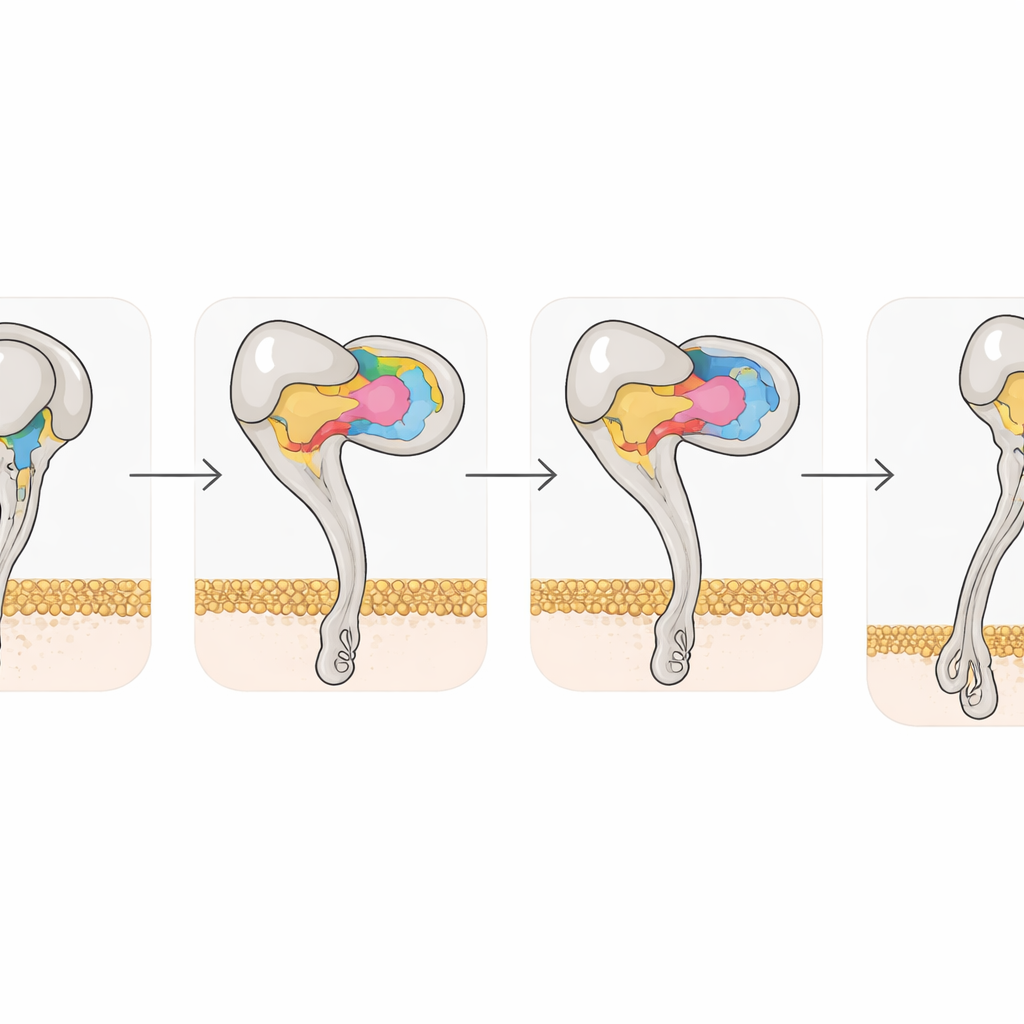
Gli istantanee strutturali hanno anche catturato come il legame della disintegrina rimodelli l’integrina stessa. L’αvβ3 libera preferisce una postura piegata e chiusa; una volta che Rho o Tmu si legano, la metà β3 del recettore subisce spostamenti coordinati in due eliche e nei siti di legame dei metalli, spingendo il recettore in uno stato completamente esteso e aperto associato a elevata attività. Tuttavia un singolo amminoacido, la tirosina 110 nella β3, aiuta a tenere insieme la forma piegata facendo da ponte tra due domini. Quando i ricercatori hanno mutato questa residuo in alanina, il recettore ha favorito spontaneamente lo stato esteso e si è legato più fortemente al suo partner naturale, la vitronectina. Questo evidenzia come cambiamenti atomici sottili possano modulare l’attivazione delle integrine e suggerisce che varianti ingegnerizzate potrebbero essere utili come strumenti per lo screening di nuovi farmaci.
Dai suggerimenti del veleno ai futuri farmaci antitumorali
Nel complesso, il lavoro mostra che le disintegrine del veleno di dimensioni medie forniscono uno scheletro altamente efficiente per mirare αvβ3, usando tre regioni di contatto coordinate e un loop di legame rigido per superare le semplici molecole a base RGD. Mappando esattamente come Tmu e Rho interagiscono con il recettore — e come piccoli cambi di sequenza ne alterino l’interazione — lo studio offre una mappa strutturale per progettare la prossima generazione di inibitori delle integrine più selettivi per αvβ3 e meno propensi a causare sanguinamento o altri effetti collaterali. In sostanza, imparando come i serpenti disabilitano con precisione la nostra macchina di adesione cellulare, gli scienziati ottengono nuove idee per trasformare queste armi naturali in terapie mirate contro il cancro e le malattie infiammatorie.
Citazione: Wang, YT., Chang, YT., Huang, CH. et al. Structural basis for the differential recognition of integrin αvβ3 by rhodostomin and trimucrin. Commun Biol 9, 583 (2026). https://doi.org/10.1038/s42003-026-10139-6
Parole chiave: integrina alpha v beta 3, disintegrine del veleno di serpente, rhodostomin trimucrin, cancro e angiogenesi, crio-microscopia elettronica