Clear Sky Science · nl
Structurele basis voor de differentiële herkenning van integrine αvβ3 door rhodostomin en trimucrin
Gifproteïnen omgevormd tot precisiegeneesmiddelen
Slangengif klinkt misschien als puur vergif, maar sommige van de daarin aanwezige moleculen zijn opmerkelijk effectief in het blokkeren van ziektegerelateerde eiwitten in ons lichaam. Deze studie onderzoekt hoe twee van die gif-afgeleide moleculen zich vasthechten aan een belangrijke celoppervlakte-receptor die gekoppeld is aan kanker en de groei van bloedvaten, en onthult atoomniveau-details die het ontwerp van veiligere, meer precieze medicijnen kunnen sturen.
Een celgreep die kanker weet uit te buiten
Onze cellen gebruiken eiwit"grepen" die integrines worden genoemd om zich aan hun omgeving te hechten en om mechanische en chemische signalen waar te nemen. Één specifieke integrine, aangeduid als αvβ3, helpt cellen te reageren op hun omgeving en speelt een grote rol bij de vorming van nieuwe bloedvaten, de uitbreiding van tumoren, het uitzaaien van kankercellen en medicijnafwijking. Daarom is αvβ3 al lang een doelwit voor anti-kanker- en anti-angiogenese-middelen. Toch heeft decennia van onderzoek geen goedgekeurde αvβ3-remmers voor menselijk gebruik opgeleverd, deels omdat het moeilijk is geweest precies te begrijpen hoe verschillende moleculen zich aan deze receptor binden en deze reguleren.
Waarom slangenvenomemoleculen zo krachtig zijn
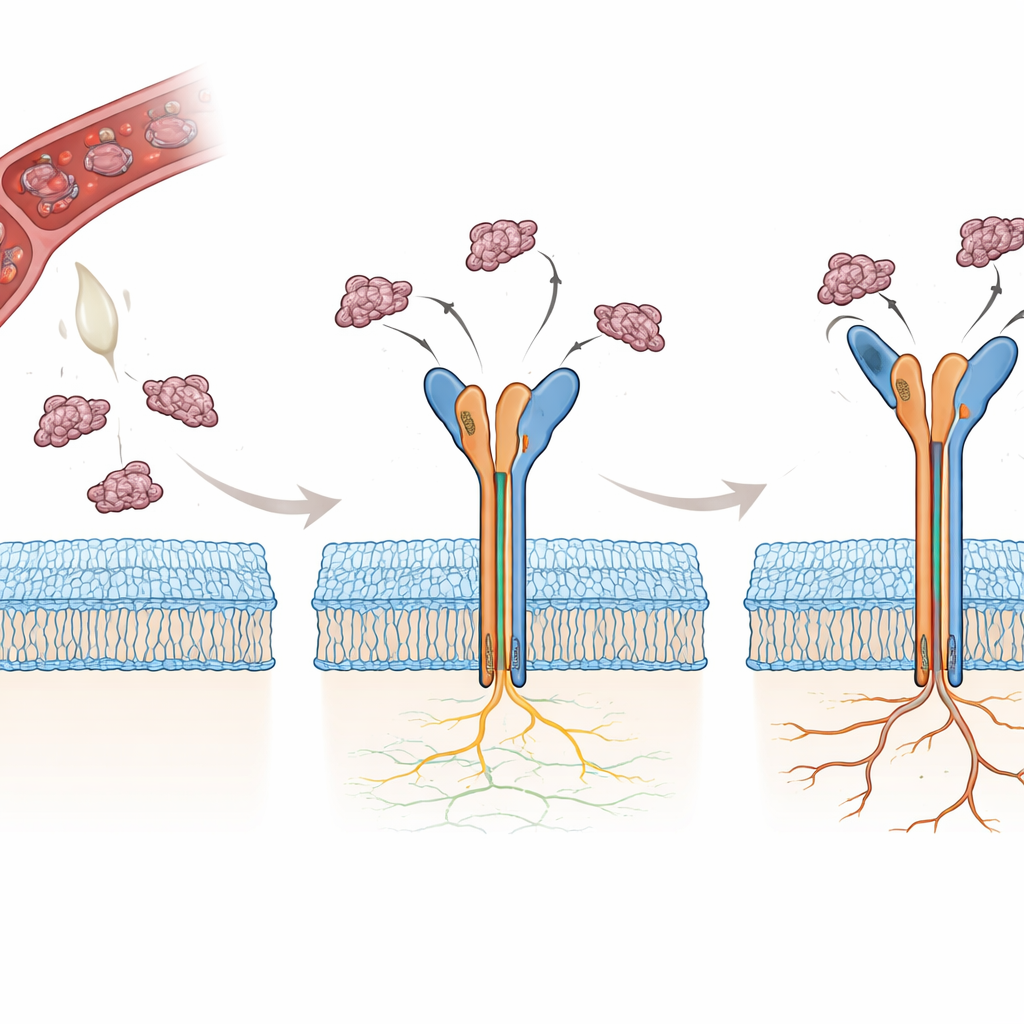
Veel slangen produceren kleine eiwitten die disintegrines worden genoemd en van nature integrines blokkeren, waardoor bloedstolling wordt belemmerd en celadhesie verstoord raakt. Twee zulke disintegrines, rhodostomin (Rho) en trimucrin (Tmu), bevatten beide een korte sequentie van drie aminozuren — arginine-glycine-asparaat, of RGD — die door αvβ3 wordt herkend. Verrassend genoeg is Tmu ongeveer drie- tot viermaal effectiever dan Rho in het uitschakelen van deze integrine. De twee moleculen delen het grootste deel van hun sequentie maar verschillen op drie cruciale plaatsen: een korte schakelaar (linker), de flexibele RGD-bevattende lus en het staartuiteinde van het eiwit. De auteurs wilden op atoomniveau bepalen hoe deze kleine verschillen de manier veranderen waarop elk gif-eiwit αvβ3 vastgrijpt en waarom dat Tmu tot een krachtiger remmer maakt.
Het vastleggen van de structuren in hoge detail
Om deze vragen te beantwoorden bepaalden de onderzoekers eerst de kristalstructuur van Tmu alleen op zeer hoge resolutie, waarmee ze bevestigden dat het een compact, rigide kader vormt dat wordt gestabiliseerd door zes disulfidebruggen. Vervolgens gebruikten ze cryogene elektronenmicroscopie om driedimensionale structuren te bepalen van αvβ3 gebonden aan respectievelijk Rho of Tmu, waarbij ze resoluties onder de drie angstrom bereikten voor het kopgedeelte van de receptor waar binding plaatsvindt. In beide gevallen zit de disintegrine in een inkeping tussen twee domeinen van het integrinekopgedeelte en schuift zijn RGD-lus in een metaalhoudende bindingsplaats. De ruggegraatvorm (backbone) van Rho en Tmu in dit gebied is vrijwel identiek, wat aantoont dat beide eiwitten al in een bindingsklare vorm aanwezig zijn in plaats van grote herschikkingen te moeten ondergaan bij interactie met de receptor.
Drie contactzones en een sterkere klem
Nadere inspectie toonde aan dat binding niet alleen door het RGD-triplet wordt bepaald. Beide disintegrines gebruiken drie samenwerkende contactzones: de RGD-lus zelf; een nabijgelegen linkerregio; en de C-terminus (staart). Bij Tmu zorgt een cluster van positief geladen aminozuren in de linker voor extra elektrostatische contacten met het negatief geladen oppervlak van de β3-subunit, waardoor het strakker op αvβ3 klemt. Rho daarentegen leunt meer op zijn staartregio voor aanvullende contacten. Toen het team specifieke sequentiesegmenten tussen de twee gif-eiwitten verwisselde, konden ze de blokkerende kracht verhogen of verlagen. Met name het overbrengen van Tmu’s geladen linker naar Rho vergrootte Rho’s vermogen om αvβ3 te remmen met ongeveer tien keer, wat bevestigt dat dit extra bindingsvlak een belangrijke bijdrage levert aan de potentie.
Hoe binding de receptor aanzet — en hoe één atoom telt
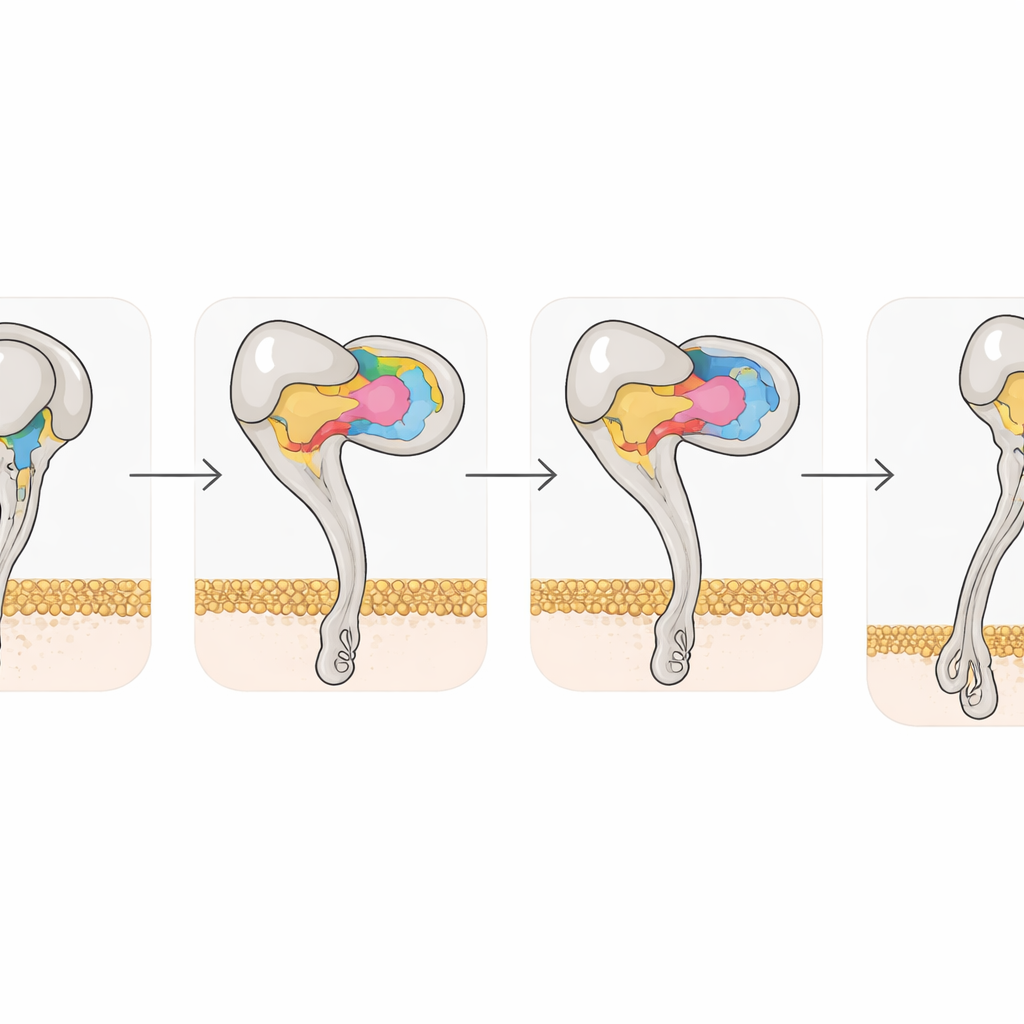
De structurele momentopnamen lieten ook zien hoe disintegrinebinding de integrine zelf hervormt. Vrije αvβ3 heeft de neiging een gebogen, gesloten houding aan te nemen; zodra Rho of Tmu bindt, ondergaat het β3-gedeelte van de receptor gecoördineerde verschuivingen in twee helices en metaalbindende sites, waardoor de receptor in een volledig uitgestrekte, open toestand komt die geassocieerd is met hoge activiteit. Toch helpt één enkel aminozuur, tyrosine 110 in β3, de gebogen vorm bij elkaar te houden door twee domeinen te overbruggen. Toen de onderzoekers dit residu naar alanine muteerden, gaf de receptor spontaan de voorkeur aan de uitgestrekte staat en bond hij sterker aan zijn natuurlijke partner, vitronektine. Dit benadrukt hoe subtiele atomaire wijzigingen integrineactivatie kunnen afstemmen en suggereert dat ontworpen varianten nuttige instrumenten kunnen zijn voor het screenen van nieuwe geneesmiddelen.
Van gifclues naar toekomstige kankergeneesmiddelen
Samengevat toont het werk aan dat middelgrote venom-disintegrines een zeer efficiënt stramien vormen om αvβ3 te targeten, waarbij drie gecoördineerde contactregio’s en een rigide bindingslus eenvoudige RGD-gebaseerde moleculen overtreffen. Door precies in kaart te brengen hoe Tmu en Rho de receptor binden — en hoe kleine sequentiewijzigingen deze interactie veranderen — biedt de studie een structureel bouwplan voor het ontwerpen van volgende generatie integrineremmers die selectiever zijn voor αvβ3 en minder kans geven op bloedingen of andere bijwerkingen. In wezen, door te leren hoe slangen onze celadhesieapparatuur met uiterste precisie uitschakelen, krijgen wetenschappers nieuwe ideeën om deze natuurlijke wapens om te zetten in gerichte therapieën tegen kanker en ontstekingsziekten.
Bronvermelding: Wang, YT., Chang, YT., Huang, CH. et al. Structural basis for the differential recognition of integrin αvβ3 by rhodostomin and trimucrin. Commun Biol 9, 583 (2026). https://doi.org/10.1038/s42003-026-10139-6
Trefwoorden: integrine alpha v beta 3, slangenvenom disintegrines, rhodostomin trimucrin, kanker en angiogenese, kryo-elektronenmicroscopie