Clear Sky Science · he
הבסיס המבני לזיהוי השונה של אינטגרין αvβ3 על־ידי רודוסטומין וטרימוּקרין
חלבוני ארס שהופכים לכלי רפואה מדויקים
ארס נחשים נשמע כמו רעל טהור, אבל חלק מהמולקולות שבו מצטיינות בחסימת חלבונים שקשורים למחלות בגופנו. המחקר הזה בוחן כיצד שתי מולקולות שמקורן בארס נקשרות לקולטן מרכזי על פני תא שמקושר לסרטן ולצמיחת כלי דם, וחושף פרטים ברמת האטום שעשויים להנחות עיצוב תרופות בטוחות ומדויקות יותר.
אחיזה תאית שהסרטן למד לנצל
התאים שלנו משתמשים ב"אחיזות" חלבוניות הנקראות אינטגרינים כדי להצמד לסביבה שלהם ולחוש רמזים מכניים וכימיים. אינטגרין מסוים בשם αvβ3 מסייע לתאים להגיב לסביבה וממלא תפקיד מרכזי בגדילת כלי דם חדשים, בהתרחבות של גידולים, בהתפשטות תאי סרטן ובהתנגדות לתרופות. בשל כך, αvβ3 היה מטרה מתמשכת לתרופות אנטי־סרטן ואנטי־אנגיוגניות. עם זאת, עשורים של מאמצים לא הניבו חוסמים מאושרים של αvβ3 לשימוש בבני אדם, בין השאר משום שקשה היה להבין בדיוק כיצד מולקולות שונות נקשרות לקולטן ומווסתות אותו.
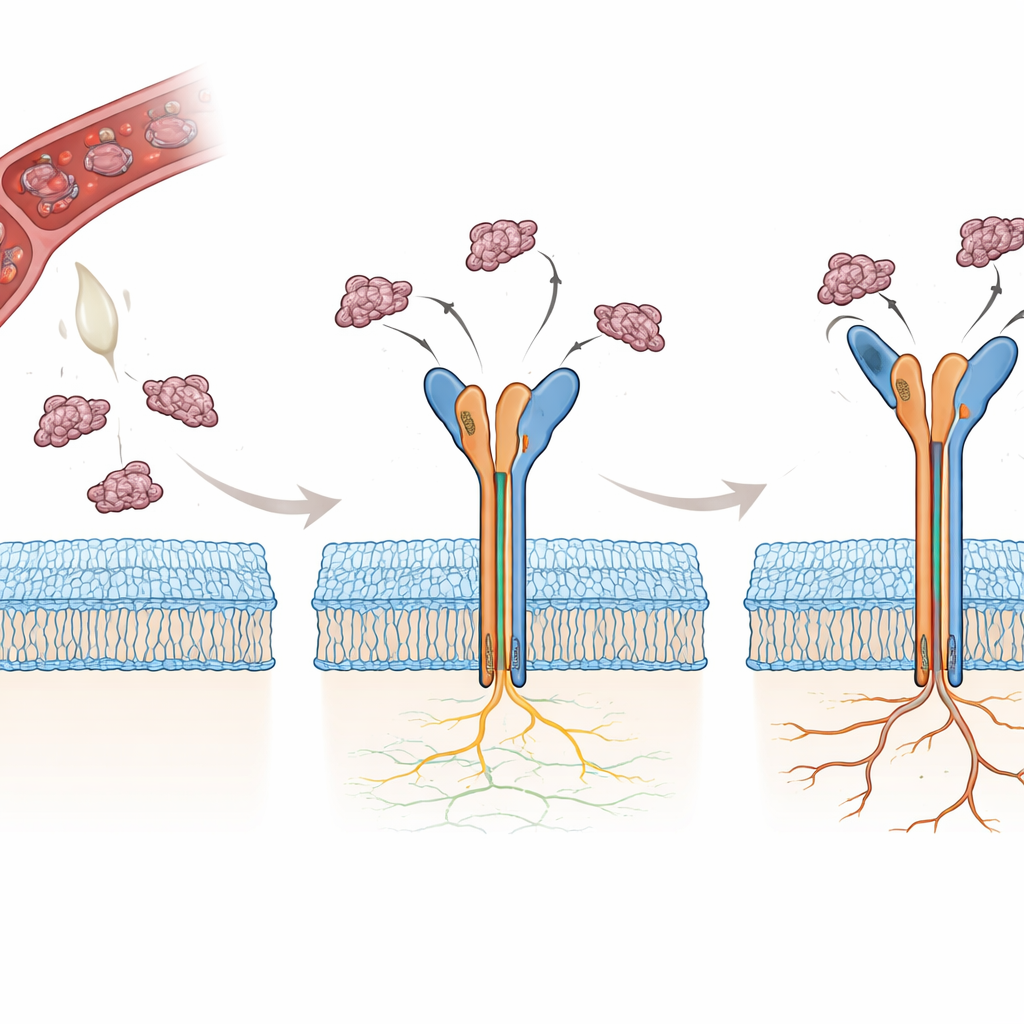
למה מולקולות ארס כל כך עוצמתיות
נחשים רבים מייצרים חלבונים קטנים הנקראים דיסינטרינים שמפגינים יכולת טבעית לחסום אינטגרינים, למנוע קרישה ולהפריע להצמדות תאים. שני דיסינטרינים כאלה, רודוסטומין (Rho) וטרימוּקרין (Tmu), מכילים רצף קצר של שלוש חומצות אמינו — ארגינין־גליצין־אספרטאט, או RGD — שמוכר על־ידי αvβ3. באופן מפתיע, Tmu יעיל בכ־שלוש עד ארבע פעמים יותר מ־Rho בכיבוי האינטגרין הזה. שתי המולקולות חולקות רוב הרצף שלהן אך שונות בשלושה אזורים מרכזיים: קישורון קצר, הלולאה הגמישה שמכילה את ה־RGD, וקצה־הזנב של החלבון. החוקרים ביקשו לקבוע, אטום־אחר־אטום, כיצד הבדלים קטנים אלה משנים את האופן שבו כל חלבון ארסי אוחז ב־αvβ3 ולמה זה הופך את Tmu למעכב עוצמתי יותר.
לכידת המבנים ברזולוציה גבוהה
כדי לענות על השאלות הללו, החוקרים פתרו תחילה את מבנה הגביש של Tmu לבדו ברזולוציה גבוהה מאוד, ואישרו שהוא יוצר שלד קומפקטי ונוקשה שמוּייצב על־ידי שישה קשרי דיסולפיד. לאחר מכן הם השתמשו בקריוגניית אלקטרון מיקרוסקופיה כדי לקבוע מבנים תלת־ממדיים של αvβ3 קשור ל־Rho או ל־Tmu, בהשגת רזולוציות מתחת לשלושה אנגסטרום לראש הקולטן שבו מתרחשת ההיקשרות. בשני המקרים נמצא שהדיסינטרין יושב בשקע בין שתי דומיינים של ראש האינטגרין ומחדיר את לולאת ה‑RGD שלו לאתר שמכיל מתכת. צורת השלד של Rho ו‑Tmu באזור זה כמעט זהה, מה שמראה ששתי המולקולות מגיעות מוכנות בקונפורמציה המותאמת לקשירה, ולא עוברות סידור גדול בעת התקשרות לקולטן.
שלוש אזורי מגע ו"מהדק" חזק יותר
בדיקה מקרוב חשפה שהקשירה אינה נשלטת רק על־ידי טריפלט ה‑RGD. שני הדיסינטרינים משתמשים בשלוש אזורי מגע משתפי פעולה: עצם לולאת ה‑RGD; אזור קישורון סמוך; וזנב קו־טרמינלי. ב‑Tmu, צבר של חומצות אמינו טעונות חיובית בקישורון יוצר קשרים אלקטרוסטטיים נוספים עם המשטח השלילי של תת־יחידת β3, ועוזר למהדק להיאחז ביתר חוזקה ב‑αvβ3. לעומת זאת, Rho סומך יותר על אזור הזנב שלו למגעים נוספים. כאשר הצוות החליף מקטעי רצף ספציפיים בין שני חלבוני הארס, הם יכלו לכוונן את כוח הבלימה למעלה או למטה. במיוחד, העברת הקישורון הממוצב בטעינה של Tmu ל‑Rho הגבירה כ־עשרת מונים את יכולת Rho לעכב את αvβ3, ואישרה ששטח קשירה נוסף זה הוא גורם מרכזי בעוצמה.
כיצד הקשירה משנה את הקולטן — ואיך אטום אחד משנה הכל
תמונות המבנה גם תפסו כיצד ההיקשרות של הדיסינטרין מעצבת מחדש את האינטגרין עצמו. αvβ3 החופשי מעדיף מצב כיפוף סגור; ברגע ש‑Rho או Tmu נקשרים, חצי‑ה־β3 של הקולטן עובר שינויים מתואמים בשתי הליקסיות ובאתרי קשירת המתכת, ודוחף את הקולטן למצב מתוח, פתוח, המזוהה עם פעילות גבוהה. עם זאת, חומצת אמינו בודדת, טירוזין 110 ב‑β3, מסייעת להחזיק את הצורה הכפופה על‑ידי גישור בין שני דומיינים. כאשר החוקרים החליפו שארית זו לאלנין, הקולטן נטה באופן ספונטני למצב המתוח וקשר בעוצמה רבה יותר לשותפו הטבעי, ויטרונקטין. ממצא זה מדגיש כיצד שינויים אטומיים עדינים יכולים לכוונן את הפעלת האינטגרין ומציע שגרסאות מהונדסות עשויות לשמש כלי סינון שימושי לתרופות חדשות.
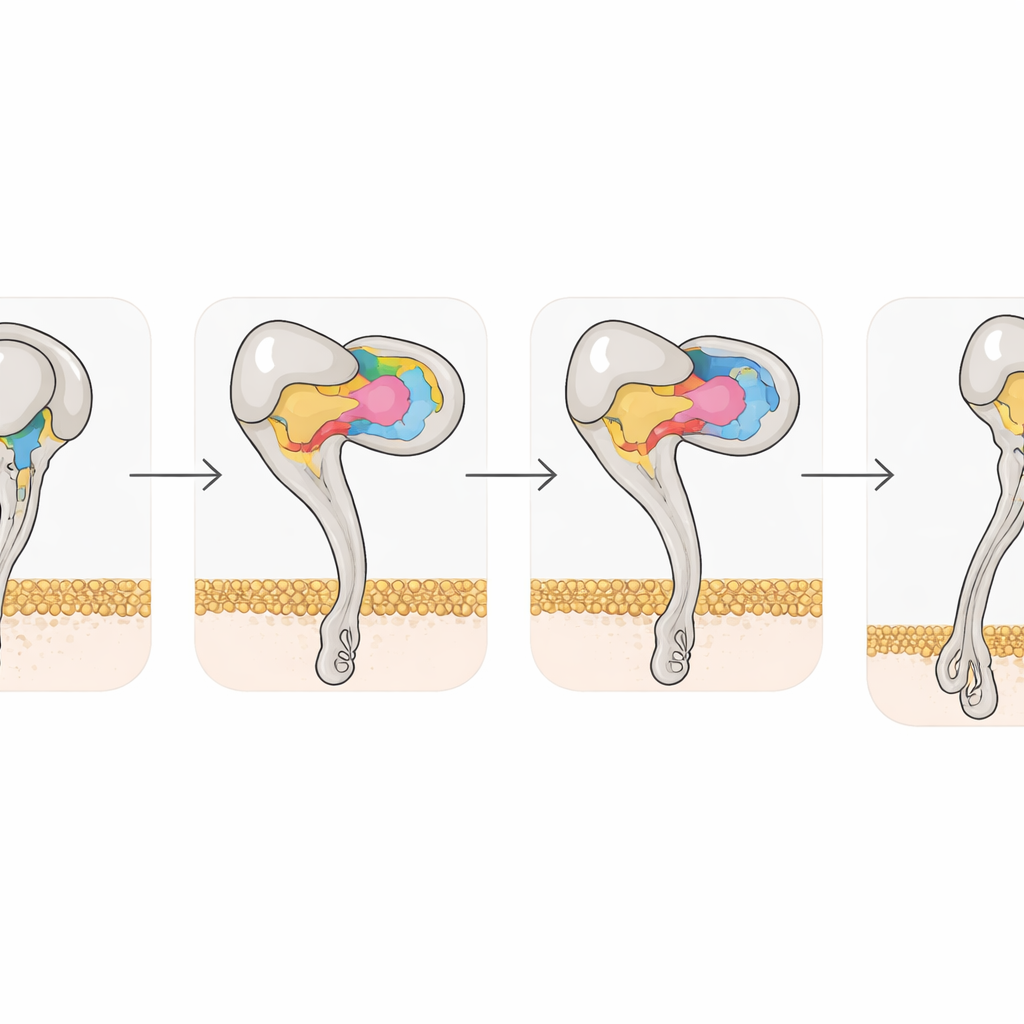
מרמזי ארס לתרופות סרטן עתידיות
בסיכומו של דבר, העבודה מראה שדיסינטרינים בגודל בינוני מהארס מספקים שלד יעיל מאד למיקוד αvβ3, באמצעות שלושה אזורי מגע מתואמים ולולאת קשירה נוקשה שמצטיינת על מולקולות מבוססות‑RGD בלבד. על ידי מיפוי מדויק של האופן שבו Tmu ו‑Rho נצמדים לקולטן — ואיך שינויים קטנים ברצף משנים את האינטראקציה הזו — המחקר מציע שרטוט מבני לתכנון דורות הבאים של חוסמי אינטגרין שיהיו בררניים יותר ל‑αvβ3 ופחות סיכונים לגרימת דימומים או תופעות לוואי אחרות. בעצם, על‑ידי למידה כיצד נחשים משביתים את מכניקת הדבקת התאים שלנו בדיוק מרבי, מדענים מקבלים רעיונות חדשים להמרת נשק טבעי זה לטיפולים ממוקדים נגד סרטן ומחלות דלקתיות.
ציטוט: Wang, YT., Chang, YT., Huang, CH. et al. Structural basis for the differential recognition of integrin αvβ3 by rhodostomin and trimucrin. Commun Biol 9, 583 (2026). https://doi.org/10.1038/s42003-026-10139-6
מילות מפתח: אינטגרין אלפא וי ביתא 3, דיסינטרינים מטריפת נחש, רודוסטומין טרימוּקרין, סרטן ואנגיוגנזה, קריואלקטרון מיקרוסקופיה