Clear Sky Science · ja
ロドストミンとトリムクリンによるインテグリンαvβ3の識別差の構造的基盤
毒から生まれた精密医療ツール
ヘビの毒は純粋な毒物のように聞こえますが、その中のいくつかの分子は私たちの体内の病態関連タンパク質をブロックするのに非常に優れています。本研究は、こうした毒由来分子のうち二つが、がんや血管新生に関連する重要な細胞表面受容体にどのように結合するかを調べ、より安全で精密な薬剤設計の指針となる原子レベルの詳細を明らかにしています。
がんが巧みに利用する細胞の『つかみ』
細胞はインテグリンと呼ばれるタンパク質の「つかみ」を使って周囲に付着し、機械的・化学的な手がかりを感知します。中でもαvβ3は環境への応答を助け、新しい血管の成長、腫瘍の拡大、がん細胞の転移、薬剤耐性に重要な役割を果たします。このためαvβ3は長年、抗がんおよび抗血管新生薬の標的とされてきましたが、異なる分子がこの受容体にどのように結合し制御するかを正確に理解することが難しく、人間用の承認薬は未だに得られていません。
なぜヘビ毒分子は強力なのか
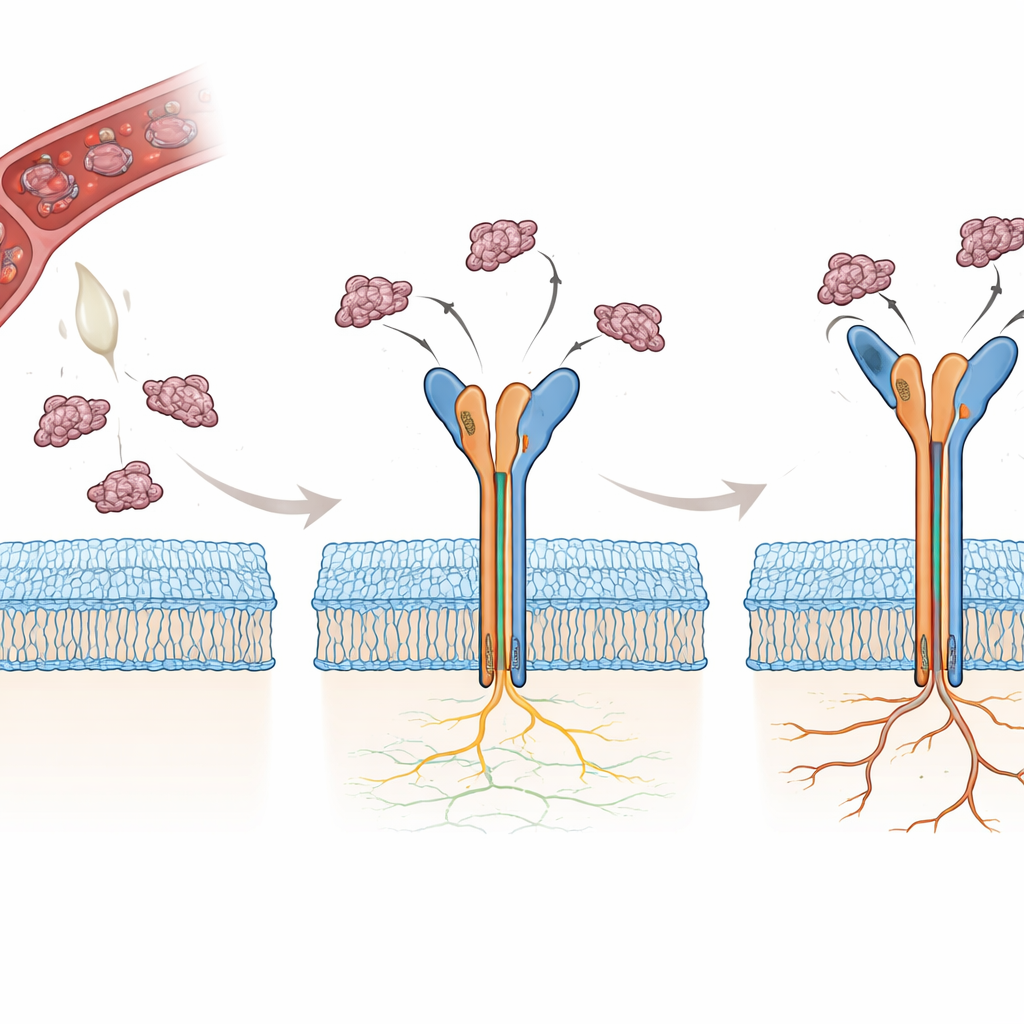
多くのヘビはディスインテグリンと呼ばれる小さなタンパク質を産生し、これが自然にインテグリンを阻害して血液凝固を妨げ、細胞接着に干渉します。ロドストミン(Rho)とトリムクリン(Tmu)はいずれもアルギニン–グリシン–アスパラギン酸(RGD)という三残基配列を含み、これがαvβ3に認識されます。驚くべきことに、TmuはRhoより約3〜4倍強力にこのインテグリンを抑制します。両者は配列の大部分を共有しますが、短いリンカー、RGDを含む可塑的なループ、タンパク質の末端尾部の三つの領域で異なります。著者らは、これらの小さな差が各毒タンパク質のαvβ3へのつかみ方をどのように変え、なぜTmuがより強力な阻害剤になるのかを原子単位で解明しようとしました。
高解像度で構造をとらえる
研究者らはまずTmu単独の結晶構造を非常に高い分解能で解き、その骨格が6つのジスルフィド結合で安定化されたコンパクトで剛直な枠組みを形成することを確認しました。次にクライオ電子顕微鏡を用いて、RhoまたはTmuが結合したαvβ3の三次元構造を決定し、結合が起こる受容体の頭部で3Å以下の解像度を得ました。両者の場合において、ディスインテグリンはインテグリン頭部の二つのドメインの間の溝に位置し、RGDループを金属含有部位に挿入しています。この領域におけるRhoとTmuの主鎖形状はほぼ同一で、両タンパク質が受容体と結合する際に大きな再配列を必要とせず、既に結合準備が整った形で到着することを示しています。
三つの接触領域とより強い締めつけ
詳細に調べると、結合はRGD三連だけで支配されているわけではないことが明らかになりました。両ディスインテグリンは相互に協調する三つの接触領域を用います:RGDループそのもの、近傍のリンカー領域、そしてC末端尾部です。Tmuでは、リンカーにある正に帯電したアミノ酸群がβ3サブユニットの負に帯電した表面と追加の静電的接触を作り、αvβ3により強く締めつけるのを助けます。これに対してRhoは、追加の接触を得るために尾部領域により依存します。研究チームが両毒タンパク質間で特定の配列セグメントを入れ替えると、阻害力を上下に調整できました。特にTmuの帯電したリンカーをRhoに移すと、Rhoのαvβ3阻害能が約10倍に増強され、この追加の結合パッチがポテンシーの主要な要因であることが確認されました。
結合が受容体をどのように作動させるか—そして一つの原子が重要な理由
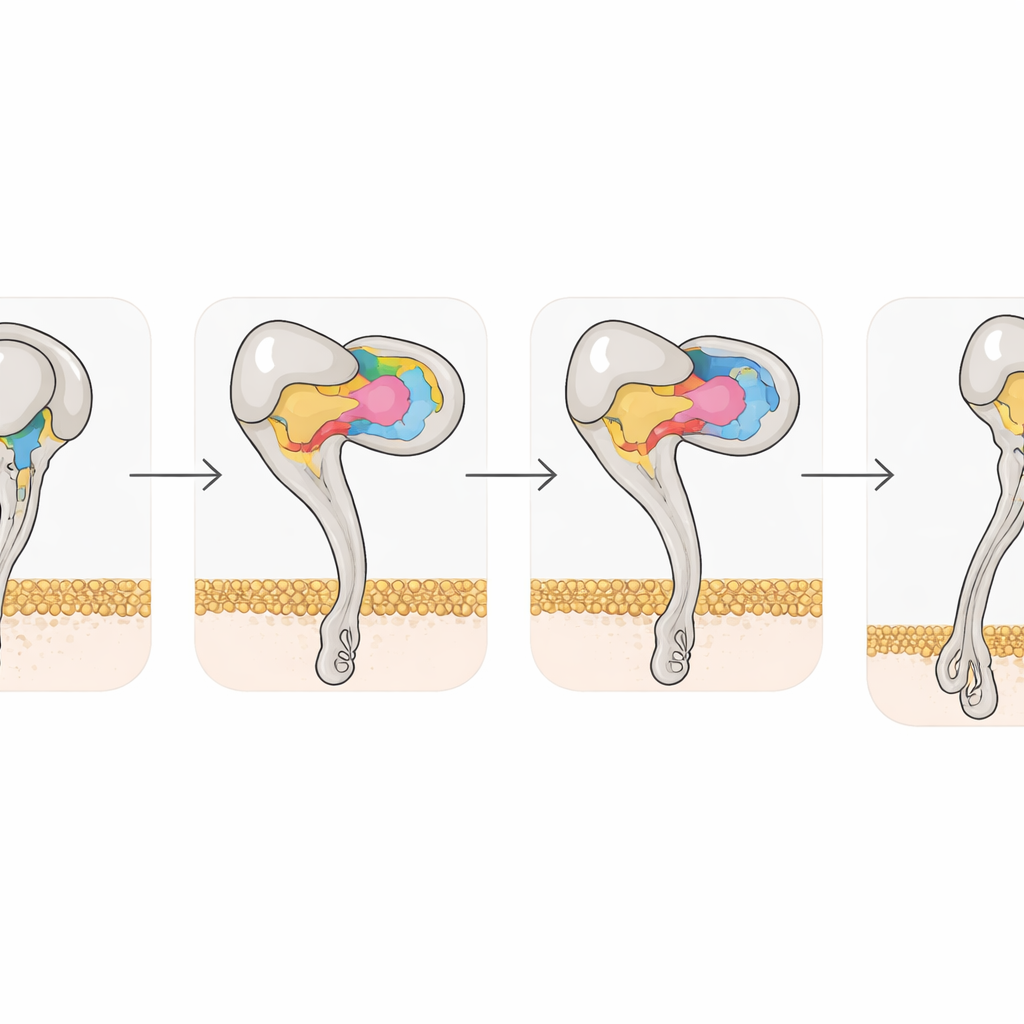
構造のスナップショットはまた、ディスインテグリン結合がインテグリン自体をどのように再形成するかを捉えました。自由なαvβ3は屈曲した閉じた姿勢を好みますが、RhoやTmuが結合すると、受容体のβ3側で二本のヘリックスと金属結合部位に協調的変位が生じ、受容体は高活性に関連する完全に伸長した開いた状態へと駆動されます。しかしβ3のチロシン110という一つのアミノ酸は二つのドメインを橋渡しして屈曲形を保つのに寄与します。研究者らがこの残基をアラニンに変異させると、受容体は自発的に伸長状態を好み、自然の結合相手であるビトロネクチンへの結合が強まりました。これは微細な原子レベルの変化がインテグリンの活性化を調整し得ることを示し、改変型が新薬のスクリーニングに有用なツールとなる可能性を示唆します。
毒の手がかりから将来の抗がん薬へ
総じて、この研究は中程度のサイズの毒性ディスインテグリンが、三つの協調する接触領域と剛直な結合ループを用いることでαvβ3を標的とする効率的な足場を提供し、単純なRGDベース分子よりも優れた性能を示すことを明らかにしました。TmuとRhoが受容体にどのように結合し、小さな配列変化がどのようにその結合を変えるかを正確に写し取ることで、本研究はαvβ3により選択的で出血などの副作用が出にくい次世代インテグリン阻害剤を設計するための構造的な設計図を提供します。要するに、ヘビが私たちの細胞接着機構を精緻に無力化する仕組みを学ぶことで、研究者たちはこれら天然の“武器”をがんや炎症性疾患に対する標的治療へと転用する新たな着想を得るのです。
引用: Wang, YT., Chang, YT., Huang, CH. et al. Structural basis for the differential recognition of integrin αvβ3 by rhodostomin and trimucrin. Commun Biol 9, 583 (2026). https://doi.org/10.1038/s42003-026-10139-6
キーワード: インテグリン αvβ3, ヘビ毒のディスインテグリン, ロドストミン トリムクリン, がんと血管新生, クライオ電子顕微鏡