Clear Sky Science · fr
Base structurale de la reconnaissance différentielle de l’intégrine αvβ3 par la rhodostomine et la trimucrine
Des protéines de venin transformées en outils de médecine de précision
Le venin de serpent évoque la toxicité pure, mais certaines de ses molécules sont étonnamment efficaces pour bloquer des protéines impliquées dans des maladies chez l’homme. Cette étude examine comment deux de ces molécules dérivées du venin se lient à un récepteur clé à la surface des cellules, lié au cancer et à la formation de vaisseaux sanguins, dévoilant des détails atomiques qui pourraient orienter la conception de médicaments plus sûrs et plus ciblés.
Une prise cellulaire que le cancer sait exploiter
Nos cellules utilisent des « prises » protéiques appelées intégrines pour s’attacher à leur environnement et percevoir des signaux mécaniques et chimiques. Une intégrine particulière, nommée αvβ3, aide les cellules à répondre à leur milieu et joue un rôle majeur dans la croissance de nouveaux vaisseaux, l’expansion tumorale, la dissémination des cellules cancéreuses et la résistance aux traitements. Pour ces raisons, αvβ3 a été une cible de longue date pour des médicaments anticancéreux et anti-angiogéniques. Pourtant, des décennies de recherche n’ont abouti à aucun inhibiteur d’αvβ3 approuvé pour l’usage humain, en partie parce qu’il a été difficile de comprendre précisément comment différentes molécules se lient à ce récepteur et le contrôlent.
Pourquoi les molécules du venin sont si puissantes
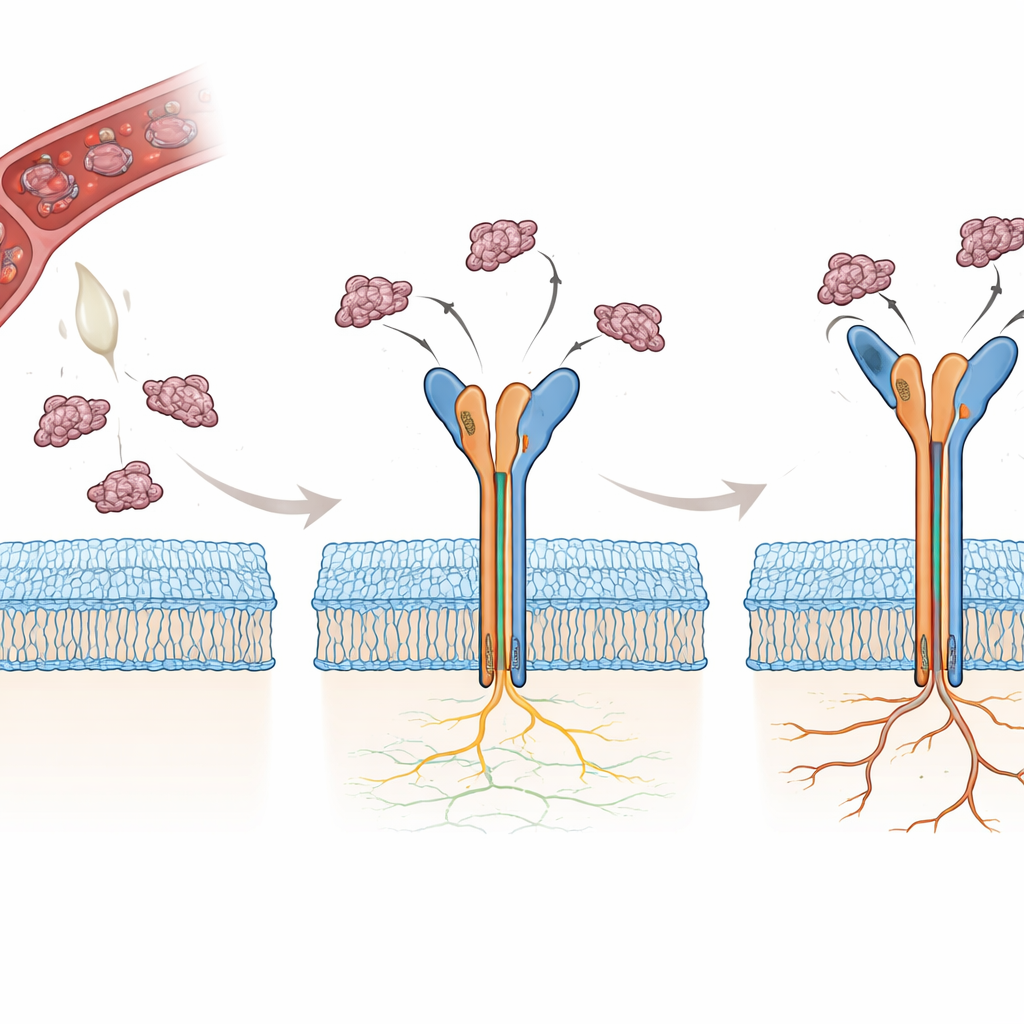
De nombreux serpents produisent de petites protéines appelées disintégrines qui bloquent naturellement les intégrines, empêchant la coagulation et perturbant l’adhésion cellulaire. Deux de ces disintégrines, la rhodostomine (Rho) et la trimucrine (Tmu), contiennent toutes deux une courte séquence de trois acides aminés — arginine-glycine-aspartate, ou RGD — reconnue par αvβ3. De manière surprenante, Tmu inhibe cet intégrine environ trois à quatre fois mieux que Rho. Les deux molécules partagent la majeure partie de leur séquence mais diffèrent en trois régions clés : un linker court, la boucle flexible contenant le motif RGD, et l’extrémité C-terminale de la protéine. Les auteurs ont cherché à déterminer, atome par atome, comment ces petites différences modifient la manière dont chaque protéine du venin saisit αvβ3 et pourquoi Tmu constitue un inhibiteur plus puissant.
Capturer les structures avec grand niveau de détail
Pour répondre à ces questions, les chercheurs ont d’abord résolu la structure cristalline de Tmu seule à très haute résolution, confirmant qu’elle forme un échafaudage compact et rigide stabilisé par six ponts disulfure. Ils ont ensuite utilisé la cryomicroscopie électronique pour déterminer des structures tridimensionnelles d’αvβ3 liée soit à Rho soit à Tmu, atteignant des résolutions inférieures à trois angströms pour la tête du récepteur où a lieu la liaison. Dans les deux cas, la disintégrine s’installe dans une cavité entre deux domaines de la tête de l’intégrine, insérant sa boucle RGD dans un site contenant un métal. La conformation de l’ossature de Rho et Tmu dans cette région est presque identique, montrant que les deux protéines arrivent déjà préformées dans une configuration prête à se lier, plutôt que d’avoir à subir de grandes réarrangements pour engager le récepteur.
Trois zones de contact et une pince plus forte
Un examen plus attentif a révélé que la liaison ne dépend pas du triplet RGD seul. Les deux disintégrines utilisent trois zones de contact coopératives : la boucle RGD elle-même ; une région de linker voisine ; et la queue C-terminale. Dans Tmu, un amas d’acides aminés chargés positivement dans le linker établit des contacts électrostatiques supplémentaires avec la surface chargée négativement de la sous-unité β3, ce qui aide la molécule à se verrouiller plus fermement sur αvβ3. Rho, en revanche, s’appuie davantage sur sa région terminale pour des contacts additionnels. Lorsque l’équipe a échangé des segments de séquence spécifiques entre les deux protéines du venin, elle a pu augmenter ou diminuer leur pouvoir bloquant. En particulier, le transfert du linker chargé de Tmu dans Rho a multiplié par environ dix la capacité de Rho à inhiber αvβ3, confirmant que ce patch de liaison supplémentaire est un contributeur majeur à la puissance inhibitrice.
Comment la liaison active le récepteur — et l’importance d’un seul atome
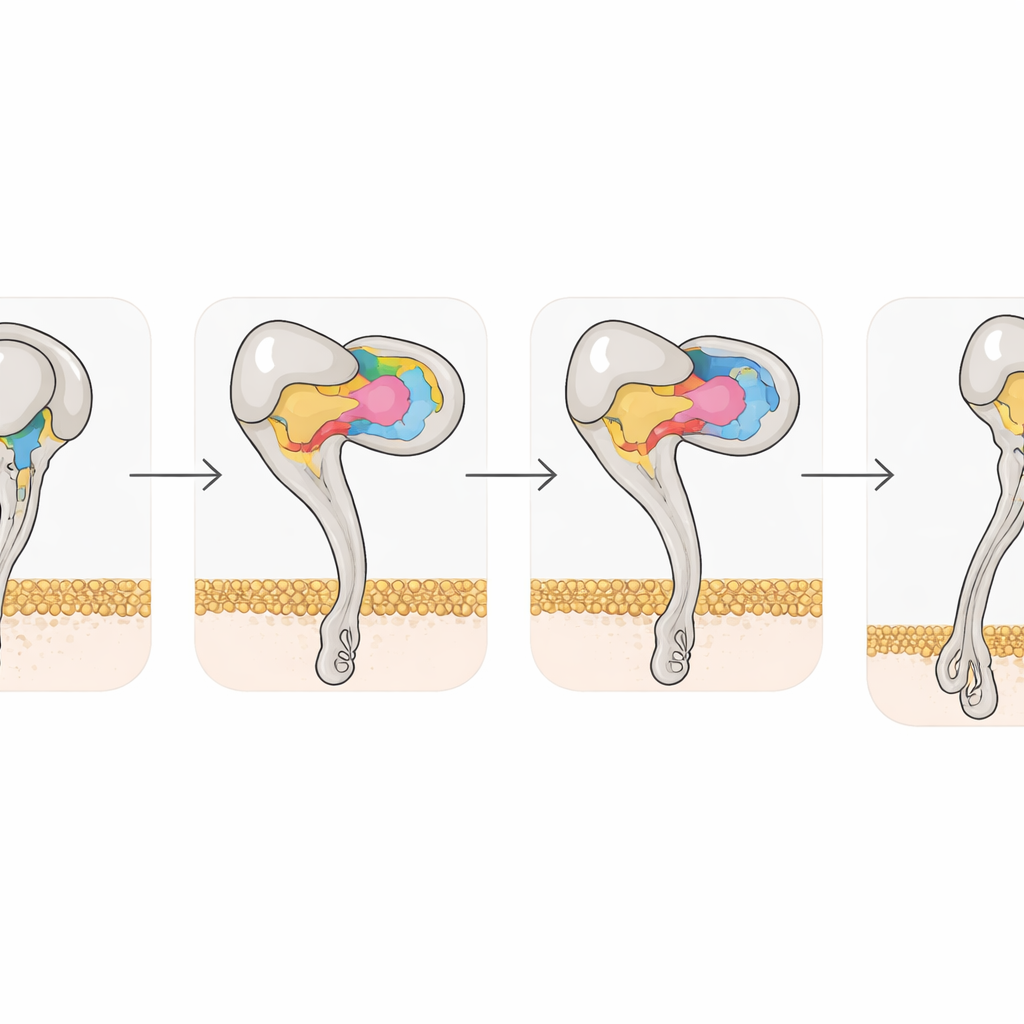
Les instantanés structurels ont également montré comment la liaison des disintégrines reconfigure l’intégrine elle-même. L’αvβ3 libre préfère une posture pliée et fermée ; une fois Rho ou Tmu liés, la moitié β3 du récepteur subit des déplacements coordonnés dans deux hélices et des sites de liaison aux métaux, entraînant le récepteur vers un état complètement étendu et ouvert associé à une forte activité. Pourtant, un seul acide aminé, la tyrosine 110 dans β3, contribue à maintenir la forme pliée en faisant le pont entre deux domaines. Lorsque les chercheurs ont muté ce résidu en alanine, le récepteur a spontanément favorisé l’état étendu et s’est lié plus fortement à son partenaire naturel, la vitronectine. Cela illustre comment de subtiles modifications atomiques peuvent régler l’activation des intégrines et suggère que des variantes conçues pourraient servir d’outils utiles pour le criblage de nouveaux médicaments.
Des indices tirés du venin vers de futurs médicaments anticancéreux
Dans l’ensemble, le travail montre que les disintégrines de taille moyenne issues du venin fournissent un échafaudage très efficace pour cibler αvβ3, utilisant trois régions de contact coordonnées et une boucle de liaison rigide pour surpasser les simples molécules basées sur le motif RGD. En cartographiant précisément comment Tmu et Rho engagent le récepteur — et comment de petits changements de séquence modifient cet engagement — l’étude offre une feuille de route structurale pour concevoir des inhibiteurs d’intégrine de nouvelle génération plus sélectifs pour αvβ3 et moins susceptibles de provoquer des saignements ou d’autres effets indésirables. En substance, en apprenant comment les serpents désactivent notre machinerie d’adhésion cellulaire avec une précision remarquable, les scientifiques obtiennent de nouvelles idées pour transformer ces armes naturelles en thérapies ciblées contre le cancer et les maladies inflammatoires.
Citation: Wang, YT., Chang, YT., Huang, CH. et al. Structural basis for the differential recognition of integrin αvβ3 by rhodostomin and trimucrin. Commun Biol 9, 583 (2026). https://doi.org/10.1038/s42003-026-10139-6
Mots-clés: intégrine alpha v beta 3, disintégrines de venin de serpent, rhodostomine trimucrine, cancer et angiogenèse, cryomicroscopie électronique