Clear Sky Science · es
Base estructural para el reconocimiento diferencial de la integrina αvβ3 por rodostomina y trimucrina
Proteínas de veneno reconvertidas en herramientas de medicina de precisión
El veneno de serpiente puede sonar a puro veneno, pero algunas de sus moléculas son extraordinariamente eficaces bloqueando proteínas vinculadas a enfermedades en nuestro organismo. Este estudio explora cómo dos de esas moléculas derivadas del veneno se adhieren a un receptor clave en la superficie celular relacionado con el cáncer y el crecimiento de vasos sanguíneos, revelando detalles a nivel atómico que podrían orientar el diseño de fármacos más precisos y seguros.
Una sujeción celular que el cáncer aprende a explotar
Nuestras células usan “sujetadores” proteicos llamados integrinas para anclarse al entorno y percibir señales mecánicas y químicas. Una integrina en particular, denominada αvβ3, ayuda a las células a responder a su entorno y desempeña un papel importante en el crecimiento de nuevos vasos sanguíneos, la expansión tumoral, la diseminación de células cancerosas y la resistencia a fármacos. Por ello, αvβ3 ha sido desde hace tiempo un objetivo para fármacos antitumorales y antiangiogénicos. Sin embargo, décadas de trabajo no han producido bloqueadores de αvβ3 aprobados para uso humano, en parte porque ha sido difícil entender exactamente cómo distintas moléculas se unen y modulan este receptor.
Por qué las moléculas del veneno son tan potentes
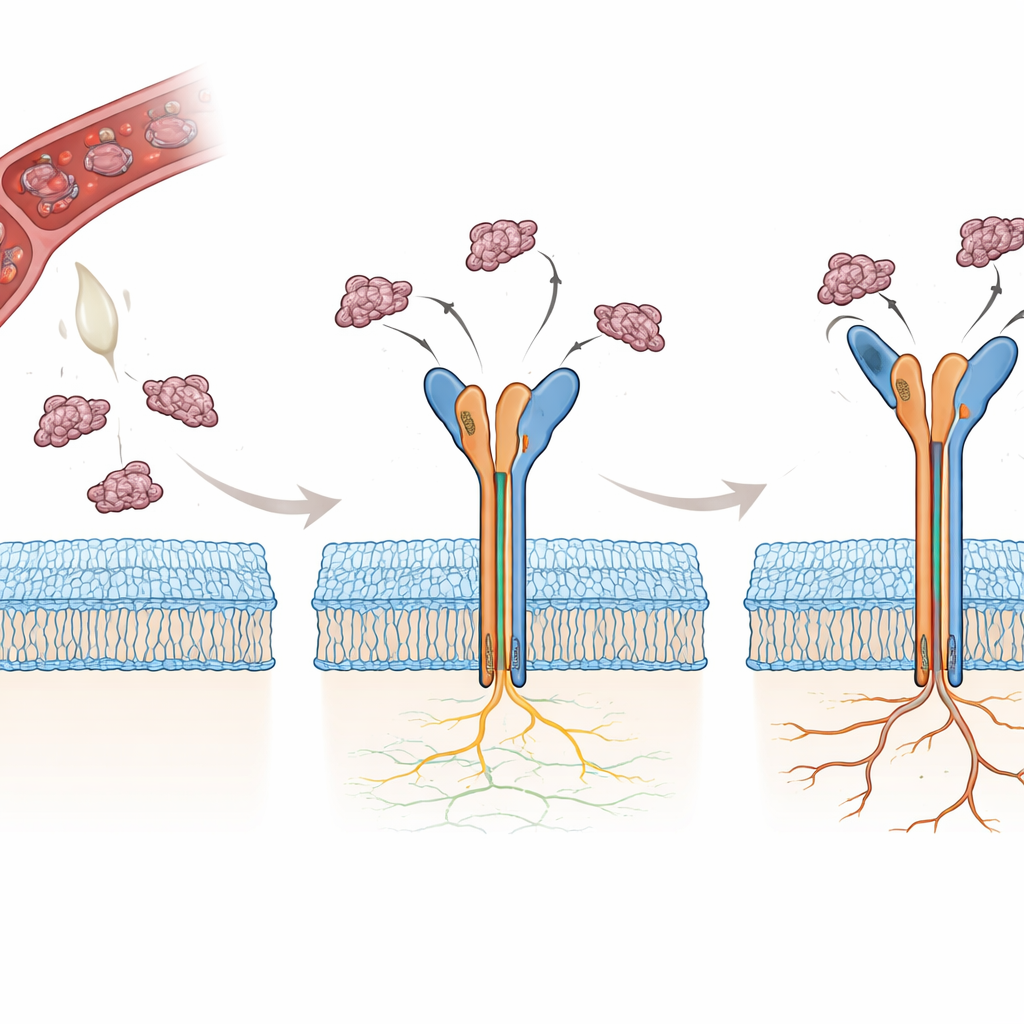
Muchas serpientes producen pequeñas proteínas llamadas disintegrinas que bloquean de forma natural a las integrinas, impidiendo la coagulación y perturbando la adhesión celular. Dos de estas disintegrinas, rodostomina (Rho) y trimucrina (Tmu), contienen una secuencia corta de tres aminoácidos —arginina-glicina-ácido aspártico, o RGD— que es reconocida por αvβ3. Sorprendentemente, Tmu es aproximadamente tres o cuatro veces mejor que Rho bloqueando esta integrina. Las dos moléculas comparten la mayor parte de su secuencia, pero difieren en tres regiones clave: un enlazador corto, el bucle flexible que contiene el RGD y el extremo C-terminal de la proteína. Los autores se propusieron determinar, átomo por átomo, cómo estas pequeñas diferencias modifican la forma en que cada proteína del veneno sujeta a αvβ3 y por qué eso convierte a Tmu en un inhibidor más potente.
Capturando las estructuras con gran detalle
Para responder a estas preguntas, los investigadores primero resolvieron la estructura cristalina de Tmu sola con muy alta resolución, confirmando que forma un armazón compacto y rígido estabilizado por seis enlaces disulfuro. Luego emplearon criomicroscopía electrónica para determinar estructuras tridimensionales de αvβ3 unida tanto a Rho como a Tmu, alcanzando resoluciones inferiores a tres angstroms en la cabeza del receptor donde se produce la unión. En ambos casos, la disintegrina se sitúa en una hendidura entre dos dominios de la cabeza de la integrina, introduciendo su bucle RGD en un sitio que contiene metal. La conformación del esqueleto de Rho y Tmu en esta región es casi idéntica, lo que muestra que ambas proteínas llegan preformadas en una geometría preparada para unirse, en lugar de sufrir grandes reorganizaciones al interactuar con el receptor.
Tres zonas de contacto y una abrazadera más fuerte
Una inspección más cercana reveló que la unión no está regida únicamente por el triplete RGD. Ambas disintegrinas usan tres zonas de contacto cooperativas: el propio bucle RGD; una región de enlazador próxima; y la cola C-terminal. En Tmu, un grupo de aminoácidos cargados positivamente en el enlazador establece contactos electrostáticos adicionales con la superficie negativamente cargada de la subunidad β3, lo que le ayuda a sujetar con más fuerza a αvβ3. Rho, en cambio, depende más de su región terminal para contactos extra. Cuando el equipo intercambió segmentos de secuencia específicos entre las dos proteínas del veneno, pudieron modular la potencia del bloqueo. En particular, transferir el enlazador cargado de Tmu a Rho aumentó la capacidad de Rho para inhibir αvβ3 en aproximadamente diez veces, confirmando que este parche de unión adicional es un contribuyente principal a la potencia.
Cómo la unión activa el receptor—y cómo importa un solo átomo
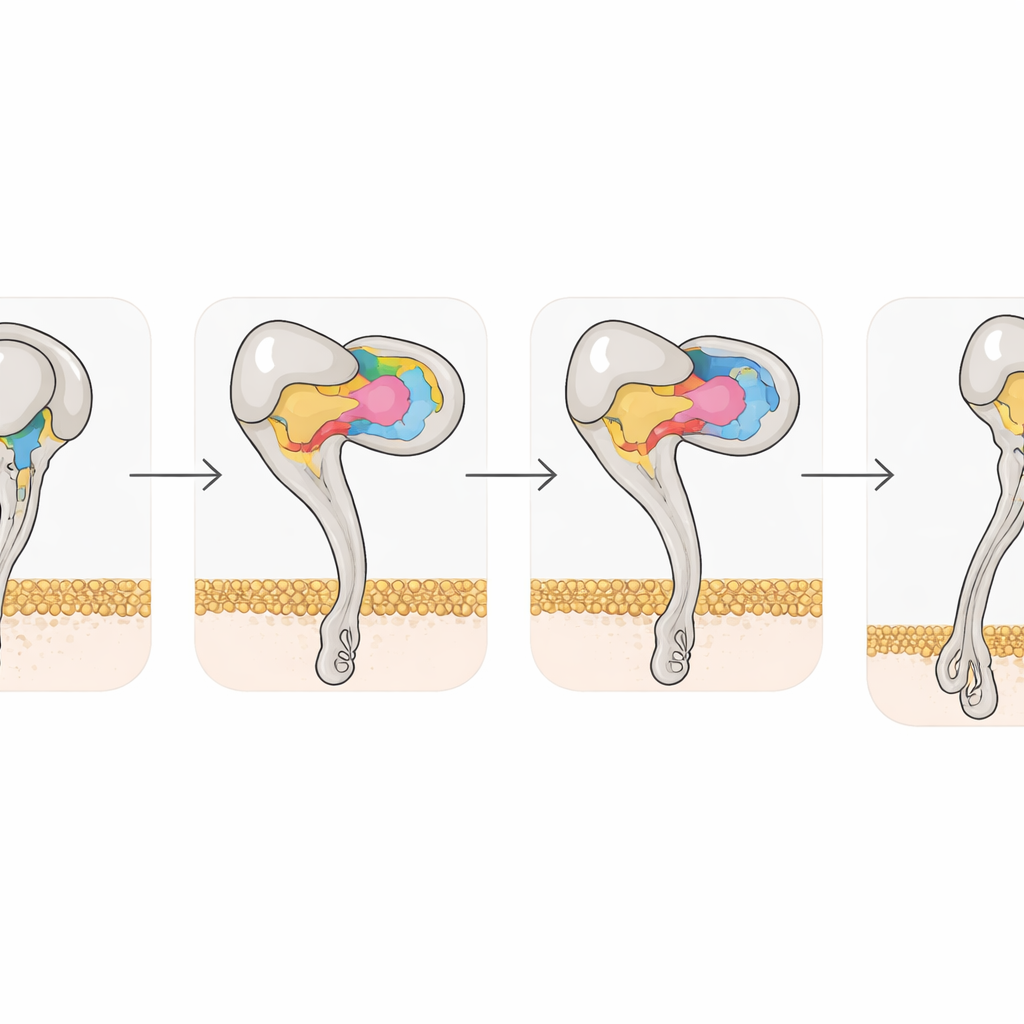
Las instantáneas estructurales también captaron cómo la unión de la disintegrina remodela la propia integrina. La αvβ3 libre prefiere una postura doblada y cerrada; cuando Rho o Tmu se unen, la mitad β3 del receptor experimenta desplazamientos coordinados en dos hélices y en sitios de unión a metales, impulsando al receptor hacia un estado completamente extendido y abierto asociado a alta actividad. No obstante, un único aminoácido, la tirosina 110 en β3, ayuda a mantener unida la forma doblada haciendo de puente entre dos dominios. Cuando los investigadores mutaron este residuo a alanina, el receptor favoreció espontáneamente el estado extendido y se unió con más fuerza a su pareja natural, la vitronectina. Esto subraya cómo cambios atómicos sutiles pueden ajustar la activación de integrinas y sugiere que variantes diseñadas podrían ser herramientas útiles para cribar nuevos fármacos.
De las pistas del veneno a futuros fármacos contra el cáncer
En conjunto, el trabajo muestra que las disintegrinas de tamaño medio derivadas del veneno proporcionan un andamio muy eficiente para dirigir selectivamente a αvβ3, usando tres regiones de contacto coordinadas y un bucle de unión rígido para superar a las moléculas basadas solo en RGD. Al mapear con precisión cómo Tmu y Rho interactúan con el receptor—y cómo pequeños cambios de secuencia modifican esa interacción—el estudio ofrece un plano estructural para diseñar bloqueadores de integrinas de nueva generación que sean más selectivos para αvβ3 y menos propensos a causar sangrado u otros efectos secundarios. En esencia, al aprender cómo las serpientes desactivan con exquisita precisión nuestra maquinaria de adhesión celular, los científicos obtienen nuevas ideas para convertir estas armas naturales en terapias dirigidas contra el cáncer y la inflamación.
Cita: Wang, YT., Chang, YT., Huang, CH. et al. Structural basis for the differential recognition of integrin αvβ3 by rhodostomin and trimucrin. Commun Biol 9, 583 (2026). https://doi.org/10.1038/s42003-026-10139-6
Palabras clave: integrina alfa v beta 3, disintegrinas de veneno de serpiente, rodostomina trimucrina, cáncer y angiogénesis, criomicroscopía electrónica