Clear Sky Science · tr
T hücreli akut lenfoblastik lösemide epigenetik ilaç yanıt imzalarını tanımlamak için histon sonrası translasyonel modifikasyonların profillenmesi
Bu kanser çalışması neden önemli
T hücreli akut lenfoblastik lösemili çocuklar ve yetişkinler için tedavi büyük ölçüde ilerledi, ancak birçok hasta yine de nüksediyor veya yoğun kemoterapinin ciddi yan etkileriyle karşılaşıyor. Hekimlerin hangi ilacın hangi hasta için işe yarayacağını daha iyi tahmin etme yöntemlerine ihtiyacı var. Bu çalışma, lösemi hücrelerindeki DNA paketleme proteinleri üzerindeki küçük kimyasal etiketlerin, hücrenin epigenetik mekanizmasına etki eden modern kanser ilaçlarına nasıl yanıt verdiğini öngörmede yardımcı olup olamayacağını araştırıyor.
DNA paketleme üzerindeki gizli kod
Her lösemi hücresinin içinde DNA, histon adı verilen proteinlerin etrafına sarılarak kromatin adı verilen sıkışık bir yapı oluşturur. Histonlar, genleri temel DNA dizisini değiştirmeden açıp kapamaya yardımcı olan birçok küçük kimyasal etiketi taşır. Bu etiketler geri çevrilebilir oldukları için ilaç hedefi olmaya elverişlidir. Birkaç böyle “epilaç” kan hastalıklarında zaten kullanılıyor, ancak T hücreli lösemide rolleri hâlâ net değil ve doktorların kimlerin bundan yararlanacağını öngörebilecek basit işaretçilere ihtiyacı bulunuyor.
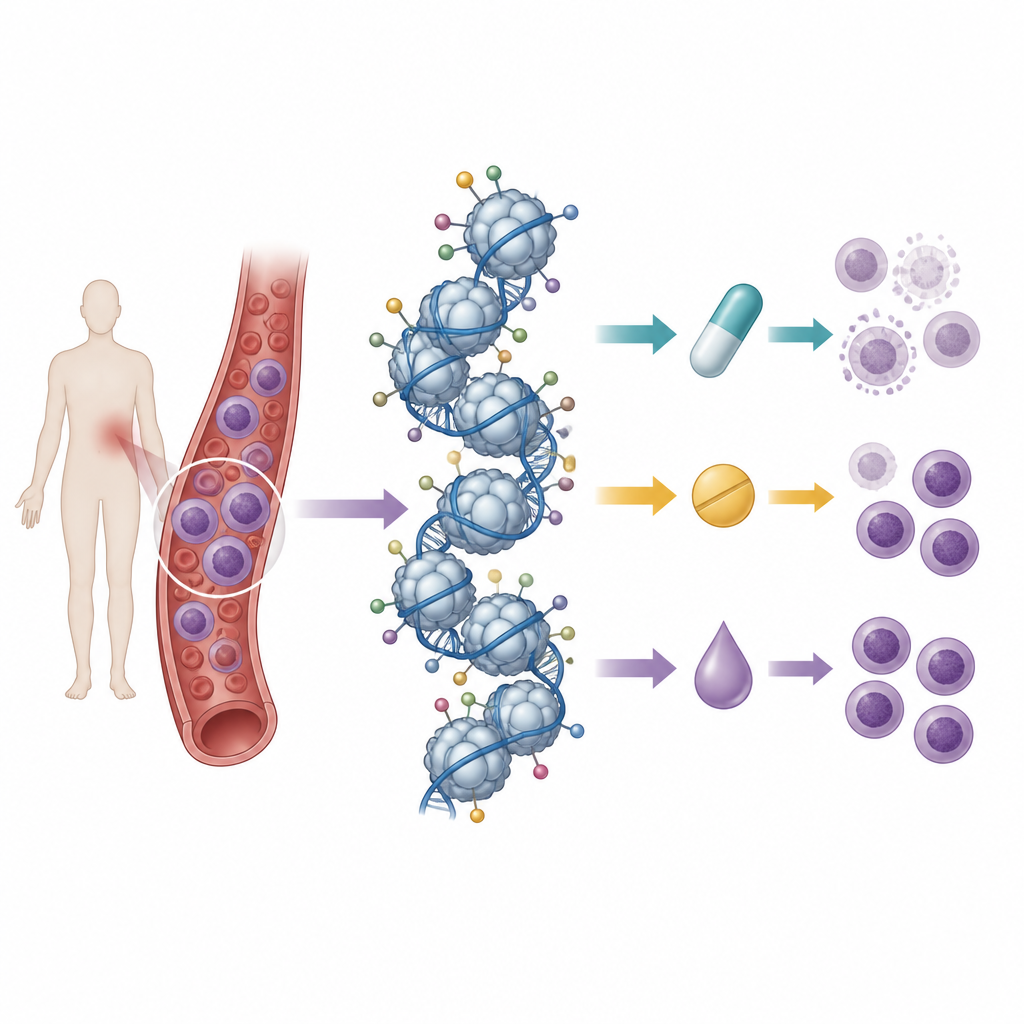
Aynı anda birçok histon işaretini okumak
Araştırmacılar, daha önce 21 T hücre lösemi hücre hattında kütle spektrometrisi kullanarak başlangıç histon etiketi desenlerini haritaladıkları çalışmayı temel aldı; bu teknik yüzlerce kimyasal işareti aynı anda ölçebilir. Ardından bu hücre hatlarını dokuz ilaçla tedavi ettiler: üç standart kemoterapi antrasiklin, üç histon deasetilazları bloke eden ilaç ve üçü DNA metilasyon enzimlerini inhibe eden ilaç. Tedavi sonrası hücre sağkalımını başlangıçtaki histon desenleriyle karşılaştırarak, her ilaca duyarlılık veya dirençle ilişkilenen “imzalar” aradılar.
Hücre hatlarının ortaya koydukları
Kültürdeki hücrelerde, belirgin histon imzaları ortaya çıktı. Antrasiklin ilaçları için H3K27me3 gibi bazı baskılayıcı işaretler daha duyarlı hatlarda genellikle daha yüksekken, özellikle birkaç dimetil grubuna ait işaretler daha kötü yanıtla ilişkilendirildi. DNA metilasyonunu hedef alan ilaçlar için bazı dimetil işaretlerin yüksek düzeyleri yine dirence işaret ederken, histon kuyruklarındaki asetil işaretleri daha iyi yanıtla ilişkilendirildi. Histon deasetilaz inhibitörleri, duyarlı ve dirençli hücre hatları arasında daha zayıf bir ayrım gösterdi, ancak en az veya en çok yanıt veren hücrelerde zenginleşmiş bazı spesifik desenler yine de gözlendi. Genel olarak bu bulgular, tek bir işaretten ziyade histon etiketlerinin birleşik manzarasının lösemi hücrelerinin epigenetik ilaçlara nasıl yanıt verdiği konusunda bilgi taşıdığını öne sürdü.
Tek bir işareti teste sokmak
Önceki çalışmalar aclarubicin’in özellikle H3K27me3 bakımından zengin hücrelerde iyi işlediğini öne sürdüğünden, ekip bu fikri doğrudan test etti. Bu işareti oluşturan enzimi bloke etmek için başka bir ilaç kullandılar ve birkaç T hücre lösemi hattında H3K27me3 düzeylerini başarıyla düşürdüler. Şaşırtıcı bir şekilde, bu hücrelerin aclarubicin’e duyarlılığı değişmedi. Ayrıca doğal olarak yüksek H3K27me3’ye sahip olup dirençli olan hücre hatları da gözlemlediler. Bu, tek bir histon etiketinin bazı bağlamlarda ilaç yanıtıyla ilişkilense bile duyarlılığı tek başına açıklamak için yeterli olmadığını gösterdi.
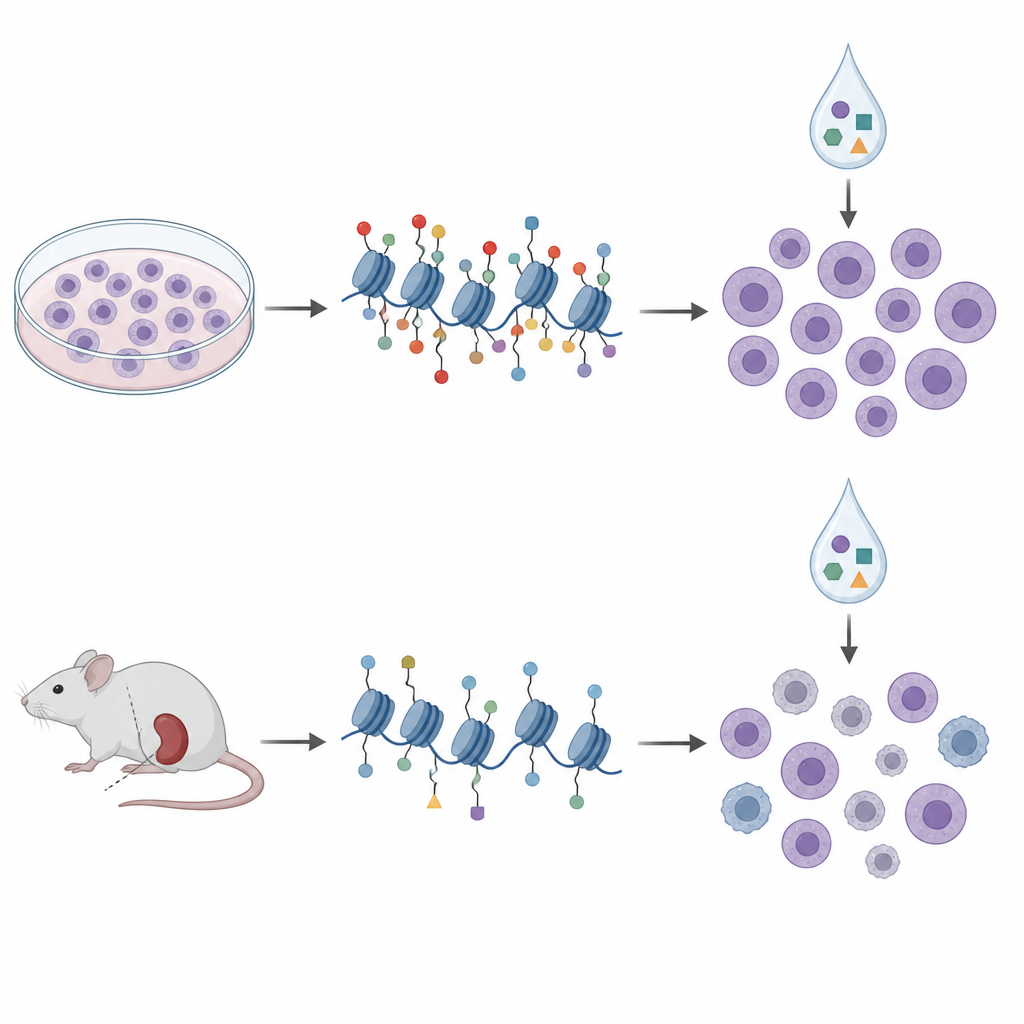
Besiyerlerinden fare modellerine
Kliniğe daha yakın bir değerlendirme yapmak için araştırmacılar, lösemi hücrelerinin hastalardan alınıp bağışıklık yetmez farelerde büyütüldüğü hasta kaynaklı ksenogreftlere (PDX) yöneldiler. On böyle modelden hücrelerde histon işaretlerini ve DNA metilasyonunu profillediler ve benzer bir epigenetik ilaç paneliyle vücut dışı olarak tedavi ettiler. Bu örneklerde histon desenleri büyük ölçüde bilinen genetik alt tipleri ve daha geniş DNA metilasyon durumlarını yansıtan dört kümeye ayrıldı; bu, histon profilinin anlamlı hastalık biyolojisini yakaladığını gösterdi. Ancak histon işaretlerini ilaç duyarlılığıyla tekrar karşılaştırdıklarında, hücre hatlarından elde edilen imzalar aktarılamadı. Aslında bazı ilişkiler tersine döndü; besiyerindeki hücrelerde aclarubicin duyarlılığına işaret eden aynı H3K27me3 işareti, fare kaynaklı hücrelerde daha düşük duyarlılıkla ilişkilendirildi.
Sabit bir kod değil, değişen bir ağ
Bu uyumsuzluğu anlamak için ekip, farklı histon işaretlerinin modeller arasında birlikte nasıl yükselip düştüğünü inceledi. Hasta kaynaklı örneklerde birçok işaret sıkı bir koordinasyon içinde hareket ederek pozitif korelasyonlardan oluşan yoğun bir ağ oluştururken, hücre hatlarında bu ağ daha gevşek ve parçalanmıştı. Bazı işaretler bir sistemde ağların merkezinde yer alırken diğerinde yer almıyordu. Bu desenler, histon etiketlerinin komşularına ve hücresel ortama bağlı olarak anlam kazanan bağlama bağımlı bir dilin parçası olarak çalıştığı görüşünü destekliyor. Uzun süreli besiyerinde büyüme, bu dili yeniden kablolayarak histon desenlerinin ilaç yanıtıyla ilişkisini değiştirmiş gibi görünüyor.
Gelecekteki lösemi bakımına etkileri
Bu çalışma, kütle spektrometrisi kullanarak T hücreli lösemide histon etiketlerinin zengin manzarasını okuma ve bunları hücrelerin epigenetik ilaçlarla nasıl başa çıktığıyla ilişkilendirme çerçevesi sunuyor. Aynı zamanda uyarıcı bir mesaj veriyor: standart hücre hatlarından elde edilen sonuçlar, daha gerçekçi hasta kaynaklı modellerde veya insanlarda yanıtları güvenilir şekilde öngörmeyebilir. Histon tabanlı biyobelirteçlerin kişiye özel tedavileri yönlendirebilmesi için araştırmacıların bu karmaşıklığı kabul etmeleri, işaret kombinasyonlarına odaklanmaları ve hastaların biyolojisini olabildiğince yakından yansıtan hastalık modellerini dikkatle seçmeleri gerekecek.
Atıf: Corveleyn, L., Provez, L., Satilmis, O. et al. Profiling histone post-translational modifications to identify signatures of epigenetic drug response in T-cell acute lymphoblastic leukemia. Sci Rep 16, 15029 (2026). https://doi.org/10.1038/s41598-026-44665-4
Anahtar kelimeler: T hücreli akut lenfoblastik lösemi, epigenetik ilaçlar, histon modifikasyonları, hasta kaynaklı ksenogreftler, ilaç yanıt biyobelirteçleri