Clear Sky Science · fr
Profilage des modifications post-traductionnelles des histones pour identifier les signatures de réponse aux médicaments épigénétiques dans la leucémie aiguë lymphoblastique T
Pourquoi cette étude sur le cancer est importante
Les traitements pour les enfants et les adultes atteints de leucémie aiguë lymphoblastique T se sont grandement améliorés, mais de nombreux patients rechutent encore ou subissent des effets secondaires graves liés à des chimiothérapies intenses. Les médecins ont besoin de meilleurs moyens pour prévoir quel traitement fonctionnera pour quel patient. Cette étude examine si de petites marques chimiques sur les protéines qui emballent l’ADN dans les cellules leucémiques peuvent aider à prédire la façon dont ces cellules répondent aux médicaments anticancéreux modernes qui ciblent la machinerie épigénétique de la cellule.
Le code caché sur l’emballage de l’ADN
À l’intérieur de chaque cellule leucémique, l’ADN est enroulé autour de protéines appelées histones, formant une structure compacte connue sous le nom de chromatine. Les histones portent de nombreuses petites marques chimiques qui agissent comme des interrupteurs, aidant à activer ou à désactiver des gènes sans modifier la séquence d’ADN sous-jacente. Parce que ces marques sont réversibles, elles constituent des cibles attractives pour des médicaments. Plusieurs de ces « épidrugs » sont déjà utilisés dans les cancers du sang, mais leur rôle dans la leucémie T reste flou, et les cliniciens manquent de marqueurs simples pour prédire qui en bénéficiera.
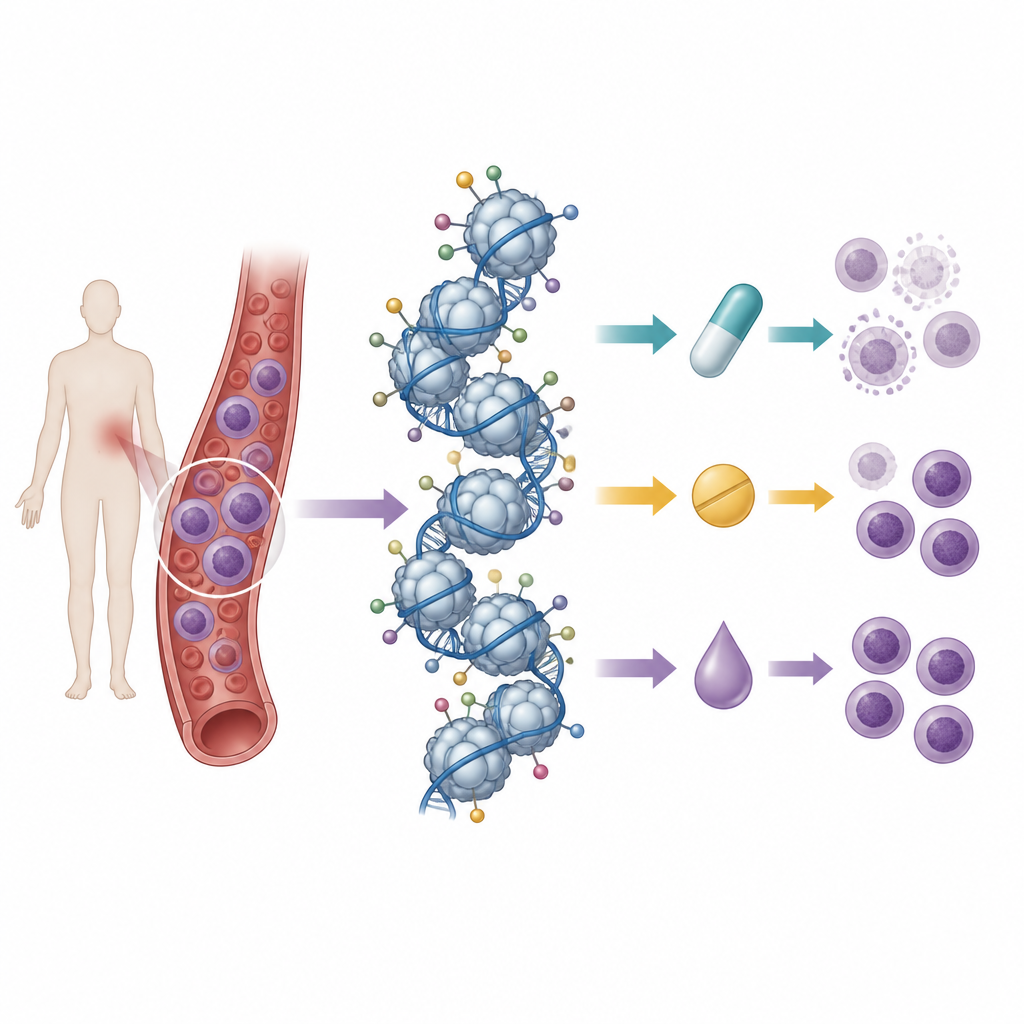
Lire de nombreuses marques d’histones à la fois
Les chercheurs ont tiré parti d’un travail antérieur dans lequel ils avaient cartographié le motif de base des marques d’histones dans 21 lignées cellulaires de leucémie T en utilisant la spectrométrie de masse, une technique capable de mesurer des centaines de marques chimiques simultanément. Ils ont ensuite traité ces lignées cellulaires avec neuf médicaments : trois anthracyclines chimiothérapeutiques classiques, trois inhibiteurs des histone désacétylases, et trois inhibiteurs des enzymes de méthylation de l’ADN. En comparant la survie cellulaire après traitement aux profils initiaux des histones, ils ont recherché des « signatures » de marques corrélant avec la sensibilité ou la résistance à chaque médicament.
Ce que les lignées cellulaires ont révélé
Dans les cultures cellulaires, des signatures d’histones distinctes ont émergé. Pour les anthracyclines, certaines marques répressives, comme une appelée H3K27me3, avaient tendance à être plus élevées dans les lignées plus sensibles, tandis que d’autres marques, en particulier plusieurs diméthylations, étaient associées à une moins bonne réponse. Pour les médicaments ciblant la méthylation de l’ADN, des niveaux élevés de certaines diméthylations indiquaient à nouveau une résistance, alors que les marques d’acétylation sur les queues d’histones s’associaient à une meilleure réponse. Les inhibiteurs des histone désacétylases montraient une séparation plus faible entre lignées sensibles et résistantes, mais certains motifs persistaient, incluant des marques spécifiques enrichies soit dans les cellules les moins réactives soit dans les plus réactives. Globalement, ces résultats suggèrent que le paysage combiné des marques d’histones, plutôt qu’une marque unique, porte l’information sur la manière dont les cellules leucémiques répondent aux médicaments épigénétiques.
Mettre à l’épreuve une marque unique
Comme des travaux antérieurs avaient suggéré que l’aclarubicine fonctionne particulièrement bien dans des cellules riches en la marque H3K27me3, l’équipe a testé directement cette idée. Ils ont utilisé un autre médicament pour bloquer l’enzyme qui ajoute cette marque et ont réussi à diminuer H3K27me3 dans plusieurs lignées de leucémie T. De façon surprenante, cela n’a pas modifié la sensibilité des cellules à l’aclarubicine. Ils ont aussi observé des lignées qui présentaient naturellement des niveaux élevés de H3K27me3 mais qui restaient résistantes. Cela montre que, même lorsqu’une marque d’histone suit la réponse au médicament dans certains contextes, elle n’est pas suffisante à elle seule pour expliquer la sensibilité.
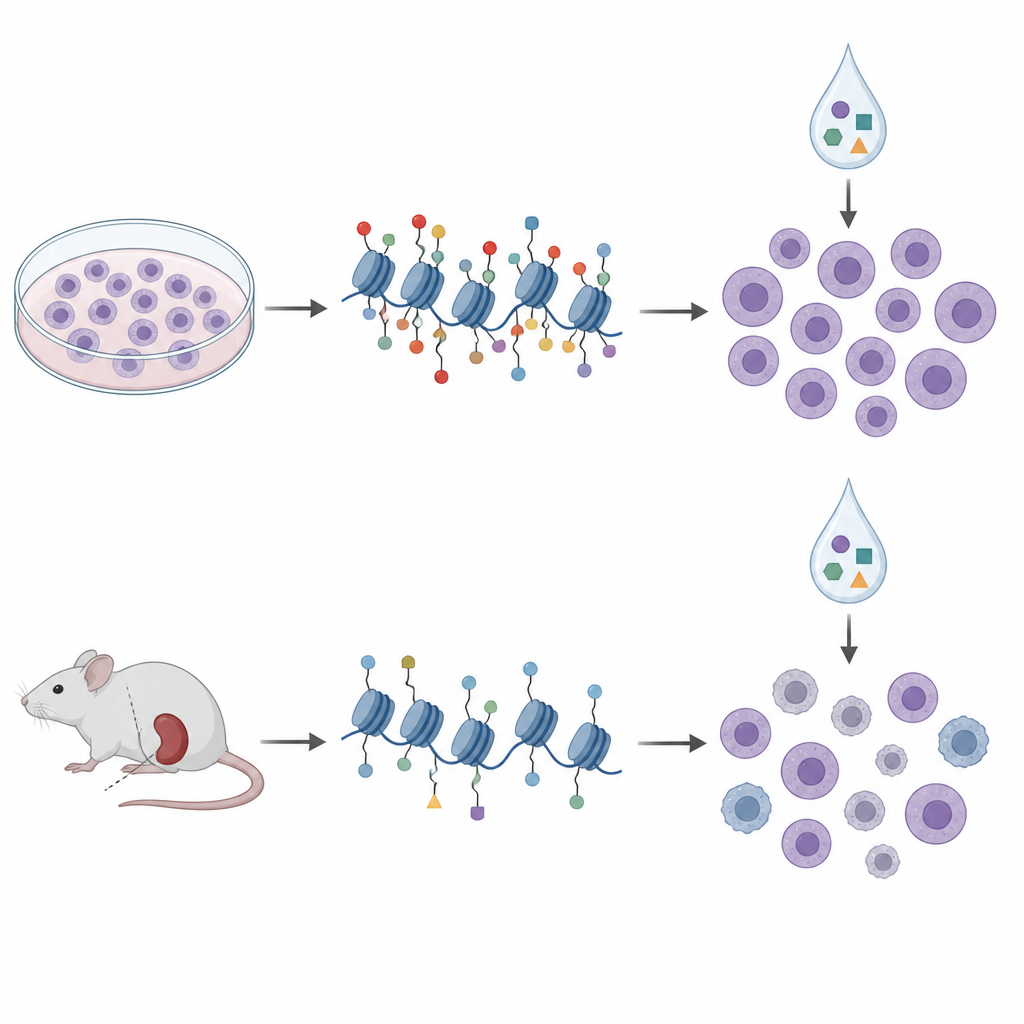
Des boîtes de culture aux modèles murins
Pour se rapprocher de la clinique, les chercheurs se sont tournés vers des xénogreffes dérivées de patients, dans lesquelles des cellules leucémiques issues de patients croissent chez des souris immunodéficientes. Ils ont profilé les marques d’histones et la méthylation de l’ADN dans des cellules provenant de dix de ces modèles et les ont traitées avec un panel similaire d’épidrugs ex vivo. Dans ces échantillons, les motifs d’histones se regroupaient en quatre clusters qui reflétaient en grande partie des sous-types génétiques connus et des états globaux de méthylation de l’ADN, suggérant que le profilage des histones capture une biologie de la maladie pertinente. Mais lorsqu’ils ont de nouveau comparé les marques d’histones à la sensibilité aux médicaments, les signatures observées dans les lignées cellulaires ne se sont pas transférées. En fait, certaines relations s’inversaient ; la même marque H3K27me3 qui indiquait une sensibilité à l’aclarubicine en culture était associée à une sensibilité plus faible dans les cellules dérivées de souris.
Un réseau changeant plutôt qu’un code fixe
Pour comprendre ce décalage, l’équipe a étudié comment différentes marques d’histones augmentent ou diminuent ensemble à travers les modèles. Dans les échantillons dérivés de patients, de nombreuses marques évoluaient en étroite coordination, formant un réseau dense de corrélations positives, tandis que dans les lignées cellulaires ce réseau était plus lâche et fragmenté. Certaines marques occupaient des positions centrales dans ces réseaux dans un système mais pas dans l’autre. Ces motifs soutiennent l’idée que les marques d’histones fonctionnent comme une langue dépendante du contexte, où le sens d’une marque donnée dépend de ses voisines et de l’environnement cellulaire. La croissance prolongée en culture semble reconfigurer cette langue de manières qui modifient la relation entre les profils d’histones et la réponse aux médicaments.
Ce que cela signifie pour les soins futurs de la leucémie
Ce travail propose un cadre pour utiliser la spectrométrie de masse afin de lire le paysage riche des marques d’histones dans la leucémie T et de les relier à la manière dont les cellules réagissent aux médicaments épigénétiques. Il délivre aussi un message de prudence : les résultats obtenus sur des lignées cellulaires standard ne prédisent pas forcément de façon fiable la réponse dans des modèles dérivés de patients, et encore moins chez l’humain. Pour que des biomarqueurs basés sur les histones guident des traitements personnalisés, les chercheurs devront embrasser cette complexité, se concentrer sur des combinaisons de marques et choisir avec soin des modèles de maladie qui reflètent la biologie des patients aussi fidèlement que possible.
Citation: Corveleyn, L., Provez, L., Satilmis, O. et al. Profiling histone post-translational modifications to identify signatures of epigenetic drug response in T-cell acute lymphoblastic leukemia. Sci Rep 16, 15029 (2026). https://doi.org/10.1038/s41598-026-44665-4
Mots-clés: leucémie aiguë lymphoblastique T, médicaments épigénétiques, modifications des histones, xénogreffes dérivées de patients, biomarqueurs de réponse aux médicaments