Clear Sky Science · ru
Профилирование посттрансляционных модификаций гистонов для выявления сигнатур эпигенетического ответа на препараты при Т-клеточном остром лимфобластном лейкозе
Почему это исследование рака важно
Лечение детей и взрослых с Т‑клеточным острым лимфобластным лейкозом значительно улучшилось, однако многие пациенты все еще рецидивируют или испытывают серьёзные побочные эффекты от интенсивной химиотерапии. Врачам нужны более точные способы предсказать, какое лекарство поможет конкретному пациенту. В этом исследовании проверяли, могут ли крошечные химические метки на белках упаковки ДНК в клетках лейкемии предсказывать, как эти клетки отреагируют на современные противораковые препараты, нацеленные на эпигенетические механизмы.
Скрытый код на упаковке ДНК
Внутри каждой клетки лейкемии ДНК намотана на белки, называемые гистонами, формируя компактную структуру — хроматин. На гистонах располагаются многочисленные небольшие химические метки, действующие как переключатели и помогающие включать или выключать гены без изменения самой последовательности ДНК. Поскольку эти метки обратимы, они привлекают внимание как мишени для лекарств. Несколько таких «эпидрог» уже применяются при заболеваниях крови, но их роль при Т‑клеточном лейкозе остается неясной, и врачам не хватает простых маркеров для прогнозирования пользы от терапии.
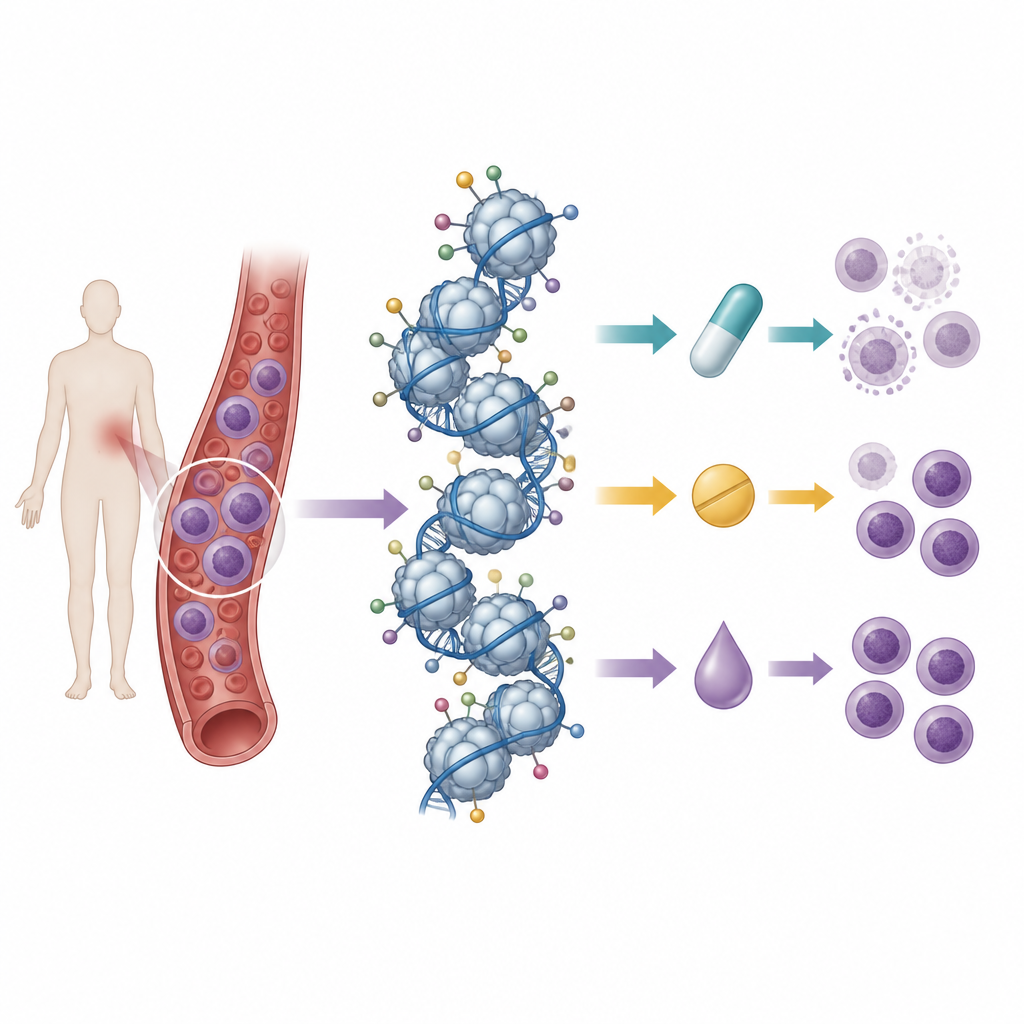
Чтение множества меток гистонов одновременно
Исследователи опирались на предыдущую работу, в которой они картировали базовый паттерн меток гистонов в 21 линии Т‑клеточного лейкоза с помощью масс‑спектрометрии — метода, позволяющего измерять сотни химических меток одновременно. Затем эти линии обрабатывали девятью препаратами: тремя стандартными антрациклиновыми химиопрепаратами, тремя ингибиторами гистондеацетилаз и тремя ингибиторами ферментов метилирования ДНК. Сравнивая выживаемость клеток после лечения с исходными паттернами гистонов, они искали «сигнатуры» меток, которые коррелировали с чувствительностью или устойчивостью к каждому препарату.
Что показали клеточные линии
В культурах клеток действительно выделялись отдельные сигнатуры гистонов. Для антрациклиновых препаратов некоторые репрессивные метки, такие как H3K27me3, чаще встречались в более чувствительных линиях, тогда как другие метки, особенно несколько диметилированных остатков, связывались с худшим ответом. Для препаратов, нацеленных на метилирование ДНК, высокие уровни некоторых диметил‑меток снова указывали на устойчивость, тогда как ацетилированные метки на хвостах гистонов ассоциировались с лучшим ответом. Ингибиторы гистондеацетилаз показывали менее чёткое разделение между чувствительными и резистентными линиями, но некоторые закономерности все же выявлялись, включая специфические метки, обогащённые либо в наименее, либо в наиболее отзывчивых клетках. В целом эти наблюдения указывали, что совокупный ландшафт меток гистонов, а не одна отдельная метка, несёт информацию о реакции клеток лейкемии на эпигенетические препараты.
Проверка одной метки
Поскольку предыдущие данные предполагали, что акларубицин особенно эффективен в клетках с высоким уровнем H3K27me3, команда проверила эту идею напрямую. Они использовали другой препарат, блокирующий энзим, накладывающий эту метку, и успешно снизили уровень H3K27me3 в нескольких линиях Т‑клеточного лейкоза. Удивительно, но это не изменило чувствительность клеток к акларубицину. Также были наблюдаемы линии, которые естественно имели высокий H3K27me3, но при этом были резистентны. Это показало: даже если отдельная метка коррелирует с ответом в одних условиях, сама по себе она недостаточна для объяснения чувствительности.
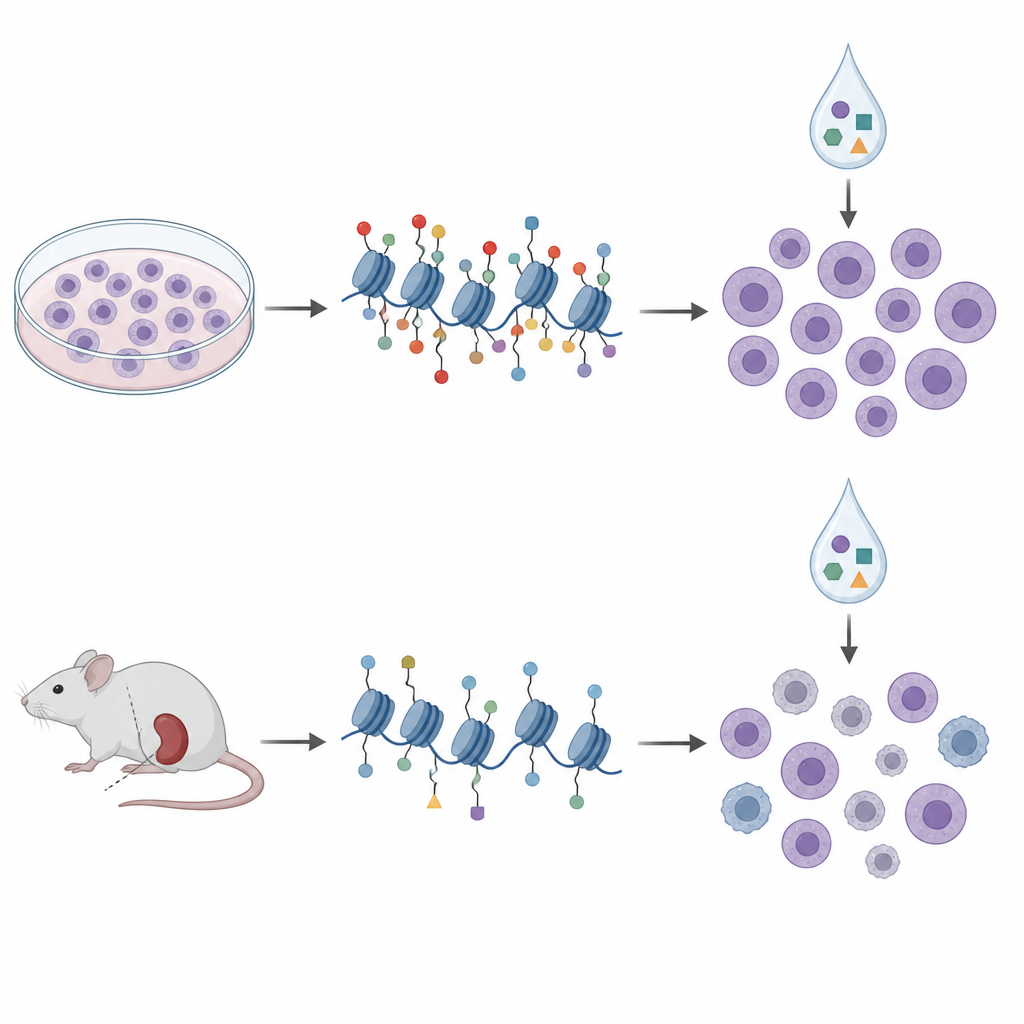
От чашек Петри к мышиным моделям
Чтобы приблизиться к клинике, исследователи обратились к ксенотрансплантатам, полученным от пациентов, где клетки лейкемии растут в иммунодефицитных мышах. Они профилировали метки гистонов и метилирование ДНК в клетках из десяти таких моделей и подвергли их воздействию аналогичного набора эпигенетических препаратов вне организма. В этих образцах паттерны гистонов сгруппировались в четыре кластера, которые в целом отражали известные генетические подтипы и более широкие состояния метилирования ДНК, что говорит о том, что профилирование гистонов улавливает значимую биологию болезни. Но при сравнении меток гистонов и чувствительности к препаратам сигнатуры из клеточных линий не переносились. Более того, некоторые связи меняли направление: та же метка H3K27me3, которая в культурах намекала на чувствительность к акларубицину, в клетках, полученных от мышей, связывалась с пониженной чувствительностью.
Сдвигающаяся сеть, а не фиксированный код
Чтобы понять это несоответствие, команда изучила, как различные метки гистонов повышаются и понижаются совместно в моделях. В пробах, полученных от пациентов, многие метки двигались в тесной координации, формируя плотную сеть положительных корреляций, тогда как в клеточных линиях эта сеть была более рыхлой и фрагментированной. Некоторые метки занимали узловые позиции в этих сетях в одной системе, но не в другой. Эти паттерны поддерживают идею о том, что метки гистонов действуют как часть контекстно‑зависимого языка, где значение любой отдельной метки зависит от соседей и от клеточной среды. Длительный рост в чашке Петри, по‑видимому, перенастраивает этот язык таким образом, что меняется связь между паттернами гистонов и ответом на препараты.
Что это значит для будущей помощи пациентам с лейкемией
Эта работа предлагает рамки для использования масс‑спектрометрии при чтении богатого ландшафта меток гистонов в Т‑клеточном лейкозе и для связывания их с реакцией клеток на эпигенетические препараты. Она также несёт предостережение: результаты, полученные на стандартных клеточных линиях, могут ненадёжно предсказывать ответы в более реалистичных моделях, полученных от пациентов, не говоря уже о людях. Чтобы маркеры на основе гистонов могли направлять персонализированное лечение, исследователям придётся учитывать эту сложность, сосредоточиться на комбинациях меток и тщательно выбирать модели болезни, максимально отражающие биологию пациентов.
Цитирование: Corveleyn, L., Provez, L., Satilmis, O. et al. Profiling histone post-translational modifications to identify signatures of epigenetic drug response in T-cell acute lymphoblastic leukemia. Sci Rep 16, 15029 (2026). https://doi.org/10.1038/s41598-026-44665-4
Ключевые слова: Т‑клеточный острый лимфобластный лейкоз, эпигенетические препараты, модификации гистонов, ксенотрансплантаты, полученные от пациента, биомаркеры ответа на препараты