Clear Sky Science · ja
T 細胞急性リンパ性白血病におけるエピジェネティック薬剤反応の署名を同定するためのヒストン翻訳後修飾のプロファイリング
このがん研究が重要な理由
T細胞急性リンパ性白血病の小児・成人治療は大きく進歩しましたが、多くの患者が再発したり、強力な化学療法による深刻な副作用を受けたりしています。どの患者にどの薬が有効かを予測する手段がより必要です。本研究は、白血病細胞のDNA包装タンパク質に付く小さな化学タグが、細胞のエピジェネティック機構に作用する現代の抗がん薬への応答を予測する手がかりになるかを検討します。
DNA包装に刻まれた隠れたコード
各白血病細胞内でDNAはヒストンと呼ばれるタンパク質の周りに巻かれ、クロマチンという凝縮構造を形成しています。ヒストンには多くの小さな化学タグが付着しており、これらはスイッチのように働いて遺伝子のオン/オフを制御し、基礎となるDNA配列を変えることなく発現を調節します。これらのタグは可逆的であるため、薬剤の標的として魅力的です。こうした「エピドラッグ」はすでに血液がんで使われていますが、T細胞白血病における役割はまだ明確でなく、誰が恩恵を受けるかを予測する単純な指標は不足しています。
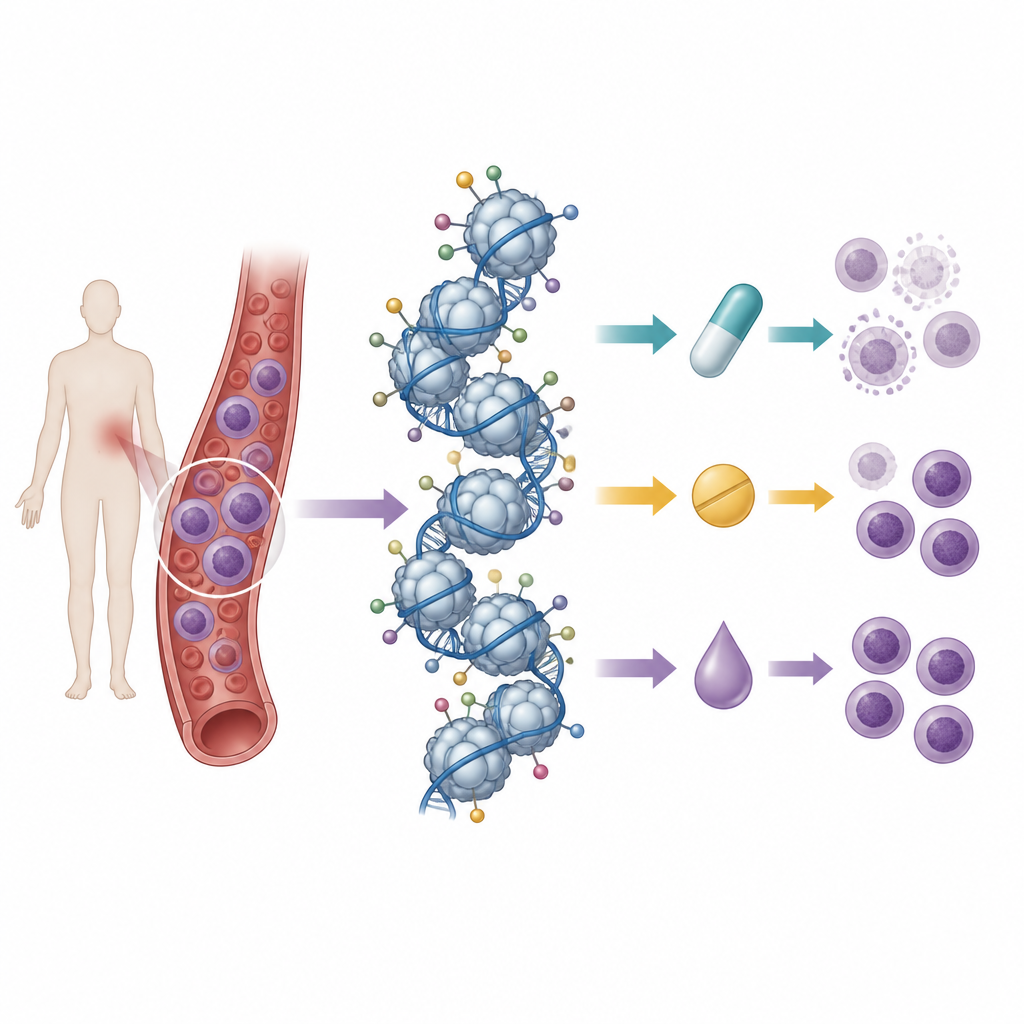
多くのヒストンマークを同時に読む
研究者らは、質量分析を用いて21のT細胞白血病細胞株のヒストンタグの基底パターンをマップした以前の取り組みを基盤にしました。質量分析は数百の化学的マークを同時に測定できます。続いてこれらの細胞株に対して9種類の薬剤を投与しました:標準的なアントラサイクリン系化学療法3剤、ヒストン脱アセチル化酵素を阻害する薬3剤、DNAメチル化酵素を阻害する薬3剤です。処置後の細胞生存と出発時のヒストンパターンを比較することで、各薬剤への感受性または耐性と連動する“署名”を探索しました。
細胞株が示したもの
培養細胞では、明確なヒストン署名が現れました。アントラサイクリン薬に対しては、H3K27me3と呼ばれる抑制的マークのような特定の抑制マークが感受性の高い株で高い傾向があり、他方でいくつかのジメチル基は反応不良と関連していました。DNAメチル化を標的とする薬では、いくつかのジメチルマークの高レベルが再び耐性を示し、ヒストン尾部のアセチルマークは良好な反応と結びついていました。ヒストン脱アセチラーゼ阻害薬では、感受性と耐性の分離は弱めでしたが、最も反応が良い/悪い細胞に富む特定のマークなど、いくつかのパターンは確認されました。全体として、どの単一マークでもなく、ヒストンタグの複合的なランドスケープがエピジェネティック薬剤への細胞応答に関する情報を保持していることが示唆されました。
単一マークを検証する
以前の研究でH3K27me3が豊富な細胞でアクラルビシンが特に有効であることが示唆されていたため、チームはこの仮説を直接検証しました。別の薬剤でこのマークを書き込む酵素を阻害し、いくつかのT細胞白血病株でH3K27me3を低下させることに成功しました。驚くべきことに、これでも細胞のアクラルビシン感受性は変わりませんでした。また、高H3K27me3でありながら耐性を示す細胞株も観察されました。これは、単一のヒストンタグがある状況で薬剤反応と相関していても、それだけで感受性を説明するには不十分であることを示しています。
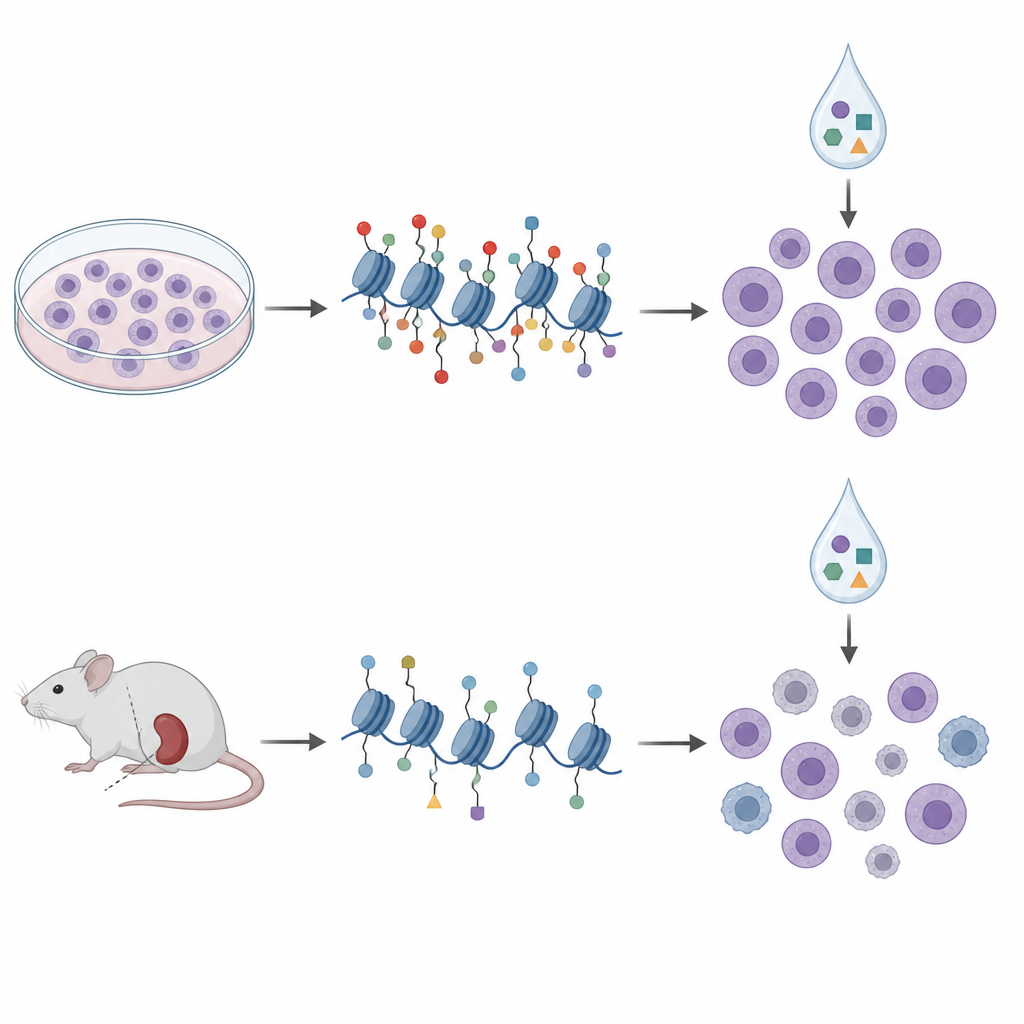
シャーレからマウスモデルへ
臨床に近づけるため、研究者らは患者由来異種移植(PDX)モデルに目を向けました。PDXでは患者の白血病細胞が免疫不全マウス内で増殖します。10のこうしたモデル由来の細胞でヒストンタグとDNAメチル化をプロファイルし、同様のエピジェネティック薬のパネルで体外処理を行いました。これらのサンプルではヒストンパターンが4つのクラスターに分類され、既知の遺伝学的サブタイプや広域のDNAメチル化状態を概ね反映しており、ヒストンプロファイリングが意味ある疾患生物学をとらえていることが示唆されました。しかし、ヒストンマークと薬剤感受性を再度比較すると、細胞株で得られた署名はそのまま当てはまりませんでした。実際にはいくつかの関係が逆転し、シャーレでアクラルビシン感受性を示唆した同じH3K27me3マークが、マウス由来細胞では低い感受性と結びつくこともありました。
固定化されたコードではなく変化するネットワーク
この不一致を理解するため、チームはモデル間で異なるヒストンマークがどのように連動して上昇・下降するかを調べました。患者由来サンプルでは多くのマークが密に協調して動き、正の相関の濃密なネットワークを形成していたのに対し、細胞株ではこのネットワークは緩く断片化していました。あるマークが一方のシステムでハブに位置しているが他方ではそうでない、というケースもありました。これらのパターンは、ヒストンタグが文脈依存の言語の一部として機能し、あるタグの意味は隣接するタグや細胞環境に依存するという考えを支持します。長期にわたるシャーレでの増殖は、この言語を書き換え、ヒストンパターンと薬剤反応の関係を変えてしまうようです。
将来の白血病治療への示唆
本研究は、質量分析を用いてT細胞白血病のヒストンマークの豊かなランドスケープを読み取り、エピジェネティック薬剤への細胞応答と結びつける枠組みを示しています。同時に注意すべき点も示しています:標準的な細胞株から得られた結果は、より現実的な患者由来モデル、ましてや人間における反応を確実に予測するとは限らないということです。ヒストンに基づくバイオマーカーを個別化治療に役立てるには、この複雑さを受け入れ、マークの組み合わせに注目し、患者の生物学をできるだけ反映する疾患モデルを慎重に選ぶ必要があります。
引用: Corveleyn, L., Provez, L., Satilmis, O. et al. Profiling histone post-translational modifications to identify signatures of epigenetic drug response in T-cell acute lymphoblastic leukemia. Sci Rep 16, 15029 (2026). https://doi.org/10.1038/s41598-026-44665-4
キーワード: T細胞急性リンパ性白血病, エピジェネティック薬剤, ヒストン修飾, 患者由来異種移植モデル, 薬剤反応バイオマーカー