Clear Sky Science · he
אפיון שינויים פוסט-טרנסלציונליים של היסטונים לזיהוי חתימות של תגובת-אפיגנטיקה בסרטן הלימפובלסטי חריף מסוג T
מדוע מחקר זה חשוב
הטיפול בילדים ובמבוגרים עם לוקמיה לימפובלסטית חריפה של תאי T השתפר משמעותית, אך מטופלים רבים עדיין חוזרים למחלה או סובלים מתופעות לוואי קשות של כימותרפיה מאסיבית. הרופאים זקוקים לדרכים טובות יותר לחזות איזו תרופה תפעל עבור איזה מטופל. מחקר זה בוחן האם טאגים כימיים זעירים על חלבוני חבישת ה-DNA בתאי הלוקמיה יכולים לעזור לחזות כיצד תאים אלה יגיבו לתרופות מודרניות הפועלות על המערכת האפיגנטית של התא.
הקוד הסמוי על חבישת ה-DNA
בתוך כל תא לוקמיה, ה-DNA מוקף חלבונים הנקראים היסטונים, ויוצר מבנה דחוס המוכר ככרומטין. להיסטונים יש טאגים כימיים רבים קטנים הפועלים כמפסקי הדלקה וכיבוי, ועוזרים להפעיל או לכבות גנים ללא שינוי ברצף ה-DNA עצמו. מאחר שהטאגים הללו הפיכים, הם מהווים מטרות אטרקטיביות לתרופות. מספר "אפי-תרופות" כאלה כבר נמצאות בשימוש בסרטנים של הדם, אך תפקידן בלוקמיה של תאי T עדיין לא ברור, והרופאים חסרים סימנים פשוטים לחיזוי מי יפיק תועלת מהן.
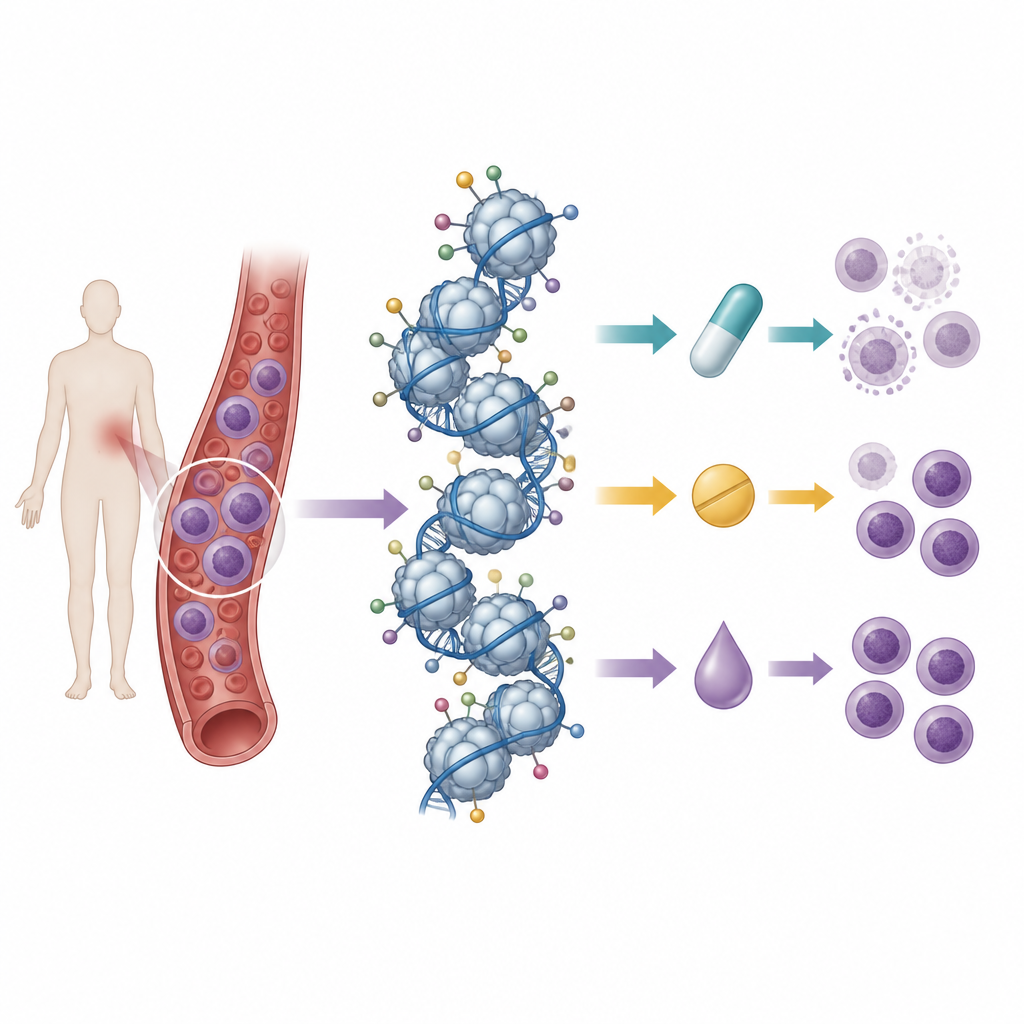
קריאת מספר סימני היסטון בו-זמנית
החוקרים בנו על מאמץ קודם בו מיפו את תבנית הבסיס של טאגי היסטונים ב-21 קווי תאי לוקמיה של תאי T באמצעות ספקטרומטריה מסה, טכניקה היכולה למדוד מאות סימנים כימיים בו-זמנית. הם טיפלו לאחר מכן בקווי תאים אלה בתשע תרופות: שלוש אנתרציקלינות כימותרפיות סטנדרטיות, שלוש תרופות החוסמות היסטון דה-אצטילאזות, ושלוש המעכבות אנזימי מתילציה של ה-DNA. על ידי השוואת הישרדות התאים לאחר הטיפול לדפוסי ההיסטונים ההתחלתיים, הם חיפשו "חתימות" של טאגים שנקשרו לרגישות או לעמידות כלפי כל תרופה.
מה גילו קווי התאים
בתאים מושרים, הופיעו חתימות היסטונים מובחנות. עבור תרופות אנתרציקלין, סימנים מדכאים מסוימים, כגון H3K27me3, נטו להיות גבוהים יותר בקווים הרגישים יותר, בעוד שסימנים אחרים, ובפרט כמה קבוצות דימתיל, נקשרו לתגובה גרועה יותר. עבור תרופות המכוונות למתילציה של ה-DNA, רמות גבוהות של כמה סימני דימתיל שוב הצביעו על עמידות, בעוד שסימני אצטיל על זנבות ההיסטון נקשרו לתגובה טובה יותר. מעכבי היסטון דה-אצטילאז הראו הפרדה חלשה יותר בין קווי תאים רגישים לעמידים, אך עדיין הופיעו דפוסים, כולל סימנים ספציפיים שעשירים בקווים הפחות או יותר רגישים. בסיכום, ממצאים אלה מצביעים על כך שהנוף המשולב של טאגי ההיסטון, ולא סימן יחיד, נושא מידע על אופן תגובת תאי הלוקמיה לאפי-תרופות.
מבחן של סימן יחיד
מכיוון שעבודה קודמת הציעה שאקלרוביצין פועל היטב במיוחד בתאים עשירים בסימן H3K27me3, הצוות בדק ישירות את הרעיון הזה. הם השתמשו בתרופה אחרת לחסימת האנזים שמטביע את הסימן הזה והצליחו להוריד את H3K27me3 בכמה קווי לוקמיה של תאי T. באופן מפתיע, זה לא שינה את רגישות התאים לאקלרוביצין. הם גם תועדו קווי תאים שהיו באופן טבעי עשירים ב-H3K27me3 אך עמידים. זאת הראתה שאף על פי שסימן היסטון יחיד יכול לעקוב אחרי תגובת-תרופה בהקשרים מסוימים, הוא אינו מספיק בפני עצמו להסביר את הרגישות.
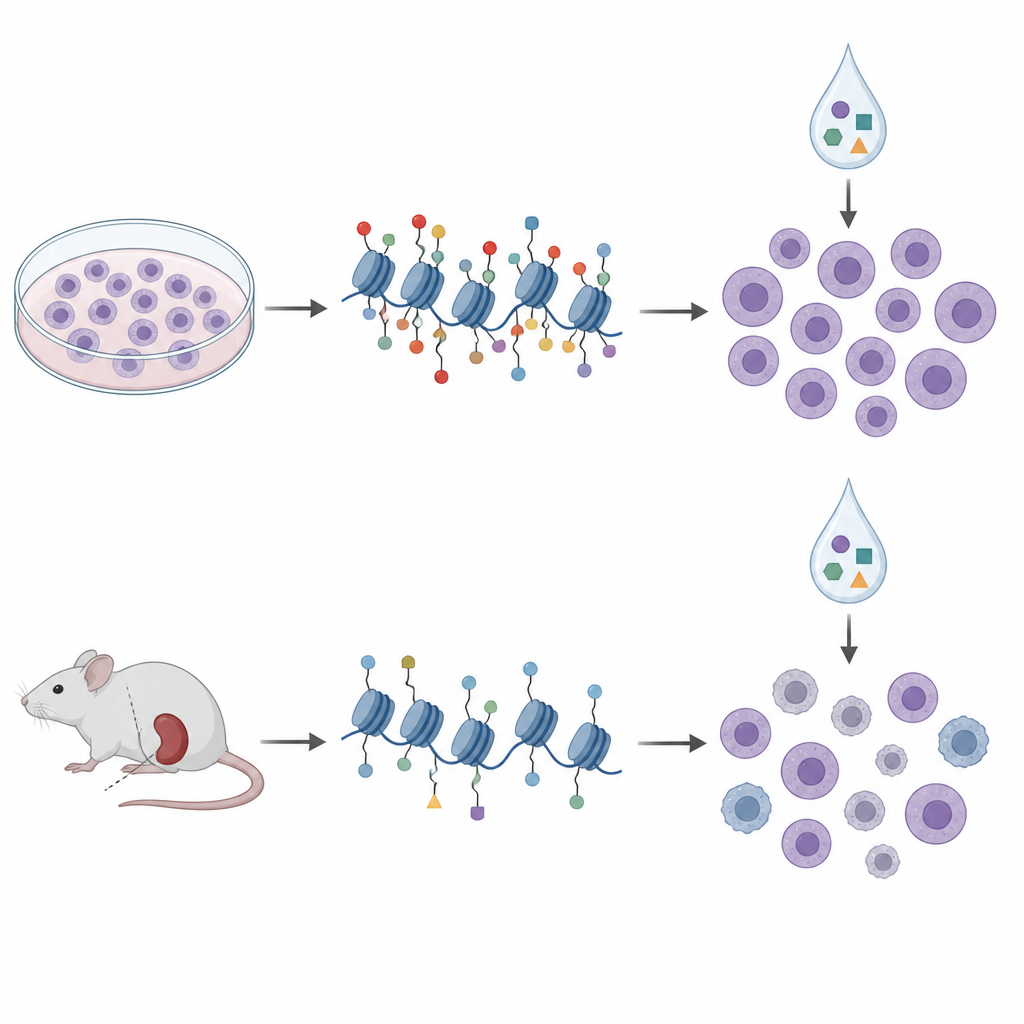
מצלחות למודלים בעכבר
כדי להתקרב יותר לשימוש קליני, החוקרים פנו לשחלופים ממקור מטופלים (patient-derived xenografts), שבהם תאי לוקמיה ממטופלים גדלים בעכברים חסרי מערכת חיסון. הם אפיינו טאגי היסטון ומתילציה של ה-DNA בתאים מעשרה מודלים כאלה וטיפלו בהם עם פנל דומה של תרופות אפיגנטיות מחוץ לגוף. בדגימות אלה, דפוסי ההיסטונים התמיינו לארבע אשכולות ששיקפו במידה רבה תת-סוגים גנטיים ידועים ומצבי מתילציה רחבים יותר של ה-DNA, מה שמרמז שמיפוי ההיסטונים לוכד ביולוגיה משמעותית של המחלה. אך כאשר השוו שוב סימני היסטון לרגישות לתרופות, החתימות מקווי התאים לא הורישו. למעשה, כמה יחסים אף התהפכו; אותו סימן H3K27me3 שרמז על רגישות לאקלרוביצין בתרביות נקשר לרגישות נמוכה יותר בתאים ממודלים ממקור מטופל.
רשת משתנה במקום קוד קבוע
כדי להבין את חוסר ההתאמה הזה, הצוות חקר כיצד סימני היסטון שונים עולים ונופלים יחד לאורך המודלים. בדגימות ממקור מטופל, סימנים רבים זזו בקורדינציה הדוקה, ויצרו רשת צפופה של מתאמים חיוביים, בעוד שבקווי תאים רשת זו הייתה רופפת וממוקדת פחות. סימנים מסוימים ישבו בצמתים של רשתות אלו במערכת אחת אך לא בשנייה. דפוסים אלה תומכים ברעיון שטאגי היסטון פועלים כחלק משפה תלויה בהקשר, שבה משמעותו של כל סימן תלויה בשכניו ובסביבת התא. גידול לטווח ארוך על צלחת נראה מחדש לכוונן שפה זו באופן שמשנה כיצד דפוסי ההיסטונים מתקשרים לתגובה לתרופות.
מה המשמעות לטיפול בלוקמיה בעתיד
עבודה זו מתווה מסגרת לשימוש בספקטרומטריה מסה כדי לקרוא את הנוף העשיר של סימני ההיסטון בלוקמיה של תאי T ולחברם לאופן שבו תאים מתמודדים עם תרופות אפיגנטיות. היא גם מעבירה אזהרה: תוצאות מקווי תאים סטנדרטיים עשויות שלא לחזות באופן אמין תגובות במודלים ריאליסטיים יותר ממקור מטופל, שלא לדבר על מטופלים עצמם. כדי שסמנים מבוססי היסטונים ידריכו טיפולים מותאמים אישית, החוקרים יצטרכו לקבל את המורכבות הזו, להתמקד בצירופים של סימנים, ולבחור בקפידה מודלים של מחלה שמשקפים את ביולוגיית המטופלים ככל האפשר.»
ציטוט: Corveleyn, L., Provez, L., Satilmis, O. et al. Profiling histone post-translational modifications to identify signatures of epigenetic drug response in T-cell acute lymphoblastic leukemia. Sci Rep 16, 15029 (2026). https://doi.org/10.1038/s41598-026-44665-4
מילות מפתח: לוקמיה לימפובלסטית חריפה של תאי T, תרופות אפיגנטיות, שינויים בהיסטונים, שחלופים ממקור מטופל (PDX), ביומרקרים לתגובה לתרופות