Clear Sky Science · nl
Profilering van post-translationele histonmodificaties om signaturen van epigenetische medicijnrespons bij T-cel acute lymfatische leukemie te identificeren
Waarom deze kankerstudie ertoe doet
De behandeling van kinderen en volwassenen met T-cel acute lymfatische leukemie is sterk verbeterd, maar veel patiënten krijgen nog steeds een terugval of ondervinden ernstige bijwerkingen van intensieve chemotherapie. Artsen hebben betere manieren nodig om te voorspellen welke medicijnen voor welke patiënt zullen werken. Deze studie onderzoekt of kleine chemische labels op eiwitten die DNA verpakken in leukemiecellen kunnen helpen voorspellen hoe die cellen reageren op moderne kankertherapieën die inwerken op de epigenetische machinerie van de cel.
De verborgen code op DNA-opslagmateriaal
In elke leukemiecellen is DNA gewikkeld rond eiwitten die histonen worden genoemd, waardoor een compacte structuur ontstaat die chromatine heet. Histonen dragen veel kleine chemische labels die als schakelaars fungeren en helpen genen aan of uit te zetten zonder de onderliggende DNA-sequentie te veranderen. Omdat deze labels omkeerbaar zijn, vormen ze aantrekkelijke doelwitten voor geneesmiddelen. Verschillende van dergelijke “epidrugs” worden al gebruikt bij bloedkankers, maar hun rol bij T-cel leukemie is nog onduidelijk en artsen missen eenvoudige markers om te voorspellen wie baat bij deze middelen heeft.
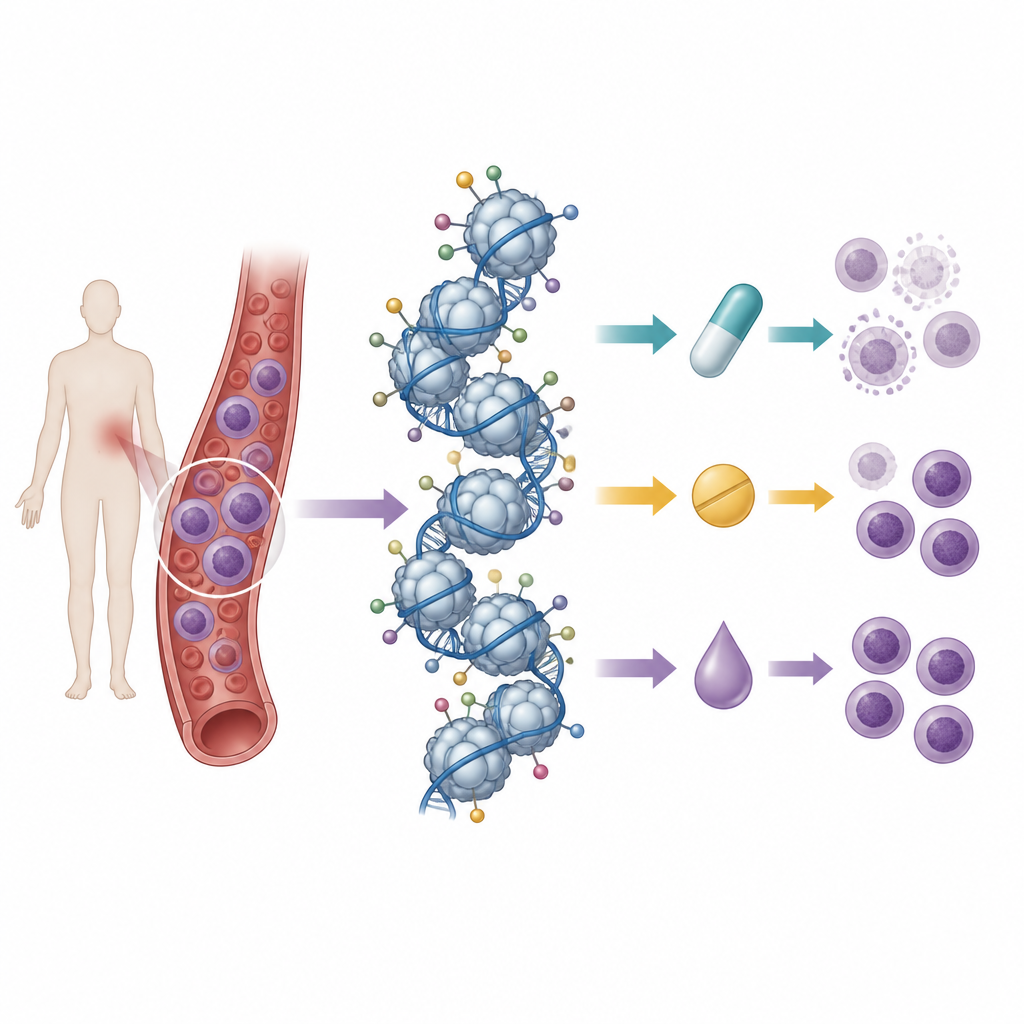
Veel histonmerken tegelijk aflezen
De onderzoekers bouwden voort op eerder werk waarin ze het basale patroon van histonlabels in 21 T-cel leukemiecellen hadden in kaart gebracht met massaspectrometrie, een techniek die honderden chemische markeringen tegelijk kan meten. Ze behandelden deze cellijnen vervolgens met negen geneesmiddelen: drie standaard chemotherapiën uit de anthracyclineklasse, drie middelen die histondeacetylases blokkeren, en drie die enzymen voor DNA-methylering remmen. Door de overleving van cellen na behandeling te vergelijken met de aanvankelijke histonpatronen, zochten ze naar “signaturen” van labels die samenhingen met gevoeligheid of resistentie voor elk middel.
Wat de celkweken onthulden
In gekweekte cellen kwamen er duidelijke histonsignaturen naar voren. Voor anthracyclines waren bepaalde repressieve markeringen, zoals H3K27me3, vaak hoger in gevoeliger cellijnen, terwijl andere markeringen, met name verschillende dimethylgroepen, geassocieerd waren met slechtere respons. Voor geneesmiddelen die DNA-methylering targeten, wezen hoge niveaus van sommige dimethylmarkeringen opnieuw op resistentie, terwijl acetylmarkeringen op histontails gelinkt waren aan betere respons. Histondeacetylaseremmers lieten een zwakkere scheiding zien tussen gevoelige en resistente cellijnen, maar sommige patronen waren nog steeds zichtbaar, inclusief specifieke markeringen die verrijkt waren in de minst of meest responsieve cellen. Over het geheel genomen suggereerden deze bevindingen dat het gecombineerde landschap van histonlabels, in plaats van één enkele markering, informatie bevat over hoe leukemiecellen reageren op epigenetische geneesmiddelen.
Een enkele markering op de proef stellen
Aangezien eerder werk suggereerde dat aclarubicine bijzonder goed werkt in cellen rijk aan de H3K27me3-markering, testte het team deze hypothese direct. Ze gebruikten een ander middel om het enzym dat deze markering aanbrengt te blokkeren en wisten H3K27me3 in meerdere T-cel leukemielijnen met succes te verlagen. Verrassend genoeg veranderde dit de gevoeligheid voor aclarubicine niet. Ze observeerden ook cellijnen die van nature hoge H3K27me3-niveaus hadden maar toch resistent waren. Dit toonde aan dat zelfs wanneer een enkele histonmarkering in sommige omstandigheden samenhangt met medicijnrespons, die markering op zichzelf niet voldoende is om gevoeligheid te verklaren.
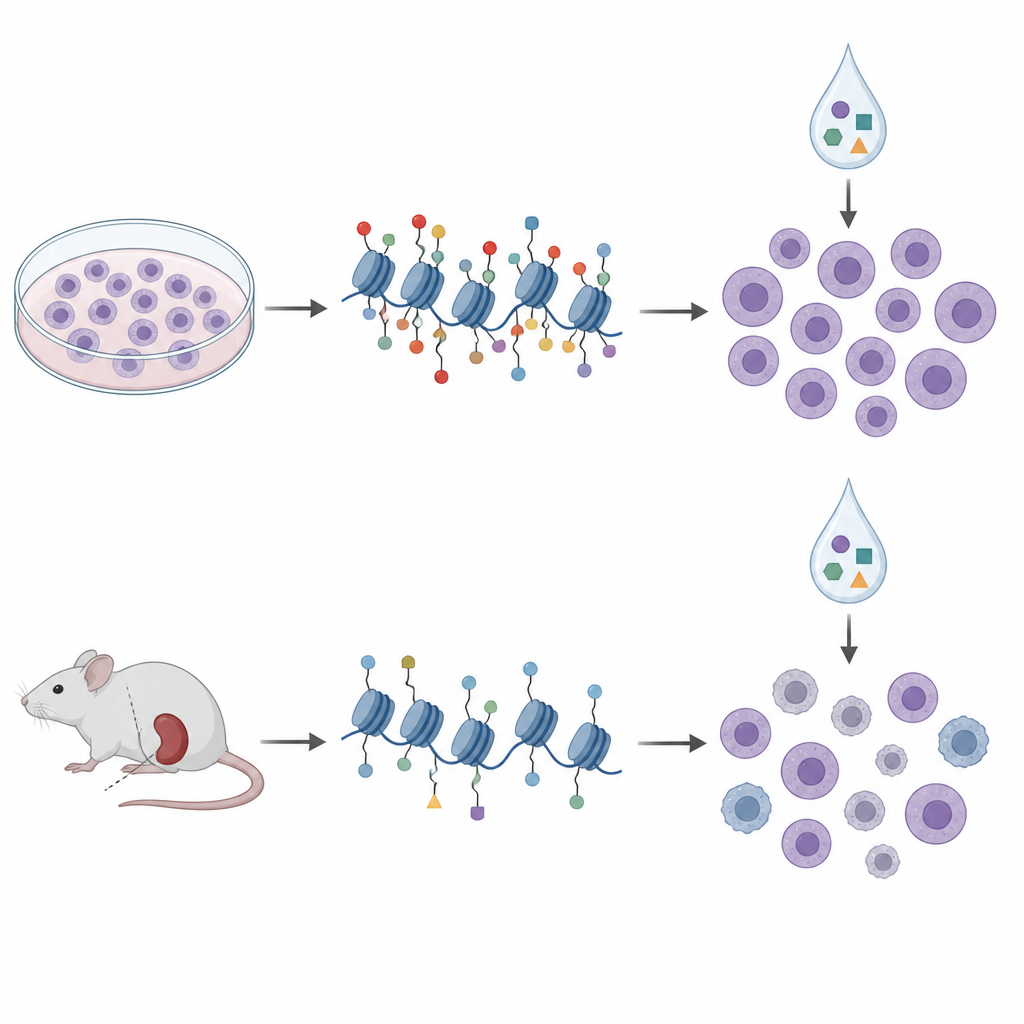
Van kweekschaaltjes naar muismodellen
Om dichter bij de kliniek te komen, schakelden de onderzoekers over op patiënt-afgeleide xenografts, waarbij leukemiecellen van patiënten groeien in immuundeficiënte muizen. Ze profielden histonlabels en DNA-methylering in cellen uit tien van dergelijke modellen en behandelden ze met een vergelijkbaar panel van epigenetische geneesmiddelen buiten het lichaam. In deze monsters groepeerden de histonpatronen in vier clusters die grotendeels overeenkwamen met bekende genetische subtypen en bredere DNA-methyleringsstaten, wat suggereert dat histonprofilering betekenisvolle ziektegerelateerde biologie vastlegt. Maar toen ze opnieuw histonmerken vergeleken met medicijngevoeligheid, droegen de signaturen uit celkweken niet over. Sterker nog, sommige relaties keerden om; hetzelfde H3K27me3-merkteken dat in kweken een aanwijzing gaf voor aclarubicinegevoeligheid, werd in de muismodellen geassocieerd met lagere gevoeligheid.
Een verschuivend netwerk in plaats van een vaste code
Om deze mismatch te begrijpen, bestudeerde het team hoe verschillende histonmarkeringen samen verhogen en verlagen over de modellen heen. In patiënt-afgeleide monsters bewogen veel markeringen in strakke coördinatie en vormden ze een dicht netwerk van positieve correlaties, terwijl dit netwerk in celkweken losser en meer gefragmenteerd was. Bepaalde markeringen zaten in de ene systeemvariant op knooppunten van deze netwerken, maar niet in de andere. Deze patronen ondersteunen het idee dat histonlabels functioneren als onderdeel van een contextafhankelijke taal, waarin de betekenis van één label afhangt van zijn buurmerken en de cellulaire omgeving. Langdurige groei in een kweek lijkt deze taal op manieren te herschikken die veranderen hoe histonpatronen samenhangen met medicijnrespons.
Wat dit betekent voor toekomstige leukemiezorg
Dit werk schetst een kader voor het gebruik van massaspectrometrie om het rijke landschap van histonmarkeringen in T-cel leukemie af te lezen en deze te koppelen aan hoe cellen omgaan met epigenetische geneesmiddelen. Het geeft ook een waarschuwende boodschap: resultaten uit standaard celkweken voorspellen mogelijk niet betrouwbaar de respons in realistischer patiënt-afgeleide modellen, en al helemaal niet bij mensen zelf. Voor histon-gebaseerde biomarkers die gepersonaliseerde behandelingen moeten sturen, zullen onderzoekers deze complexiteit moeten omarmen, zich richten op combinaties van markeringen en zorgvuldig ziektemodellen moeten kiezen die de biologie van patiënten zo getrouw mogelijk weergeven.
Bronvermelding: Corveleyn, L., Provez, L., Satilmis, O. et al. Profiling histone post-translational modifications to identify signatures of epigenetic drug response in T-cell acute lymphoblastic leukemia. Sci Rep 16, 15029 (2026). https://doi.org/10.1038/s41598-026-44665-4
Trefwoorden: T-cel acute lymfatische leukemie, epigenetische geneesmiddelen, histonmodificaties, patiënt-afgeleide xenografts, biomarkers voor medicijnrespons