Clear Sky Science · de
Profiling von posttranslationalen Histonmodifikationen zur Identifizierung von Signaturen epigenetischer Arzneimittelantworten bei T‑Zell‑akuter lymphatischer Leukämie
Warum diese Krebsstudie wichtig ist
Die Behandlung von Kindern und Erwachsenen mit T‑Zell‑akuter lymphatischer Leukämie hat sich stark verbessert, dennoch erleiden viele Patientinnen und Patienten Rückfälle oder schwere Nebenwirkungen durch intensive Chemotherapie. Ärztinnen und Ärzte benötigen bessere Methoden, um vorherzusagen, welches Medikament für welchen Patienten wirkt. Diese Studie untersucht, ob winzige chemische Markierungen auf Proteinen, die die DNA verpacken, dabei helfen können, vorherzusagen, wie Zellen auf moderne Krebsmedikamente reagieren, die an der epigenetischen Maschinerie der Zelle ansetzen.
Der verborgene Code auf der DNA‑Verpackung
In jeder Leukämiezelle ist die DNA um Proteine gewickelt, die Histone genannt werden, wodurch eine kompakte Struktur entsteht, das Chromatin. Histone tragen viele kleine chemische Markierungen, die wie Schalter wirken und helfen, Gene an‑ oder auszuschalten, ohne die zugrundeliegende DNA‑Sequenz zu verändern. Da diese Markierungen reversibel sind, stellen sie attraktive Ziele für Medikamente dar. Mehrere solcher „Epidrugs“ werden bereits bei Blutkrebserkrankungen eingesetzt, doch ihre Rolle bei T‑Zell‑Leukämie ist noch unklar, und es fehlen einfache Marker, um vorherzusagen, wer davon profitiert.
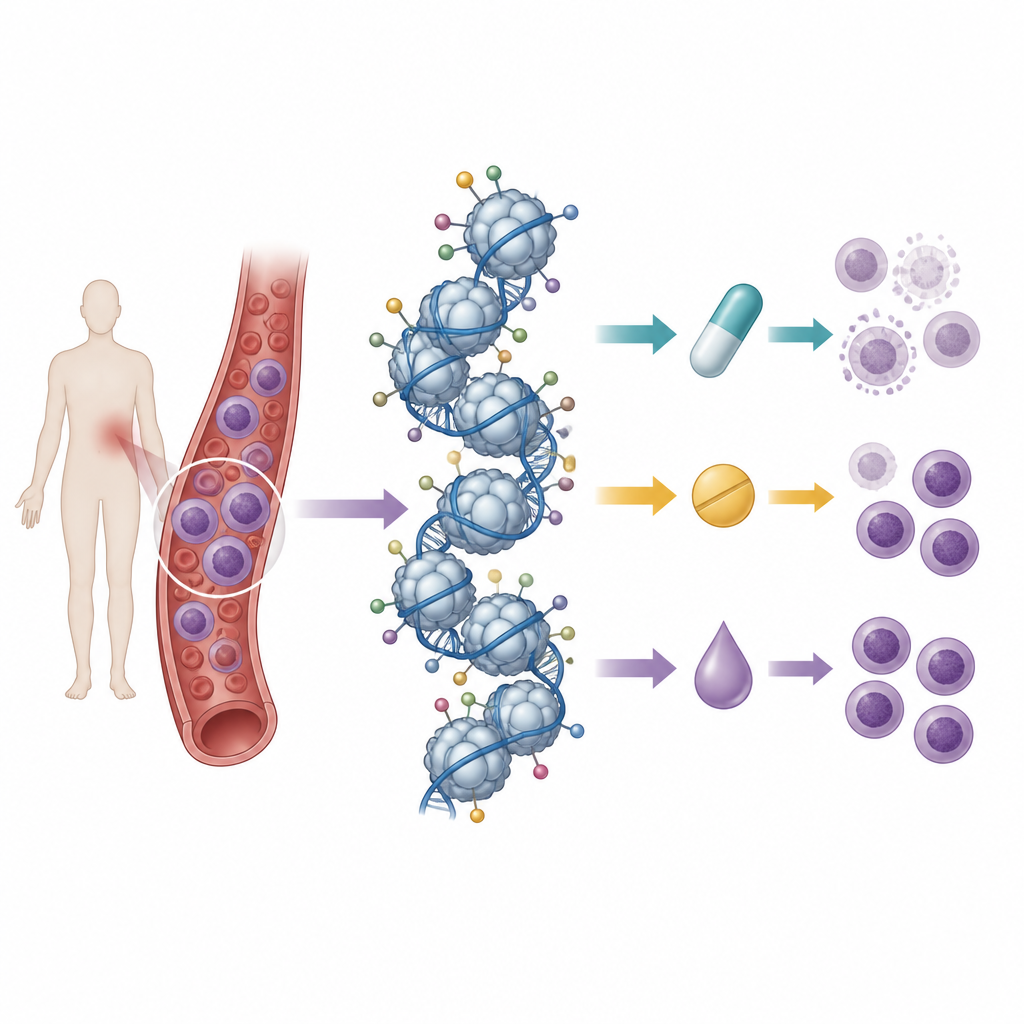
Viele Histonmarken gleichzeitig lesen
Die Forschenden bauten auf einer früheren Arbeit auf, in der sie das Ausgangsmuster von Histonmarkierungen in 21 T‑Zell‑Leukämie‑Zelllinien mittels Massenspektrometrie kartiert hatten, einer Technik, die Hunderte chemischer Markierungen gleichzeitig messen kann. Anschließend behandelten sie diese Zelllinien mit neun Wirkstoffen: drei Standard‑Chemotherapie‑Anthrazyklinen, drei Hemmstoffen der Histondeacetylasen und drei Hemmstoffen der DNA‑Methylierungsenzyme. Durch den Vergleich des Zellüberlebens nach der Behandlung mit den anfänglichen Histonmustern suchten sie nach „Signaturen“ von Markierungen, die mit Sensitivität oder Resistenz gegenüber jedem Wirkstoff korrelierten.
Was die Zelllinien zeigten
In kultivierten Zellen traten tatsächlich unterscheidbare Histonsignaturen zutage. Für Anthrazykline zeigten sich bestimmte repressive Markierungen, etwa eine mit der Bezeichnung H3K27me3, tendenziell erhöht in empfindlicheren Linien, während andere Markierungen, insbesondere mehrere Dimethylgruppen, mit schlechterer Reaktion verknüpft waren. Bei Wirkstoffen, die die DNA‑Methylierung ansprechen, deuteten hohe Niveaus einiger Dimethylmarken erneut auf Resistenz hin, während Acetylmarken an Histonschwänzen mit besserer Ansprechrate assoziiert waren. Inhibitoren der Histondeacetylasen zeigten eine schwächere Trennung zwischen sensitiven und resistenten Zelllinien, doch traten dennoch einige Muster auf, einschließlich spezifischer Markierungen, die in den am wenigsten bzw. am meisten ansprechenden Zellen angereichert waren. Insgesamt deuten diese Befunde darauf hin, dass die kombinierte Landschaft von Histonmarken — und nicht einzelne Markierungen allein — Informationen darüber trägt, wie Leukämiezellen auf epigenetische Wirkstoffe reagieren.
Eine einzelne Marke auf die Probe stellen
Da frühere Arbeiten nahegelegt hatten, dass Aclarubicin besonders gut in Zellen wirkt, die reich an der H3K27me3‑Marke sind, prüfte das Team diese Idee direkt. Sie verwendeten ein anderes Medikament, um das Enzym zu blockieren, das diese Marke setzt, und konnten H3K27me3 in mehreren T‑Zell‑Leukämie‑Linien erfolgreich reduzieren. Überraschenderweise veränderte das die Empfindlichkeit der Zellen gegenüber Aclarubicin nicht. Sie beobachteten außerdem Zelllinien, die natürlicherweise hohe H3K27me3‑Werte hatten, aber resistent waren. Das zeigte, dass selbst wenn eine einzelne Histonmarke in bestimmten Kontexten mit der Arzneimittelantwort korreliert, sie allein nicht ausreicht, um Sensitivität zu erklären.
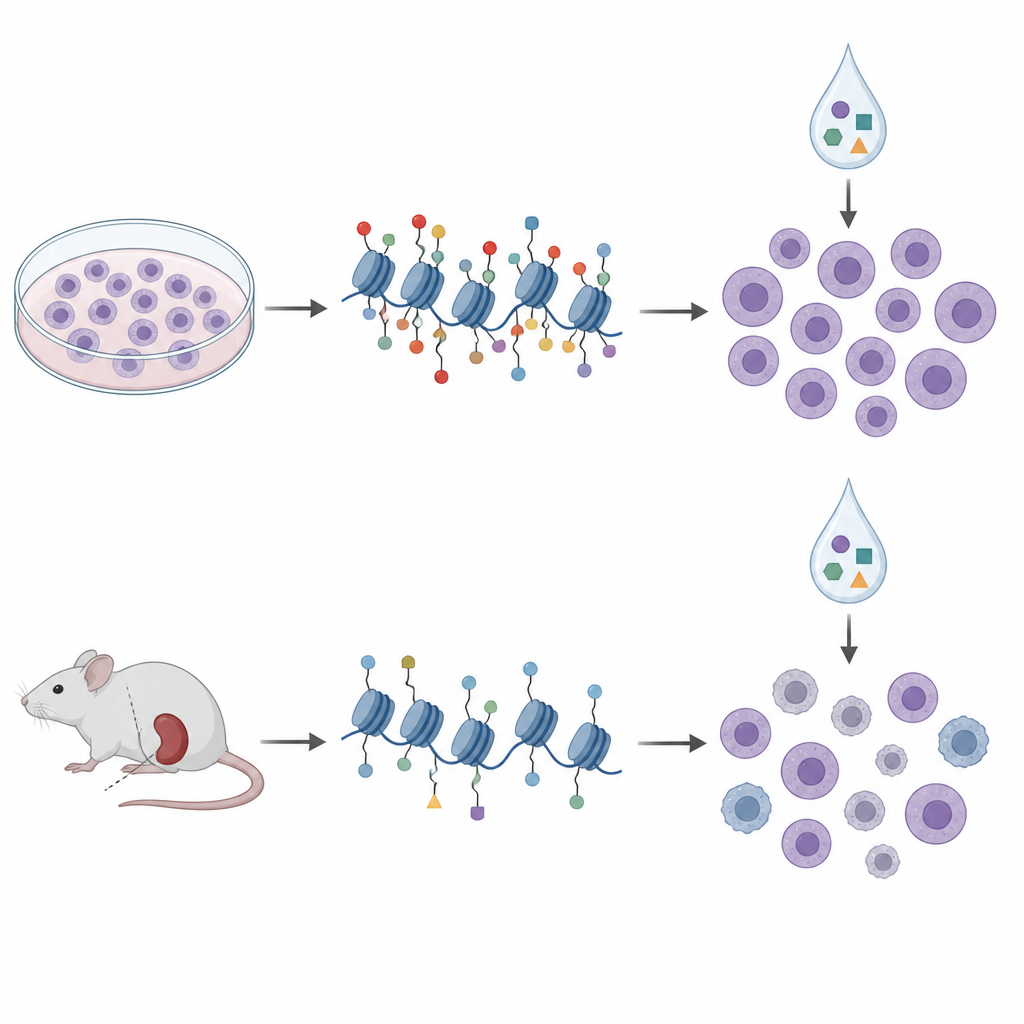
Von Schalen zur Maus
Um der klinischen Realität näherzukommen, griffen die Forschenden auf patientenabgeleitete Xenografts zurück, in denen Leukämiezellen von Patientinnen und Patienten in immundefizienten Mäusen wachsen. Sie analysierten Histonmarken und DNA‑Methylierung in Zellen aus zehn solchen Modellen und behandelten sie ex vivo mit einem ähnlichen Panel epigenetischer Wirkstoffe. In diesen Proben gruppierten sich Histonmuster in vier Cluster, die weitgehend bekannte genetische Subtypen und breitere DNA‑Methylierungszustände widerspiegelten, was darauf hindeutet, dass Histonprofilierung relevante Krankheitsbiologie erfasst. Als sie jedoch erneut Histonmarken mit Arzneimittelempfindlichkeit verglichen, ließen sich die Signaturen aus den Zelllinien nicht übertragen. Tatsächlich kehrten sich einige Beziehungen um; dieselbe H3K27me3‑Marke, die in Kultur auf Aclarubicin‑Sensitivität hindeutete, war in den maus‑abgeleiteten Zellen mit geringerer Sensitivität verbunden.
Ein sich wandelndes Netzwerk statt eines festen Codes
Um diese Diskrepanz zu verstehen, untersuchte das Team, wie verschiedene Histonmarken in den Modellen gemeinsam an‑ und abnehmen. In patientenabgeleiteten Proben bewegten sich viele Markierungen eng koordiniert und bildeten ein dichtes Netzwerk positiver Korrelationen, während dieses Netzwerk in Zelllinien lockerer und fragmentierter war. Bestimmte Markierungen standen in einem System im Zentrum des Netzwerks, im anderen jedoch nicht. Diese Muster stützen die Idee, dass Histonmarken als Teil einer kontextabhängigen Sprache wirken, in der die Bedeutung einer einzelnen Marke von ihren Nachbarn und der zellulären Umgebung abhängt. Langfristiges Wachstum in der Kultur scheint diese Sprache so umzuschreiben, dass sich die Beziehung zwischen Histonmustern und Arzneimittelantwort verändert.
Was das für die künftige Leukämieversorgung bedeutet
Diese Arbeit skizziert ein Rahmenkonzept zur Nutzung von Massenspektrometrie, um die reichhaltige Landschaft der Histonmarken bei T‑Zell‑Leukämie zu erfassen und sie mit dem Umgang der Zellen mit epigenetischen Wirkstoffen zu verknüpfen. Sie liefert zugleich eine mahnende Botschaft: Ergebnisse aus Standard‑Zelllinien sagen möglicherweise nicht zuverlässig das Ansprechen in realistischeren patientenabgeleiteten Modellen voraus, geschweige denn beim Menschen. Damit histonbasierte Biomarker personalisierte Behandlungen leiten können, müssen Forschende diese Komplexität annehmen, den Fokus auf Kombinationen von Marken legen und Krankheitsmodelle sorgfältig auswählen, die die Biologie von Patientinnen und Patienten so genau wie möglich widerspiegeln.
Zitation: Corveleyn, L., Provez, L., Satilmis, O. et al. Profiling histone post-translational modifications to identify signatures of epigenetic drug response in T-cell acute lymphoblastic leukemia. Sci Rep 16, 15029 (2026). https://doi.org/10.1038/s41598-026-44665-4
Schlüsselwörter: T‑Zell‑akute lymphatische Leukämie, epigenetische Wirkstoffe, Histonmodifikationen, patientenabgeleitete Xenografts, Biomarker der Arzneimittelantwort