Clear Sky Science · ar
توصيف التعديلات بعد الترجمة على الهيستونات لتحديد بصمات استجابة الأدوية فوق الجينية في اللوكيميا اللمفاوية الحادة للخلايا التائية
لماذا تهم هذه الدراسة السرطانية
تحسّن علاج الأطفال والبالغين المصابين باللوكيميا اللمفاوية الحادة للخلايا التائية بشكل كبير، ومع ذلك يظل العديد من المرضى يعانون من انتكاسات أو آثار جانبية خطيرة نتيجة العلاج الكيميائي المكثف. يحتاج الأطباء إلى طرق أفضل للتنبؤ بأي الأدوية ستنجح مع أي مريض. تستقصي هذه الدراسة ما إذا كانت العلامات الكيميائية الدقيقة على بروتينات تغليف الحمض النووي في خلايا اللوكيميا يمكن أن تساعد في التنبؤ بكيفية استجابة تلك الخلايا لأدوية السرطان الحديثة التي تستهدف آليات فوق جينية في الخلية.
الرمز الخفي على تغليف الحمض النووي
داخل كل خلية لوكيميا، يلتف الحمض النووي حول بروتينات تسمى الهيستونات، مكوِّناً بنية مدمجة تُعرف بالكروماتين. تحمل الهيستونات العديد من العلامات الكيميائية الصغيرة التي تعمل كمفاتيح، تساعد على تشغيل أو إيقاف الجينات دون تغيير تسلسل الحمض النووي الأساسي. وبما أن هذه العلامات قابلة للعكس، فهي أهداف جذابة للأدوية. عدد من هذه «الأدوية الفوق جينية» مستخدمة بالفعل في أمراض الدم، لكن دورها في اللوكيميا التائية لا يزال غير واضح، ويفتقر الأطباء إلى علامات بسيطة يمكنها التنبؤ بمن سيستفيد منها.
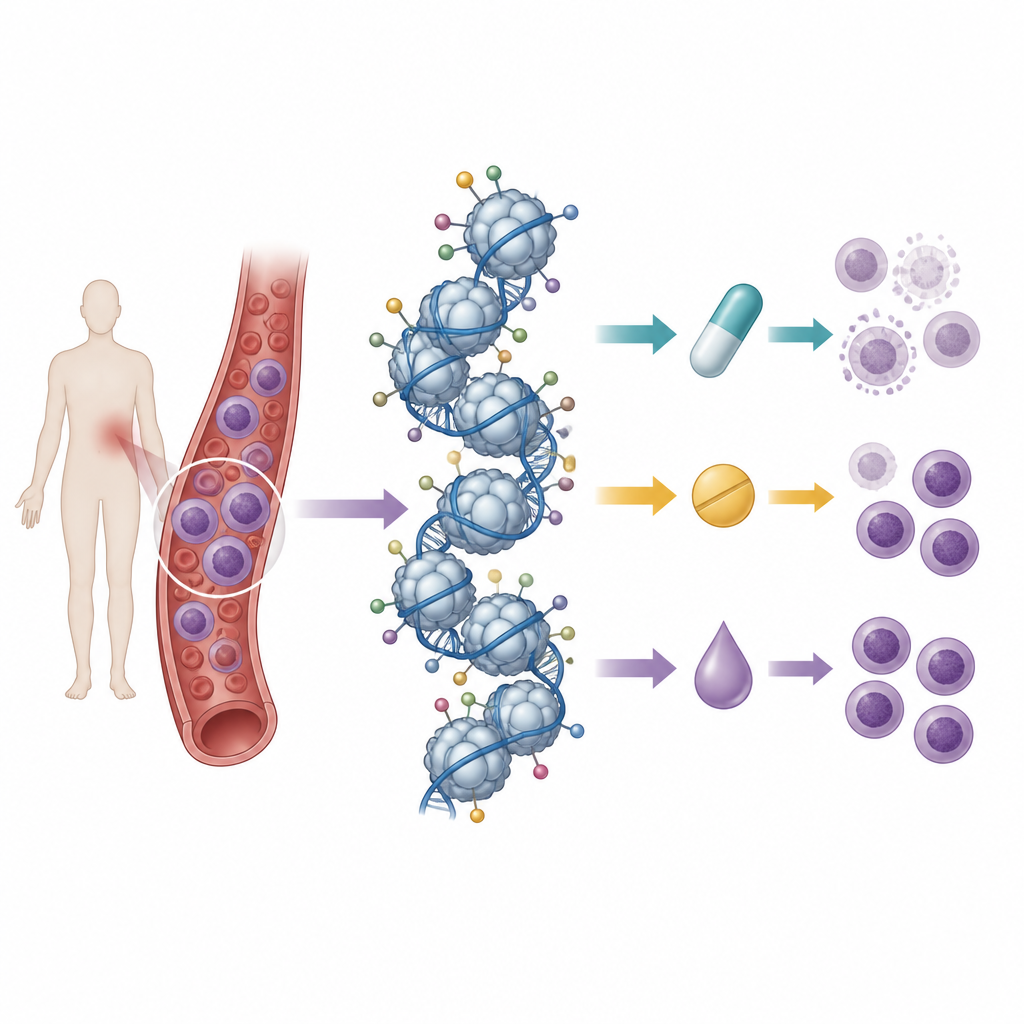
قراءة العديد من علامات الهيستون دفعة واحدة
بنى الباحثون على جهد سابق قاموا فيه برسم نمط أساسي لعلامات الهيستون في 21 خط خلية لسرطان الخلايا التائية باستخدام مطيافية الكتلة، وهي تقنية تستطيع قياس المئات من العلامات الكيميائية دفعة واحدة. ثم عالَجوا خطوط الخلايا هذه بتسعة أدوية: ثلاثة أنثراسيكلينات من العلاج الكيميائي التقليدي، وثلاثة أدوية تحجب ناقلات أسيتيل الهيستون (هيدروجينازات الأسيتيل)، وثلاثة مثبطات لإنزيمات مثيلة الحمض النووي. بمقارنة بقاء الخلايا بعد العلاج مع أنماط الهيستون الابتدائية، بحثوا عن «بصمات» من العلامات التي تترافق مع الحساسية أو المقاومة لكل دواء.
ما كشفته خطوط الخلايا
في الخلايا المستزرعة، برزت بصمات هيستون مميزة. بالنسبة لأدوية الأنثراسيكلين، كانت بعض العلامات الكابحة، مثل تلك المسماة H3K27me3، تميل إلى أن تكون أعلى في الخطوط الأكثر حساسية، بينما كانت علامات أخرى، خاصة عدة مجموعات ثنائية الميثلة، مرتبطة باستجابة أضعف. بالنسبة للأدوية التي تستهدف مثيلة الحمض النووي، أشارت المستويات العالية لبعض علامات ثنائية الميثلة مرة أخرى إلى المقاومة، في حين ارتبطت علامات الأسيتيل على ذيول الهيستون باستجابة أفضل. أظهرت مثبطات ناقلات الأسيتيل للهيستون فصلًا أضعف بين الخطوط الحساسة والمقاومة، لكن بعض الأنماط ظلت واضحة، بما في ذلك علامات محددة مُثرية إما في الخلايا الأقل أو الأكثر استجابة. بشكل عام، اقترحت هذه النتائج أن المشهد المشترك لعلامات الهيستون، بدلاً من أي علامة فردية، يحمل معلومات حول كيفية استجابة خلايا اللوكيميا للأدوية فوق الجينية.
اختبار علامة واحدة مباشرة
بما أن أعمالًا سابقة أشارت إلى أن الأكلاروبسين يعمل جيدًا خصوصًا في الخلايا الغنية بعلامة H3K27me3، اختبر الفريق هذه الفكرة مباشرة. استخدموا دواءً آخر لحجب الإنزيم الذي يضيف هذه العلامة ونجحوا في خفض H3K27me3 في عدة خطوط خلايا للوكيميا الخلايا التائية. ولدهشتهم، لم يغير ذلك من حساسية الخلايا للأكلاروبسين. كما لاحظوا خطوط خلايا كانت طبيعيًا تحتوي مستويات عالية من H3K27me3 لكنها كانت مقاومة. أظهر ذلك أنه حتى عندما تترافق علامة هيستون واحدة مع استجابة الدواء في بعض السياقات، فهي ليست كافية بمفردها لشرح الحساسية.
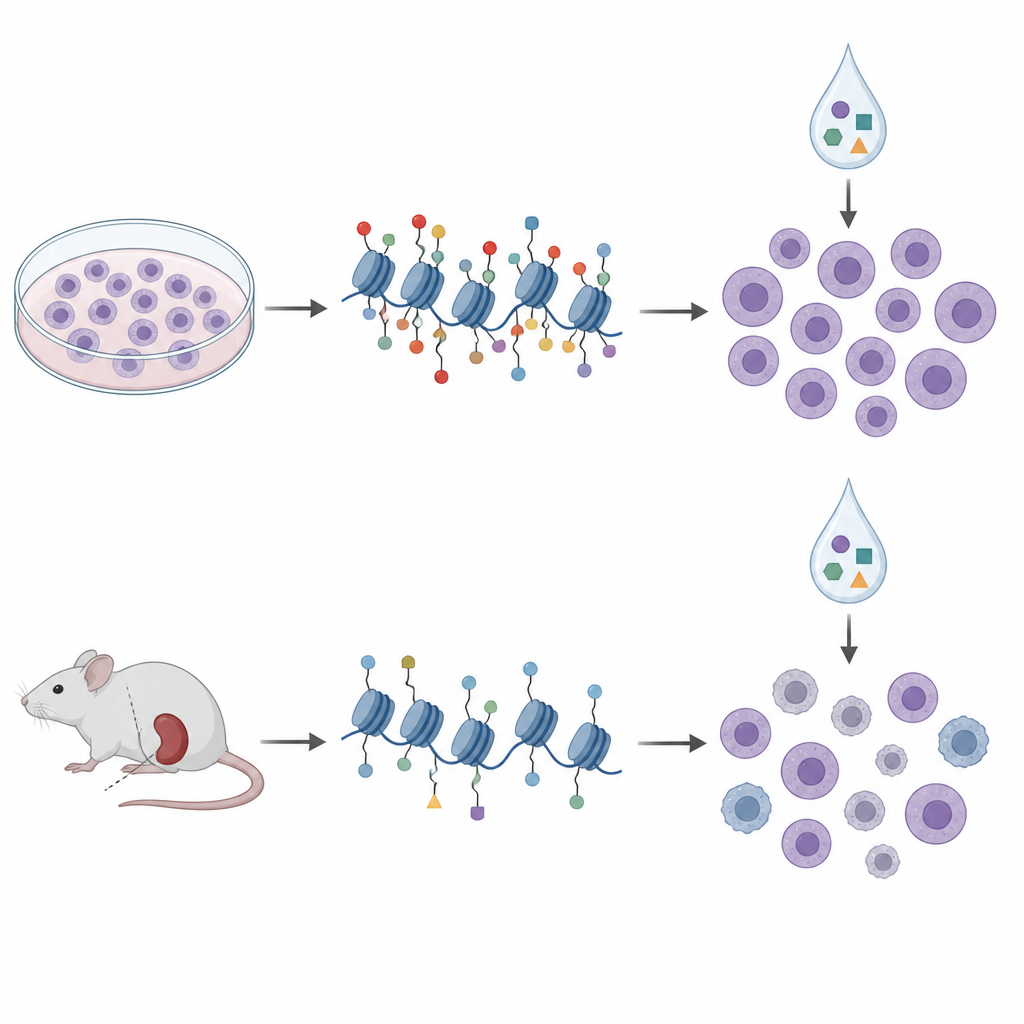
من أطباق الزرع إلى نماذج الفأر
للانتقال أقرب إلى العيادة، اتجه الباحثون إلى نماذج مستزرَعَة من المرضى، حيث تنمو خلايا اللوكيميا المأخوذة من مرضى داخل فئران ناقصة المناعة. قاموا بعمل بروفايل لعلامات الهيستون ومثيلة الحمض النووي في خلايا من عشرة نماذج من هذا النوع وعالجوها بمجموعة مماثلة من الأدوية الفوق جينية خارج الجسم. في هذه العينات، تجمعت أنماط الهيستون في أربع مجموعات انعكست إلى حد كبير مع الأنواع الجينية المعروفة وحالات مثيلة الحمض النووي الأوسع، مما يشير إلى أن بروفايل الهيستون يلتقط بيولوجيا مرض ذات معنى. لكن عندما قارنوا مرة أخرى علامات الهيستون بحساسية الدواء، لم تنتقل البصمات المستقاة من خطوط الخلايا. في الواقع، انعكست بعض العلاقات؛ فالعلامة نفسها H3K27me3 التي ألمحت إلى حساسية للأكلاروبسين في الأطباق ارتبطت بحساسية أقل في الخلايا المشتقة من الفئران.
شبكة متغيرة بدلاً من كود ثابت
لفهم هذا التفاوت، درس الفريق كيف ترتفع وتهبط علامات هيستون مختلفة معًا عبر النماذج. في العينات المستمدة من المرضى، تحركت العديد من العلامات بتناسق وثيق، مكونة شبكة كثيفة من الارتباطات الإيجابية، بينما كانت هذه الشبكة في خطوط الخلايا أرخى وأكثر تفككًا. جلست علامات معينة في مراكز هذه الشبكات في نظام واحد لكنها لم تكن كذلك في الآخر. تدعم هذه الأنماط الفكرة القائلة إن علامات الهيستون تعمل كجزء من لغة تعتمد على السياق، حيث تعتمد دلالة أي علامة واحدة على جيرانها والبيئة الخلوية. يبدو أن النمو طويل الأمد في طبق يعيد توصيل هذه اللغة بطرق تغير كيفية ارتباط أنماط الهيستون باستجابة الدواء.
ما الذي يعنيه هذا لرعاية اللوكيميا المستقبلية
ترسم هذه الدراسة إطارًا لاستخدام مطيافية الكتلة لقراءة المشهد الغني لعلامات الهيستون في اللوكيميا اللمفاوية الحادة للخلايا التائية وربطها بكيفية تعامل الخلايا مع الأدوية فوق الجينية. كما تقدم رسالة تحذيرية: قد لا تتنبأ نتائج خطوط الخلايا القياسية باستجابات النماذج المستمدة من المرضى، ناهيك عن الأشخاص، بشكل موثوق. لكي ترشد المؤشرات المستندة إلى الهيستون العلاجات الشخصية، سيحتاج الباحثون إلى احتضان هذه التعقيدات، والتركيز على تراكيب من العلامات، والاختيار الدقيق لنماذج المرض التي تعكس بيولوجيا المرضى بأكبر قدر ممكن من الدقة.
الاستشهاد: Corveleyn, L., Provez, L., Satilmis, O. et al. Profiling histone post-translational modifications to identify signatures of epigenetic drug response in T-cell acute lymphoblastic leukemia. Sci Rep 16, 15029 (2026). https://doi.org/10.1038/s41598-026-44665-4
الكلمات المفتاحية: اللوكيميا اللمفاوية الحادة للخلايا التائية, الأدوية فوق الجينية, تعديلات الهيستون, نماذج المستزرَع من المرضى, مؤشرات استجابة الدواء