Clear Sky Science · es
Perfilado de modificaciones postraduccionales de histonas para identificar firmas de respuesta a fármacos epigenéticos en la leucemia linfoblástica aguda de células T
Por qué importa este estudio sobre el cáncer
El tratamiento de niños y adultos con leucemia linfoblástica aguda de células T ha mejorado mucho, sin embargo muchos pacientes siguen recayendo o sufren efectos secundarios graves por la quimioterapia intensa. Los médicos necesitan mejores formas de predecir qué medicamentos funcionarán en cada paciente. Este estudio explora si pequeñas marcas químicas en las proteínas que empaquetan el ADN en las células leucémicas pueden ayudar a pronosticar cómo responderán esas células a fármacos modernos que actúan sobre la maquinaria epigenética celular.
El código oculto en el empaquetamiento del ADN
Dentro de cada célula leucémica, el ADN se envuelve alrededor de proteínas llamadas histonas, formando una estructura compacta conocida como cromatina. Las histonas llevan muchas pequeñas marcas químicas que actúan como interruptores, ayudando a activar o desactivar genes sin cambiar la secuencia de ADN subyacente. Debido a que estas marcas son reversibles, son dianas atractivas para fármacos. Varios de estos «epifármacos» ya se usan en cánceres hematológicos, pero su papel en la leucemia de células T sigue sin estar claro, y los médicos carecen de marcadores sencillos para predecir quién se beneficiará de ellos.
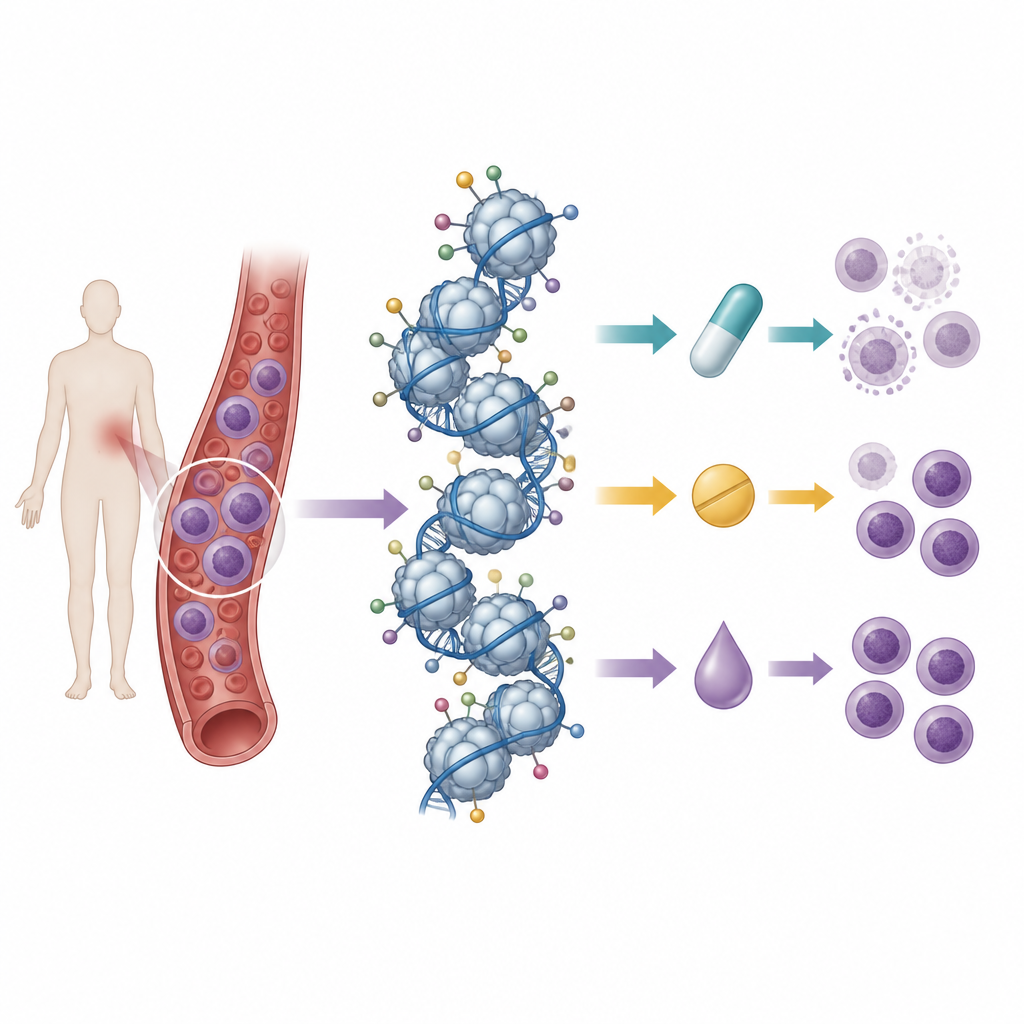
Leer muchas marcas de histonas a la vez
Los investigadores se basaron en un esfuerzo previo en el que habían cartografiado el patrón basal de marcas de histonas en 21 líneas celulares de leucemia de células T usando espectrometría de masas, una técnica que puede medir cientos de marcas químicas a la vez. Luego trataron estas líneas celulares con nueve fármacos: tres antraciclinas de quimioterapia estándar, tres fármacos que bloquean las histona desacetilasas y tres que inhiben enzimas de metilación del ADN. Al comparar la supervivencia celular tras el tratamiento con los patrones iniciales de histonas, buscaron «firmas» de marcas que se correlacionaran con sensibilidad o resistencia a cada fármaco.
Lo que revelaron las líneas celulares
En células en cultivo surgieron firmas de histonas distintas. Para las antraciclinas, ciertas marcas represivas, como una llamada H3K27me3, tendían a ser más altas en las líneas más sensibles, mientras que otras marcas, especialmente varios grupos dimetilo, se asociaron con peor respuesta. Para los fármacos que actúan sobre la metilación del ADN, niveles altos de algunos dimetilos volvieron a señalar resistencia, mientras que las marcas de acetilación en las colas de las histonas se asociaron con mejor respuesta. Los inhibidores de histona desacetilasas mostraron una separación más débil entre líneas sensibles y resistentes, pero aún aparecieron algunos patrones, incluidas marcas específicas enriquecidas en las células menos o más responsivas. En conjunto, estos hallazgos sugirieron que el paisaje combinado de marcas de histonas, más que cualquier marca individual, contiene información sobre cómo responden las células leucémicas a los fármacos epigenéticos.
Poner a prueba una sola marca
Puesto que trabajos anteriores habían sugerido que la aclarubicina funciona especialmente bien en células ricas en la marca H3K27me3, el equipo probó esta idea directamente. Utilizaron otro fármaco para bloquear la enzima que escribe esta marca y consiguieron reducir H3K27me3 en varias líneas de leucemia de células T. Sorprendentemente, esto no cambió la sensibilidad de las células a la aclarubicina. También observaron líneas celulares que naturalmente tenían alta H3K27me3 pero eran resistentes. Esto mostró que, aun cuando una sola marca de histona se correlacione con la respuesta a fármacos en algunos contextos, no es suficiente por sí sola para explicar la sensibilidad.
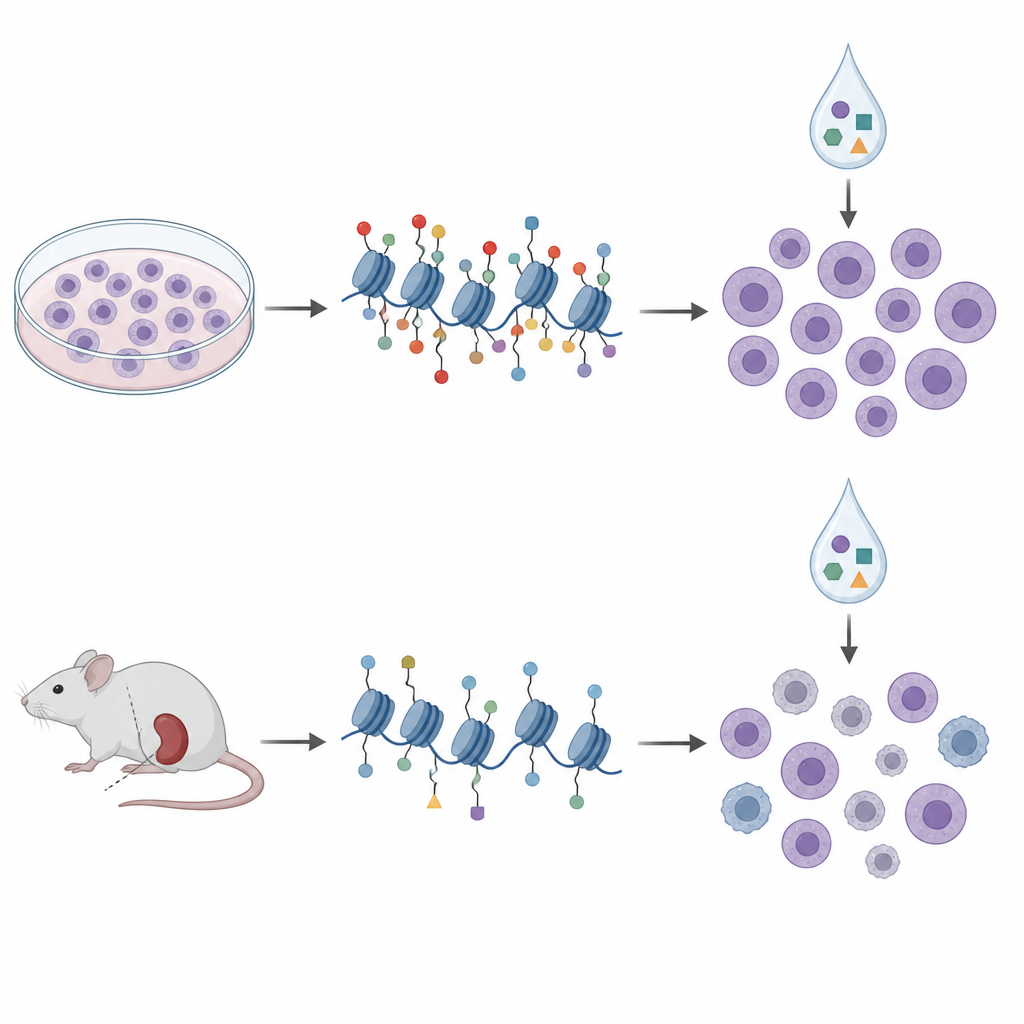
De los platos a los modelos en ratón
Para acercarse más a la clínica, los investigadores recurrieron a xenoinjertos derivados de pacientes, en los que células leucémicas procedentes de pacientes crecen en ratones inmunodeficientes. Perfilizaron marcas de histonas y la metilación del ADN en células de diez modelos de este tipo y las trataron con un panel similar de epifármacos fuera del organismo. En estas muestras, los patrones de histonas se agruparon en cuatro clústeres que reflejaban en gran medida subtipos genéticos conocidos y estados más amplios de metilación del ADN, lo que sugiere que el perfilado de histonas captura biología significativa de la enfermedad. Pero cuando compararon de nuevo las marcas de histonas con la sensibilidad a fármacos, las firmas obtenidas en líneas celulares no se trasladaron. De hecho, algunas relaciones invirtieron su dirección; la misma marca H3K27me3 que apuntaba a sensibilidad a la aclarubicina en cultivo se asoció con menor sensibilidad en las células derivadas de ratones.
Una red cambiante en lugar de un código fijo
Para entender este desacuerdo, el equipo estudió cómo distintas marcas de histonas suben y bajan conjuntamente a través de los modelos. En las muestras derivadas de pacientes, muchas marcas se movían en estrecha coordinación, formando una densa red de correlaciones positivas, mientras que en las líneas celulares esta red era más laxa y fragmentada. Ciertas marcas ocupaban nodos centrales de estas redes en un sistema pero no en el otro. Estos patrones apoyan la idea de que las marcas de histonas operan como parte de un lenguaje dependiente del contexto, donde el significado de una marca depende de sus vecinas y del entorno celular. El crecimiento a largo plazo en cultivo parece reconfigurar ese lenguaje de formas que cambian cómo los patrones de histonas se relacionan con la respuesta a fármacos.
Qué implica esto para la atención futura de la leucemia
Este trabajo traza un marco para usar espectrometría de masas para leer el rico paisaje de marcas de histonas en la leucemia de células T y vincularlas con la manera en que las células manejan los fármacos epigenéticos. También transmite un mensaje de cautela: los resultados en líneas celulares estándar pueden no predecir de forma fiable las respuestas en modelos más realistas derivados de pacientes, y mucho menos en personas. Para que los biomarcadores basados en histonas guíen tratamientos personalizados, los investigadores deberán aceptar esta complejidad, centrarse en combinaciones de marcas y elegir cuidadosamente modelos de enfermedad que reflejen la biología de los pacientes lo más fielmente posible.
Cita: Corveleyn, L., Provez, L., Satilmis, O. et al. Profiling histone post-translational modifications to identify signatures of epigenetic drug response in T-cell acute lymphoblastic leukemia. Sci Rep 16, 15029 (2026). https://doi.org/10.1038/s41598-026-44665-4
Palabras clave: leucemia linfoblástica aguda de células T, fármacos epigenéticos, modificaciones de histonas, xenoinjertos derivados de pacientes, biomarcadores de respuesta a fármacos