Clear Sky Science · sv
Profilering av histoners posttranslationella modifieringar för att identifiera signaturer för epigenetisk läkemedelsrespons vid T-cells akut lymfatisk leukemi
Varför denna cancerstudie är viktig
Behandlingen för barn och vuxna med T‑cells akut lymfatisk leukemi har förbättrats avsevärt, men många patienter drabbas fortfarande av återfall eller svåra biverkningar från intensiv cytostatikabehandling. Läkare behöver bättre sätt att förutsäga vilka läkemedel som fungerar för vilken patient. Denna studie undersöker om små kemiska märken på DNA‑packningsproteiner i leukemiceller kan hjälpa till att förutsäga hur dessa celler svarar på moderna cancerläkemedel som verkar på cellens epigenetiska maskineri.
Den dolda koden på DNA‑packningen
I varje leukemicell är DNA lindat runt proteiner som kallas histoner och bildar en kompakt struktur som kallas kromatin. Histoner bär många små kemiska märken som fungerar som strömbrytare och hjälper till att slå på eller av gener utan att förändra den underliggande DNA‑sekvensen. Eftersom dessa märken är reversibla är de attraktiva mål för läkemedel. Flera sådana ”epiläkemedel” används redan vid blodcancer, men deras roll i T‑cellsleukemi är fortfarande oklar, och läkare saknar enkla markörer för att förutsäga vilka som kommer att ha nytta av dem.
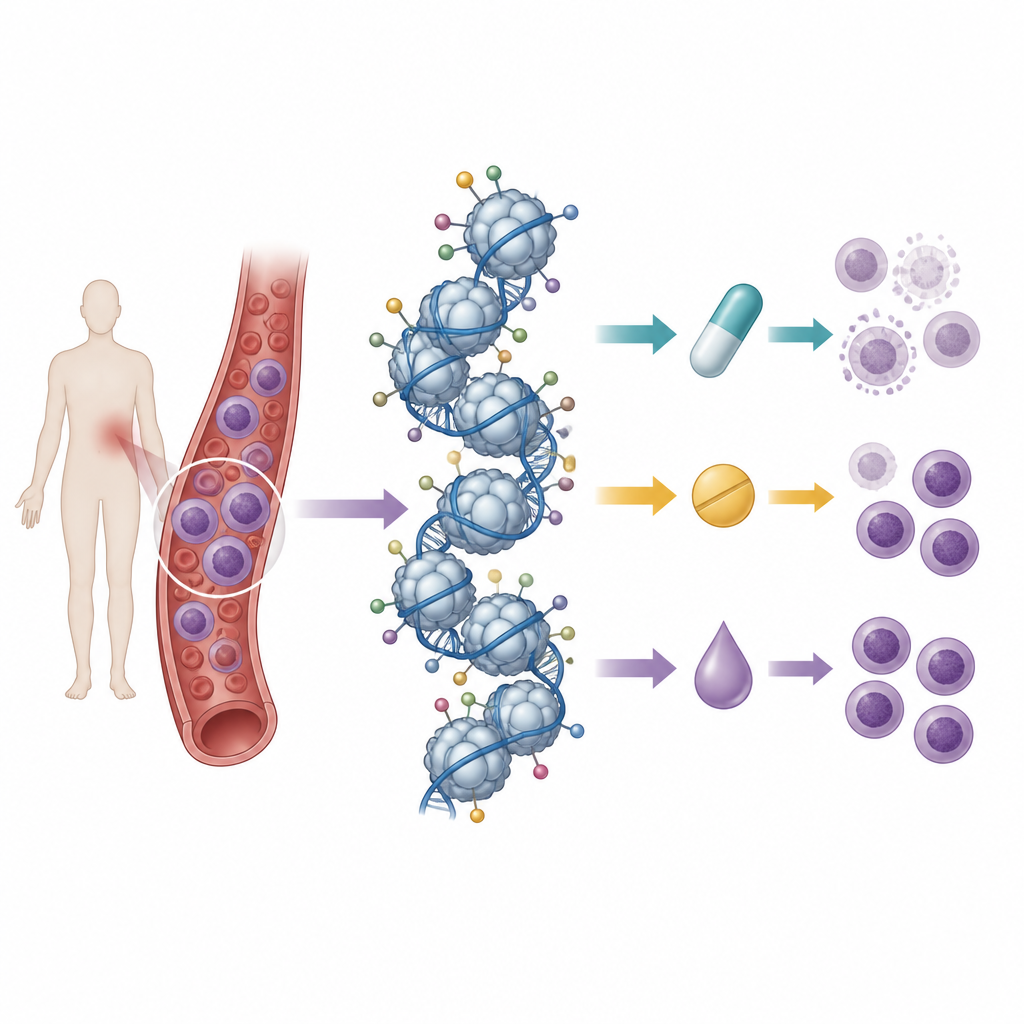
Läsa många histonmärken samtidigt
Forskarna byggde vidare på ett tidigare arbete där de kartlagt baslinjemönstret av histonmärken i 21 T‑cellsleukemicellinjer med masspektrometri, en teknik som kan mäta hundratals kemiska märken samtidigt. De behandlade dessa cellinjer med nio läkemedel: tre standard‑antracykliner, tre läkemedel som blockerar histondeacetylaser och tre som hämmar DNA‑metyleringsenzym. Genom att jämföra cellsurvival efter behandling med de ursprungliga histonmönstren sökte de efter ”signaturer” av märken som korrelerade med känslighet eller resistens mot varje läkemedel.
Vad cellinjerna avslöjade
I odlade celler framträdde tydliga histonsignaturer. För antracykliner tenderade vissa repressiva märken, såsom H3K27me3, att vara högre i mer känsliga linjer, medan andra märken, särskilt flera dimetylgrupper, var kopplade till sämre respons. För läkemedel som riktar sig mot DNA‑metylering pekade höga nivåer av vissa dimetylmärken återigen mot resistens, medan acetylmärken på histontails var förknippade med bättre respons. Histondeacetylashämmare visade en svagare separation mellan känsliga och resistenta cellinjer, men vissa mönster framkom ändå, inklusive specifika märken som var förhöjda i antingen de minst eller mest responsiva cellerna. Sammantaget tyder dessa fynd på att det samlade landskapet av histonmärken, snarare än något enskilt märke, bär information om hur leukemiceller svarar på epigenetiska läkemedel.
Sätta ett enskilt märke på prov
Tidigare arbete hade antytt att aclarubicin fungerar särskilt väl i celler rika på H3K27me3‑märket, så teamet testade denna idé direkt. De använde ett annat läkemedel för att blockera enzymet som skriver detta märke och lyckades sänka H3K27me3 i flera T‑cellsleukemicellinjer. Överraskande nog förändrade detta inte cellernas känslighet för aclarubicin. De observerade också cellinjer som naturligt hade höga nivåer av H3K27me3 men ändå var resistenta. Detta visade att även när ett enskilt histonmärke korrelerar med läkemedelsrespons i vissa sammanhang är det inte tillräckligt i sig för att förklara känslighet.
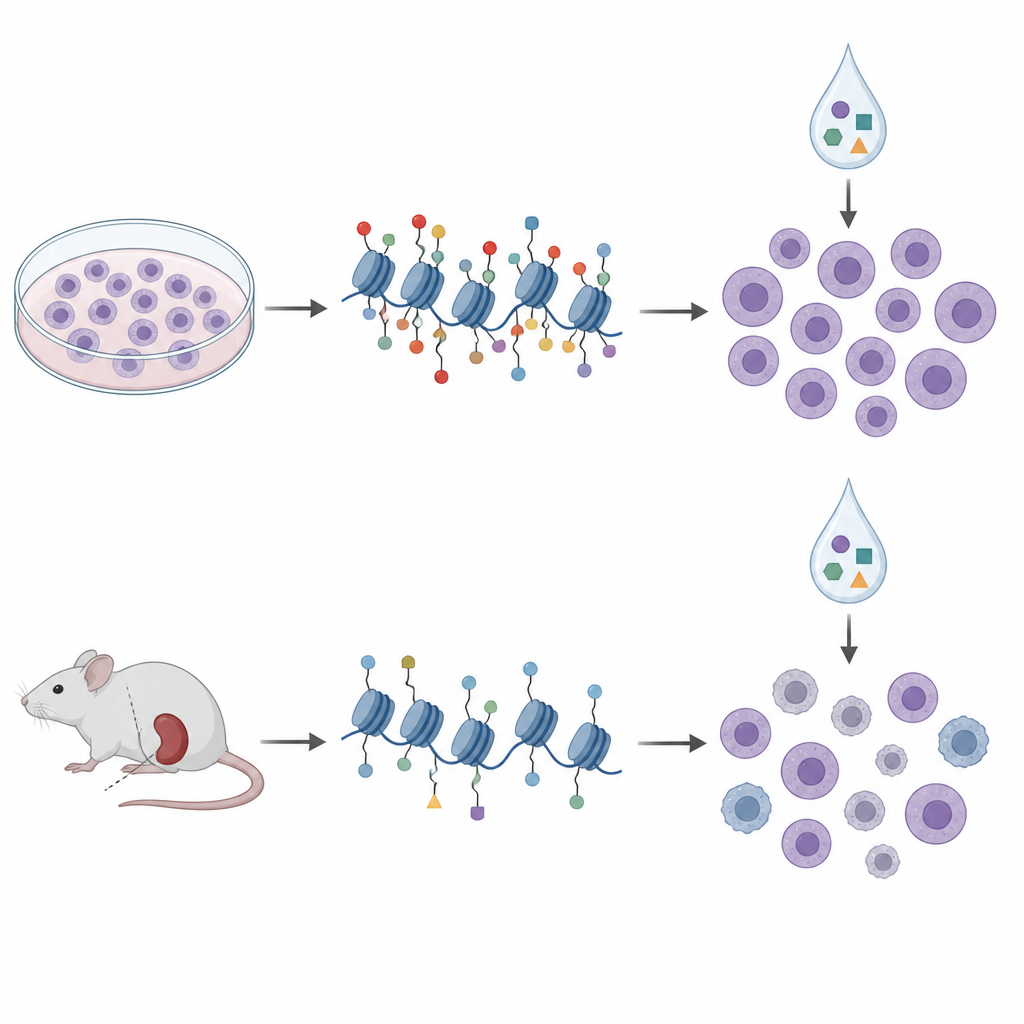
Från petriskålar till musemodeller
För att komma närmare kliniken vände sig forskarna till patient‑härledda xenograft‑modeller, där leukemiceller från patienter växer i immundefekta möss. De profilerade histonmärken och DNA‑metylering i celler från tio sådana modeller och behandlade dem med ett liknande panel av epigenetiska läkemedel utanför kroppen. I dessa prover grupperade sig histonmönstren i fyra kluster som till stor del speglade kända genetiska subtyper och bredare DNA‑metyleringsstatus, vilket antyder att histonprofilering fångar meningsfull sjukdomsbiologi. Men när de återigen jämförde histonmärken med läkemedelskänslighet överfördes inte signaturerna från cellinjerna. Faktum är att vissa samband vände riktning; samma H3K27me3‑märke som antydde känslighet för aclarubicin i odlingar var kopplat till lägre känslighet i de mus‑härledda cellerna.
Ett föränderligt nätverk snarare än en fast kod
För att förstå denna mismatch studerade teamet hur olika histonmärken steg och sjönk tillsammans över modellerna. I patient‑härledda prover rörde sig många märken i tät koordination och bildade ett tätt nätverk av positiva korrelationer, medan detta nätverk i cellinjer var lösare och mer fragmenterat. Vissa märken satt i navet av dessa nätverk i det ena systemet men inte i det andra. Dessa mönster stöder idén att histonmärken verkar som en kontextberoende språkform, där betydelsen av ett enskilt märke beror på dess grannar och cellens miljö. Långvarig odling i skålar verkar omkoppla detta språk på sätt som ändrar hur histonmönster relaterar till läkemedelsrespons.
Vad detta betyder för framtida leukemivård
Detta arbete beskriver en ram för att använda masspektrometri för att läsa det rika landskapet av histonmärken i T‑cellsleukemi och koppla dem till hur celler hanterar epigenetiska läkemedel. Det levererar också ett varningens budskap: resultat från standardiserade cellinjer förutsäger inte nödvändigtvis svar i mer realistiska patient‑härledda modeller, än mindre hos människor. För att histonbaserade biomarkörer ska kunna vägleda personanpassade behandlingar måste forskare omfamna denna komplexitet, fokusera på kombinationer av märken och noggrant välja sjukdomsmodeller som speglar patienternas biologi så troget som möjligt.
Citering: Corveleyn, L., Provez, L., Satilmis, O. et al. Profiling histone post-translational modifications to identify signatures of epigenetic drug response in T-cell acute lymphoblastic leukemia. Sci Rep 16, 15029 (2026). https://doi.org/10.1038/s41598-026-44665-4
Nyckelord: T‑cells akut lymfatisk leukemi, epigenetiska läkemedel, histonmodifieringar, patient‑härledda xenograft, biomarkörer för läkemedelsrespons